La investigación en el desarrollo embrionario humano ha alcanzado hitos significativos, permitiendo a los científicos observar y comprender fases críticas de la vida que hasta ahora permanecían ocultas. Estos avances prometen revolucionar la medicina reproductiva, ofrecer nuevas esperanzas para el tratamiento de la infertilidad y mejorar la comprensión de diversas patologías del desarrollo.
Reproducción del Desarrollo Embrionario Temprano en Laboratorio
Un equipo internacional de investigadores del IIS La Fe, Fundación IVI, Universidad de Stanford y Babraham Institute ha logrado un avance decisivo: reproducir por primera vez en el laboratorio la implantación del embrión humano hasta el día 14 de desarrollo, el límite legal para su estudio. Este logro permite observar con mayor detalle una fase clave del inicio del embarazo, hasta ahora muy limitada para la investigación científica.
“En este estudio, por primera vez, hemos conseguido una implantación embrionaria humana en el laboratorio y hemos desarrollado un modelo y con ese modelo hemos construido nuestro modelo 3D tridimensional que replica, hasta día 14, la implantación embrionaria humana”, explica el doctor Francisco Domínguez, jefe de Receptividad Endometrial y Fundación Embrionaria en Fundación IVI. Hasta ahora, este momento, uno de los más críticos del embarazo, era especialmente difícil de analizar fuera del útero, lo que limitaba el conocimiento de las causas de muchos fallos reproductivos.
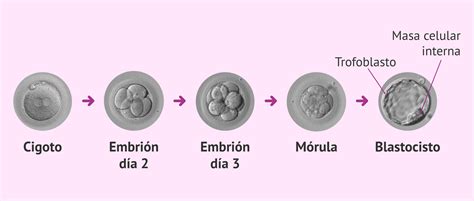
El nuevo modelo permite reproducir de forma controlada el entorno del endometrio humano durante los primeros días de desarrollo embrionario. “Ello nos va a permitir poder estudiar los casos de algunas mujeres que tienen fallo de implantación repetido por qué se produce este fallo de implantación. Vamos a coger las células de esas pacientes, las vamos a cultivar en nuestro laboratorio y vamos a determinar las razones por las cuales esas pacientes tienen estos fallos de implantación”, recalca el doctor Francisco Domínguez. Este enfoque facilitará el análisis de problemas reproductivos que afectan a un número creciente de mujeres.
Este avance abre la puerta a tratamientos más personalizados en reproducción asistida, ya que “hasta ahora, esto no se ha podido realizar porque no teníamos buenos modelos que replicarán lo que está ocurriendo en el útero humano. Obviamente, esto es muy difícil de estudiar. Esto también abre unas posibilidades de medicina personalizada en nuestro campo que hasta ahora no teníamos”. La investigación podría contribuir a mejorar la eficacia de los tratamientos y a reducir la incertidumbre en los procesos reproductivos.
Desvelando la "Caja Negra" del Desarrollo Embrionario: La Gastrulación
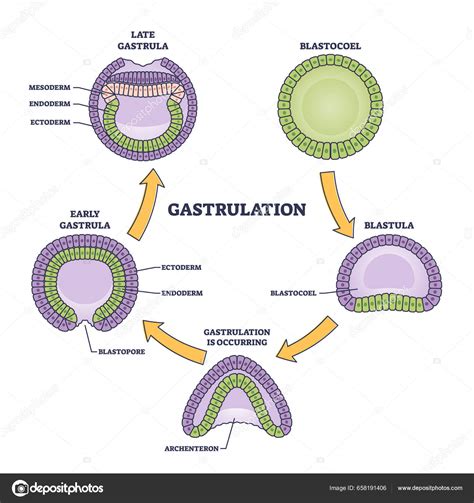
Entrar en el misterio de los primeros 28 días de vida, un periodo conocido como la "caja negra" del desarrollo embrionario, era hasta ahora imposible para la ciencia. Un hallazgo histórico ha revelado los mecanismos que forman nuestros órganos durante la gastrulación, una fase crítica que ocurre entre los días 14 y 28 del desarrollo embrionario. Durante este periodo se moldean los primeros pasos de la formación de los órganos.
Para superar las limitaciones éticas y técnicas que impedían el estudio de este periodo, un equipo utilizó embriones de macacos, que comparten una notable conservación genética y similitudes anatómicas con los humanos. Mediante inteligencia artificial y transcriptómica espacial, se capturó un mapa preciso de cómo se expresan los genes en cada célula de un embrión temprano, creando un modelo digital en tres dimensiones. Este mapa digital permite entender el origen de múltiples trastornos del desarrollo.
Un estudio, con participación del Consejo Superior de Investigaciones Científicas (CSIC) y del Centro Nacional de Investigaciones Cardiovasculares, aporta nuevos datos sobre la red de genes asociadas al gen p63, implicado en multitud de procesos del desarrollo embrionario de vertebrados y que, en caso de presentar alteraciones en su función, se asocia a patologías clínicas y defectos congénitos humanos como malformaciones en las extremidades, labio leporino o defectos en la piel.
Avances en la Creación de Embrioides y Modelos de Desarrollo
Científicos de China y España han creado embrioides de primate capaces de desarrollarse hasta los 25 días, tres días después de completarse la gastrulación. Esta hazaña permite, por primera vez, observar de manera continua el desarrollo temprano de un mono, un hito relevante porque los ratones presentan diferencias clave respecto a los humanos en esta etapa. El equipo liderado por la bióloga Wang Hongmei, tras 27 años de estudios sistemáticos, logró descifrar los patrones de desarrollo de embriones normales.
Para lograrlo, los científicos partieron de células madre embrionarias de primate y las llevaron primero al estado de blastocisto. Después aplicaron una innovadora técnica de cultivo en suspensión líquida que permitió su crecimiento tridimensional y su progresión hasta alcanzar un nivel de organización comparable al de embriones reales. Los embrioides mostraron los primeros esbozos de cerebro, tubo digestivo, tejido muscular, sangre e incluso células germinales primordiales, precursoras de óvulos y espermatozoides.
Cómo se produce la fecundación | Animación 3D
Este avance no solo abre la puerta a estudiar por qué solo uno de cada tres embriones humanos llega a término, sino también a comprender el origen de muchas malformaciones congénitas cuyo origen se cree que reside precisamente en errores durante la gastrulación. Martínez-Arias subraya que muchas mutaciones cuyas consecuencias aparecen semanas después tienen su raíz en esta fase crítica, por lo que identificar su origen es clave para futuros tratamientos.
Modelos de Embrión para Entender la Formación de Órganos y Trastornos Sanguíneos
Investigadores de la Universidad de Cambridge han utilizado células madre humanas para crear estructuras tridimensionales similares a embriones, denominadas "hematoides", que replican ciertos aspectos del desarrollo humano temprano, incluyendo la producción de células madre sanguíneas. Estas estructuras autoorganizadas imitan el proceso de desarrollo de los embriones humanos, produciendo sangre después de aproximadamente dos semanas de desarrollo en el laboratorio.
El primer autor del trabajo, Jitesh Neupane, destaca que los hematoides tienen un gran potencial para comprender mejor la formación de la sangre durante el desarrollo humano temprano, simular trastornos sanguíneos como la leucemia y producir células madre sanguíneas de larga duración para trasplantes. "Nuestro nuevo modelo imita el desarrollo de la sangre fetal humana en el laboratorio", expone Neupane. Esto podría permitir estudiar cómo surgen en el útero las enfermedades que afectan a los niños pequeños, especialmente formas de leucemia, y rastrear la causa de enfermedades que los modelos animales no pueden replicar por completo.
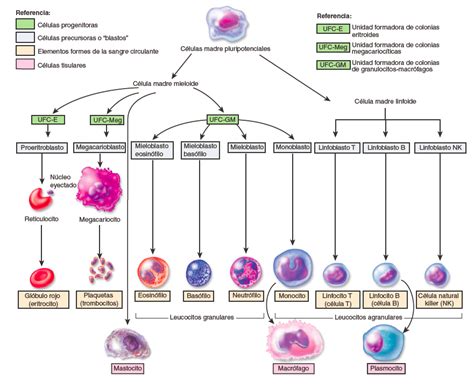
Las células madre humanas utilizadas para derivar hematoides pueden crearse a partir de cualquier célula del cuerpo, lo que tiene un gran potencial para la medicina personalizada. El nuevo método imita el proceso natural de desarrollo, basándose en un modelo autoorganizado donde el entorno de soporte intrínseco de las células impulsa la formación de células sanguíneas y células cardíacas. La capacidad de producir células sanguíneas humanas en el laboratorio marca un paso significativo hacia futuras terapias regenerativas.
Los hematoides muestran derivados de las tres capas germinales: ectodermo, mesodermo y endodermo, que establecen la base del cuerpo humano. Al decimotercer día, se observó la aparición de manchas rojas de sangre en los hematoides. Las células madre sanguíneas de los hematoides pueden diferenciarse en varios tipos de células sanguíneas, incluyendo células inmunitarias especializadas, como los linfocitos T.
Control del Desarrollo Embrionario: La Transición Materno-Cigótica
Una investigación internacional ha descubierto un proceso clave que permite al embrión “tomar el control” de su desarrollo mediante una modificación química de una proteína que activa su propio genoma y elimina las instrucciones heredadas de la madre. Este hallazgo revela un mecanismo esencial para el inicio de la vida en vertebrados y muestra que la regulación química de proteínas dirige los primeros pasos tras la fecundación.
Durante las primeras horas después de la fecundación, el embrión depende de moléculas maternas almacenadas en el óvulo. Este periodo, llamado transición materno-cigótica, termina cuando el embrión activa por primera vez su genoma, un paso crucial para que su desarrollo continúe. Cualquier fallo en este proceso puede dar lugar a problemas de implantación o malformaciones en etapas tempranas. Comprender su regulación es fundamental para entender los primeros estadios de la embriogénesis, de gran relevancia en el campo de la fertilidad.
Los investigadores utilizaron la herramienta genética CRISPR-RfxCas13d para estudiar el papel de los factores maternos. El cribado reveló que una proteína (la quinasa Bckdk) es esencial para la activación del genoma embrionario. Sin ella, el embrión no logra iniciar correctamente su desarrollo. Esta proteína actúa regulando otra proteína (Phf10) que necesita ser modificada químicamente para cumplir su función, manteniendo en equilibrio unas marcas químicas en las histonas que deciden qué genes estarán activos.
Comprender cómo se regula el inicio de la vida tiene implicaciones directas en fertilidad, pero también en procesos donde las células diferenciadas recuperan un estado de pluripotencialidad, similar al embrionario, como ocurre en el cáncer o en la regeneración de tejidos.
tags: #ultimas #noticias #sobre #desarrollo #embrionario #ciencia