La infertilidad masculina es una condición que afecta aproximadamente a la mitad de las parejas que buscan ayuda para concebir. Se define como la incapacidad de lograr un embarazo espontáneo después de un año de relaciones sexuales sin el uso de métodos anticonceptivos. Aunque históricamente se ha centrado la atención en el factor femenino, se reconoce que el factor masculino es el único responsable en el 20% de los casos y contribuye en el 50% de las ocasiones. Leen Antonio, profesora de la Universidad de Lovaina y experta en reproducción, advierte que la infertilidad masculina solo se detecta en el 11% de los casos, lo que subraya la necesidad de una evaluación integral. Un enfoque diagnóstico adecuado permite identificar una causa específica en la mayoría de los casos y ofrecer el tratamiento con mayor probabilidad de éxito.
Las principales causas médicas detrás de la infertilidad masculina incluyen desequilibrios hormonales, condiciones genéticas, infecciones, enfermedades crónicas o ciertos medicamentos. Sin embargo, en un 30-40% de los pacientes con alteraciones del espermiograma, el examen físico y las pruebas de laboratorio no logran objetivar una causa específica, clasificando a estos pacientes como portadores de infertilidad masculina idiopática.
En el pasado, muchas parejas con factor masculino severo habrían tenido que recurrir a semen de donante o considerar la adopción. Sin embargo, los avances en las técnicas de recuperación espermática, asociadas a la inyección intracitoplasmática de espermatozoides (ICSI), han permitido a numerosas parejas tener descendencia. A pesar de estos avances, existen situaciones en las que es imposible recuperar gametos viables o existe un riesgo de transmitir alteraciones genéticas a la descendencia. En estos casos, una discusión adecuada entre el especialista y la pareja es esencial para decidir la mejor conducta.
Factores de infertilidad masculina - Día a Día
Objetivos de la evaluación en el hombre infértil
La evaluación completa del hombre infértil permite al especialista:
- Tratar las alteraciones corregibles.
- Identificar las condiciones sin tratamiento específico para ofrecer técnicas de reproducción asistida utilizando espermatozoides del paciente.
- Identificar las condiciones donde será imposible recuperar gametos masculinos viables, pudiendo ofrecer técnicas de reproducción asistida con semen de donante o adopción.
- Reconocer enfermedades graves que puedan manifestarse como infertilidad.
- Diagnosticar alteraciones genéticas que puedan afectar la salud o el potencial reproductivo de la descendencia.
Evaluación del hombre infértil
Se debe realizar una evaluación del factor masculino cuando no se logra embarazo después de un año de relaciones sexuales sin protección. Esta evaluación debe adelantarse si existen factores de riesgo para infertilidad masculina (ej. criptorquidia bilateral) o femenina (ej. edad mayor a 35 años) dentro de la pareja. La edad femenina es la variable más importante para el éxito en la reproducción asistida.
Las causas de infertilidad masculina pueden ser congénitas o adquiridas, y se clasifican en patología pre-testicular (eje hipotálamo-hipófisis-gónadas), testicular o post-testicular (desde el testículo hasta los conductos eyaculadores). Se asume que la infertilidad idiopática está causada por múltiples factores, como alteraciones endocrinas, estrés oxidativo, alteraciones genéticas y epigenéticas.
Evaluación básica
La evaluación básica del paciente que consulta por infertilidad incluye:
- Anamnesis médica y sexual: Identifica factores de riesgo o hábitos de comportamiento que pueden repercutir en la fertilidad, como enfermedades previas (criptorquidia, infecciones de transmisión sexual, infecciones respiratorias a repetición), cirugías previas (inguinal, retroperitoneal o genital), historia reproductiva de la pareja, hábitos sexuales, alteraciones de la libido, disfunción eréctil y alteraciones de la eyaculación. También se revisan los fármacos, drogas y exposiciones ambientales a tóxicos.
- Examen físico: Se inicia con una inspección general del paciente para buscar alteraciones del hábito corporal, caracteres sexuales secundarios, ginecomastia o cicatrices de cirugías. Se examina el pene (posición del meato urinario, estigmas de ITS), se palpan los testículos (tamaño, consistencia, induraciones) y los epidídimos (dilatación, induración, dolor). La identificación de ambos conductos deferentes es crucial, ya que su ausencia puede indicar agenesia congénita bilateral de conductos deferentes (CBAVD) o alteraciones embrionarias del conducto mesonéfrico (asociado a agenesia renal ipsilateral). El examen finaliza con un tacto rectal para evaluar los reflejos espinales a nivel sacro.
- Dos espermiogramas: El análisis de los parámetros seminales es la piedra angular de la evaluación andrológica. Las muestras se recolectan en el hogar o laboratorio, se mantienen a temperatura ambiente y se analizan en una hora. El paciente debe mantener abstinencia sexual de 3 a 5 días. Los valores de referencia actuales son los publicados por la OMS en 2010.
Interpretación de los parámetros seminales
Un volumen seminal bajo (< 1,5ml) puede deberse a recolección incompleta, baja testosterona, eyaculación retrógrada u obstrucción de los conductos eyaculadores. Esta última se sospecha con un pH < 7,2 y baja fructosa.
Oligozoospermia se define como una concentración espermática bajo 15 millones/ml. No se diagnostica azoospermia (ausencia de espermatozoides) hasta centrifugar la muestra. Si se confirma, se debe diferenciar entre azoospermia obstructiva (OA) y no obstructiva (NOA).
La leucocitozoospermia (> 1 millón de leucocitos/ml) puede reflejar una infección genitourinaria. Es importante no confundir células redondas con leucocitos, ya que las primeras también incluyen células germinales inmaduras.
Astenozoospermia se define como una movilidad progresiva menor a 32% o una movilidad total menor a 40%. Es inespecífica y puede asociarse a varicocele, defectos ultraestructurales, anticuerpos anti-espermáticos o ser idiopática.
Teratozoospermia se define como menos de 4% de formas normales. Se ha relacionado con fracasos en técnicas como FIV o IUI, pero no con ICSI o embarazos espontáneos.
Estudio avanzado
Según los resultados de la evaluación básica, se puede solicitar un estudio más avanzado:
- Perfil endocrinológico: Las alteraciones del eje hipotálamo-hipófisis-gónadas son causas frecuentes de infertilidad. Una evaluación básica con FSH y testosterona está indicada en todos los pacientes con alteraciones en el espermiograma, función sexual o hallazgos clínicos sugestivos de endocrinopatía. Si la testosterona es baja, se completa con LH y prolactina. Una FSH elevada es indicativa de falla en la espermatogénesis. La prolactina es importante en pacientes con disminución de la libido, disfunción sexual, ginecomastia o galactorrea, ya que micro y macroadenomas productores de prolactina son tumores hipofisarios comunes que afectan negativamente las células productoras de gonadotropinas.
- Análisis de orina post-eyaculación: Se realiza en pacientes con volumen seminal menor a 1,5ml donde se ha descartado CBAVD e hipogonadismo. Un número significativo de espermatozoides en el pellet centrifugado indica eyaculación retrógrada.
- Ecotomografía testicular o transrectal:
- Testicular: Indicada en pacientes con dificultad para realizar un examen escrotal adecuado (obesos, cirugía escrotal previa, testículos altos o hidroceles grandes), masas testiculares sospechosas o alteraciones en el espermiograma por el mayor riesgo de cáncer testicular. Permite objetivar patología testicular, epididimaria o del cordón espermático.
- Transrectal: Indicada en el estudio de azoospermia u oligozoospermia obstructiva, especialmente en pacientes con bajo volumen seminal, pH acidótico y baja fructosa. Vesículas seminales dilatadas, conductos eyaculadores dilatados o quistes prostáticos de línea media sugieren obstrucción.
- Evaluación genética: Anormalidades cariotípicas y microdeleciones del cromosoma Y son comunes en pacientes con alteración de la espermatogénesis (6% de hombres con infertilidad presentan alteraciones cromosómicas). El síndrome de Klinefelter (47 XXY) es la anormalidad cromosómica más diagnosticada. Las microdeleciones del cromosoma Y afectan al 10-13% de pacientes con azoospermia. Las deleciones AZFa y AZFb se asocian a azoospermia no tratable, mientras que la AZFc se asocia a oligozoospermia severa con éxito de recuperación espermática del 80%, aunque la mutación se transmite a la descendencia masculina. Se recomienda consejería genética, cariotipo y microdeleciones del cromosoma Y en pacientes con azoospermia no obstructiva y oligozoospermia severa (< 5 millones por ml). El 70% de los pacientes con CBAVD sin síntomas de fibrosis quística poseen una mutación del gen CFTR.
- Pruebas especializadas: Como la fragmentación del ADN espermático.
Infertilidad masculina por factor pretesticular (endocrino)
La infertilidad masculina causada por factor pretesticular se debe a problemas en el sistema endocrino, lo que provoca una incorrecta formación de los espermatozoides, manifestándose en defectos de morfología, cantidad o movilidad. La formación de espermatozoides depende de un complejo sistema hormonal que comienza en el cerebro (hipotálamo), continúa en la hipófisis y culmina en el testículo, y que se autorregula.
Eje hormonal hipotálamo-hipófisis-testículo
El hipotálamo segrega la Hormona liberadora de gonadotropina (GnRH), que actúa sobre la hipófisis. La hipófisis, una glándula neuroendocrina, es la encargada de segregar las hormonas necesarias para la formación de espermatozoides: la Hormona Folículo Estimulante (FSH) y la Hormona Luteinizante (LH).
Dentro del testículo, las espermatogonias son las células madre que se diferencian para formar espermatozoides. Otras células esenciales para la regulación hormonal son:
- Células de Leydig: Tienen receptores específicos para la LH. Cuando la LH las estimula, producen testosterona, crucial para la espermatogénesis.
- Células de Sertoli: Son células de soporte. Cuando la FSH las estimula, también actúan sobre las células de Leydig para que secreten más testosterona.
- Células germinales o espermatogonias: Células madre que dan lugar a los espermatozoides mediante divisiones sucesivas, dependiendo de los estímulos hormonales.
Cuando los niveles de testosterona son suficientes y elevados, se inhibe la secreción de LH, que llega al cerebro e indica que los niveles son adecuados. De esta forma, se regula la secreción de GnRH y FSH, manteniendo los niveles hormonales óptimos para la espermatogénesis.
Causas de la esterilidad masculina pretesticular
El proceso hormonal debe estar perfectamente ajustado para la formación adecuada de espermatozoides. A continuación, se detallan algunas causas de esterilidad masculina por factor pretesticular:
Hipogonadismo hipergonadotrófico (primario)
Es una alteración caracterizada por una insuficiencia testicular para secretar testosterona y/o espermatozoides, a pesar de que el hipotálamo y la hipófisis funcionan con normalidad y producen suficiente FSH. El problema radica en que las células de Leydig no pueden generar suficiente testosterona, afectando la correcta generación de espermatozoides. La causa es una lesión primaria, congénita o adquirida, en los testículos.Los motivos incluyen:
- Alteraciones genéticas: Síndrome de Klinefelter (47 XXY), Síndrome de Reifenstein, Síndrome de Ullrich-Noonan, etc.
- Enfermedades sistémicas: Cirrosis hepática, insuficiencia renal crónica, etc.
- Enfermedades infecciosas.
- Alteración en el receptor de gonadotropinas.
- Otras, como fallo testicular autoinmune o anorquia (ausencia de testículos).
Como consecuencia, los testículos pueden ser pequeños y presentarse oligozoospermia u azoospermia. El tratamiento de esta alteración consiste en la aplicación directa de testosterona, ya que la estimulación del testículo no tendría sentido al ser adecuada la producción cerebral de FSH y LH.
Hipogonadismo hipogonadotrófico (secundario)
Este tipo de hipogonadismo es causado por un fallo testicular secundario a una enfermedad hipotálamo-hipofisaria, es decir, alteraciones del hipotálamo o de la hipófisis. Algunos factores causantes son:
- Daño en la hipófisis o en el hipotálamo: Debido a cirugía, lesión, tumor, radiación, etc.
- Anomalías genéticas.
- Hemocromatosis: Acumulación de hierro en el organismo.
- Estrés intenso.
- Enfermedades crónicas prolongadas.
- Consumo de drogas, medicamentos esteroides u opioides.
Una alteración heredable de este hipogonadismo es el síndrome de Kallmann, donde los pacientes pueden presentar también ausencia de olfato (anosmia). El tratamiento dependerá del origen del problema, pero una posible solución es un tratamiento sustitutivo hormonal que estimule la actuación del testículo y eleve las concentraciones de hormonas sexuales.
Diabetes
La diabetes, caracterizada por un aumento de los niveles de glucosa en sangre, provoca una reducción de la calidad de los espermatozoides. Produce alteraciones en el ADN y defectos en su reparación, lo que conlleva una acumulación de daños por fragmentación del ADN espermático en hombres diabéticos. La esterilidad masculina asociada a la diabetes se debe a cambios metabólicos o a complicaciones secundarias, como daños nerviosos o afectación de vasos sanguíneos en una diabetes no controlada y sin tratamiento.
Problemas de tiroides
La glándula tiroides, una glándula endocrina que segrega diversas hormonas, puede causar infertilidad. El hipotiroidismo o el hipertiroidismo (defecto o exceso en la producción de hormona tiroidea) provocan alteraciones en varios procesos metabólicos que afectan la maduración de los espermatozoides. Es importante tener en cuenta que en casos de bocio o nódulos donde la glándula tiroides presenta una alteración anatómica pero no funcional, la fertilidad no se ve afectada.
Hiperprolactinemia
Se refiere a niveles elevados de prolactina en sangre. Esta alteración suele derivarse de un hipogonadismo hipogonadotrófico. Un aumento de los niveles de prolactina conlleva una reducción de la secreción de FSH y LH, lo que puede producir oligozoospermia o incluso disfunción eréctil y pérdida del deseo sexual. El diagnóstico se realiza mediante un análisis de sangre por la mañana, evitando situaciones de estrés. Una vez diagnosticada, se establece un tratamiento para normalizar los niveles de prolactina y restablecer la capacidad reproductiva.
Tratamientos de la infertilidad masculina
El tratamiento de la infertilidad masculina dependerá del problema específico, y muchas veces implica una combinación de medicamentos, abordajes quirúrgicos y técnicas de reproducción asistida. En algunos casos severos, no hay tratamiento disponible.
Tratamientos no invasivos
En hombres con alteraciones en la movilidad y concentración espermática sin causa aparente, los cambios en el estilo de vida pueden mejorar la calidad del semen y aumentar las posibilidades de concepción. Estos incluyen la pérdida de peso, el aumento de la actividad física y la reducción del consumo de alcohol y tabaco. El consumo excesivo de alcohol (más de 2 bebidas alcohólicas al día) tiene un impacto negativo sobre los niveles de testosterona, que se restaura al cesar su ingesta. Asimismo, el uso de complejos vitamínicos y antioxidantes puede mejorar los parámetros del semen.
Tratamientos hormonales (Endocrinoterapia)
Los tratamientos hormonales sustitutivos se utilizan en casos de hipogonadismo hipogonadotrófico (hipogonadismo secundario), incluyendo las causas congénitas. Estos casos deben tratarse con una combinación de gonadotropina coriónica humana (hCG) y hormona foliculoestimulante (FSH) o con hormona liberadora de gonadotropina (GnRH) en pulsos mediante terapia de bomba para estimular la espermatogénesis.
- Gonadotropinas (LH y FSH): Estas hormonas estimulan la producción de esperma en los testículos. Se prescriben cuando la glándula pituitaria no produce suficientes niveles de LH y FSH. La FSH es crucial en hombres para apoyar la producción de esperma, actuando sobre las células de Sertoli. La idoneidad y eficacia dependen de la causa subyacente y las circunstancias individuales.
- Moduladores selectivos del receptor de estrógeno (SERM): Pueden mejorar la calidad del semen estimulando la glándula pituitaria para producir gonadotropinas. Su idoneidad y eficacia también dependen de la causa subyacente y las circunstancias individuales.
Es importante destacar que nunca se debe usar terapia con testosterona para el tratamiento de la infertilidad masculina, ya que las inyecciones de testosterona tienen un impacto negativo directo en la producción de esperma al suprimir el eje hipotálamo-hipófisis-gonadal.
Tratamiento del varicocele
El varicocele (dilatación de las venas que drenan el testículo) es una causa común de alteración de la fertilidad en el varón. Es necesario tratarlo en los siguientes casos:
- Varicocele en adolescentes con reducción del volumen testicular y evidencia de disfunción testicular progresiva.
- Hombres infértiles con un varicocele clínico, parámetros seminales anormales y una infertilidad de otro modo sin explicación, para mejorar las tasas de fertilidad.
No se recomienda tratar el varicocele en hombres infértiles con un análisis de semen normal ni en hombres con un varicocele subclínico.
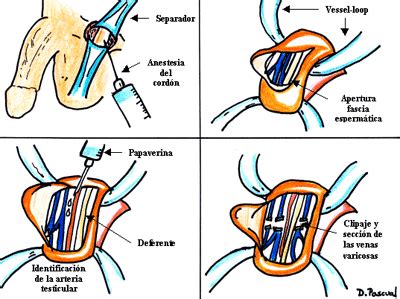
La varicocelectomía microquirúrgica es la técnica de elección. Puede considerarse en hombres con fragmentación elevada del ADN, infertilidad inexplicable o fracaso de técnicas de reproducción asistida (incluyendo pérdidas recurrentes de embarazo, fallos de embriogénesis e implantación). Esta técnica, realizada a través de una mínima incisión sobre el pubis, permite seccionar las venas dilatadas. El uso del microscopio mejora la precisión, disminuye las complicaciones y ha demostrado las mejores tasas de resolución del varicocele y mejora de la calidad del semen.
Tratamientos invasivos y técnicas de reproducción asistida (TRA)
Si los parámetros del semen no pueden mejorarse con medicamentos o cirugía, se pueden utilizar técnicas de reproducción asistida.
Azoospermia obstructiva (AO)
Es la forma menos común de azoospermia (20-40% del total). Generalmente se presenta en hombres con FSH normal, testículos de tamaño normal y aumento del epidídimo. La obstrucción puede darse a varios niveles (intratesticular, epididimaria, deferencial, conductos eyaculadores) o el conducto deferente puede estar ausente unilateral o bilateralmente. El tratamiento es esencialmente quirúrgico, buscando diagnosticar y solucionar el nivel de obstrucción. Si no es posible, el siguiente paso es la obtención de espermatozoides para TRA.
Azoospermia no obstructiva (NOA)
Se define por la ausencia de espermatozoides en al menos dos seminogramas con volumen eyaculado normal. La causa puede ser un problema en el eje hipotálamo-hipofisario-gonadal o una enfermedad testicular. La mejor opción de tratamiento es la detección y toma de espermatozoides vivos directamente de los testículos, lo cual forma parte de las terapias de reproducción asistida.
Proceso general de las TRA
Un ciclo de reproducción asistida implica varios pasos:
- Estimulación farmacológica de la mujer para producir múltiples folículos ováricos, mientras se inhibe el ciclo menstrual.
- Administración de medicación para madurar los óvulos cuando los folículos alcanzan el desarrollo adecuado, seguido de su selección y extracción.
- Obtención de material genético del hombre.
- Fertilización mediante FIV o ICSI.
- Implantación de los embriones en el útero en el momento óptimo para el endometrio.
Tipos de TRA
- Inseminación intrauterina (IIU): Se administra el semen de la pareja o de un donante directamente en el útero, con o sin estimulación ovárica, en el momento óptimo del ciclo menstrual. Requiere una adecuada calidad del semen y que la mujer tenga menos de 40 años para opciones de éxito favorables.
- Fertilización in vitro (FIV): Se realiza estimulación ovárica, se almacenan los óvulos mediante punción guiada por ecografía. Los óvulos procesados se unen al esperma y el resultado se incuba durante 2-3 días. Los embriones resultantes se implantan intraútero.
- Inyección intracitoplasmática de espermatozoides (ICSI): Se inyecta un solo espermatozoide directamente dentro del óvulo. A diferencia de la FIV, donde los oocitos se mezclan con el semen y se fecundan naturalmente, en la ICSI se inyecta un espermatozoide seleccionado a través de una micropipeta. Actualmente, es la técnica de reproducción asistida más empleada.
Es crucial que la elección de un tratamiento de fertilidad se base en los parámetros de salud reproductiva de ambos miembros de la pareja. No todos los casos de infertilidad masculina se pueden tratar eficazmente con intervenciones, lo que subraya la necesidad de más ensayos clínicos de alta calidad para mejorar la comprensión de sus causas y desarrollar intervenciones médicas destinadas a mejorar la calidad del semen.
tags: #endocrinoterapia #en #infertilidad #masculina