Existe un gran desconocimiento sobre cómo viven los embriones congelados. Lejos de las imaginaciones populares, los embriones son microscópicos y ocupan muy poco espacio. Viven en tanques con compartimentos, donde se agrupan por familias en cubiletes de plástico de diferentes colores. Dentro de estos cubiletes, se conservan en finas barritas de plástico llamadas "pajuelas", cada una capaz de albergar uno, dos o tres embriones. Estas pajuelas contienen una varilla interna etiquetada con información identificativa.
La congelación de embriones puede realizarse en diversas etapas de desarrollo, desde el día de la fecundación (una sola célula) hasta cinco o seis días después, en estadio de blastocisto, cuando ya poseen múltiples células pero conservan un tamaño reducido. Durante los primeros siete días de vida, los embriones se desarrollan dentro de la membrana externa del ovocito, similar a cómo los pollitos crecen dentro de la cáscara de un huevo. La eclosión del blastocisto ocurre cuando las células rompen esta membrana, permitiendo al embrión salir para implantarse en el útero.
El proceso de congelación tradicional de embriones dura aproximadamente unas horas. Los embriones se sumergen en una solución crioprotectora para minimizar la formación de cristales de hielo y se aspiran cuidadosamente a las pajuelas. Posteriormente, se someten a un descenso progresivo de temperatura en una máquina congeladora, alcanzando los -196°C en unos 90 minutos. Sin embargo, en la actualidad se prefiere la vitrificación, una técnica desarrollada para superar las limitaciones de la congelación tradicional, especialmente con ovocitos, que poseen una alta cantidad de agua sensible a la formación de cristales de hielo.
Una de las complejidades asociadas a la congelación y descongelación de embriones es la posible pérdida o daño celular. Si un embrión congelado en cuatro células sufre daños y queda reducido a dos, aún puede tener la capacidad de continuar su desarrollo y volver a alcanzar las cuatro células en pocas horas. No se conoce un límite de tiempo definitivo para la vida de un embrión en estado congelado; de hecho, se ha presentado el caso de un niño nacido tras 13 años y medio de congelación.
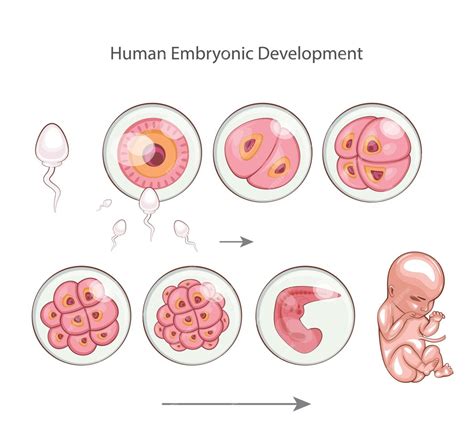
Comprendiendo la Eclosión del Blastocisto
El término eclosión se refiere a la salida del embrión de la estructura que lo envuelve. Este proceso es análogo a la salida de un pollito del huevo. En el contexto embrionario humano, la eclosión es necesaria para que el embrión pueda anidar en el endometrio uterino. Esta estructura envolvente es la zona pelúcida, una capa protectora que se mantiene hasta el estadio de blastocisto. La implantación ocurre por el contacto directo de las células embrionarias con las endometriales, no de la zona pelúcida.
La zona pelúcida es una barrera elástica y moldeable, compuesta por proteínas y azúcares, que se adapta al crecimiento del embrión. A medida que el embrión se desarrolla, la zona pelúcida se va debilitando para permitir su salida. El trofoectodermo, por su parte, es el grupo de células que invaden el endometrio, dando lugar a la placenta y formando una parte significativa de la estructura del blastocisto.
Eclosión Asistida: Una Técnica para Facilitar la Implantación
La eclosión asistida (Assisted Hatching - AH) es una técnica utilizada en laboratorios de reproducción asistida que consiste en facilitar la salida del embrión de su zona pelúcida. Esto se logra adelgazando o creando una pequeña apertura en esta capa externa para ayudar al embrión a liberarse y buscar el lugar idóneo para la implantación en el útero.
Métodos de Eclosión Asistida
Existen principalmente dos técnicas para realizar la eclosión asistida:
- Mediante láser: Utiliza un láser para crear un orificio preciso en la zona pelúcida.
- Disolución química: Emplea una solución ácida (Tyrode ácido) para disolver parcialmente la zona pelúcida.
También es posible realizar un orificio o simplemente adelgazar la zona pelúcida para facilitar la eclosión embrionaria.
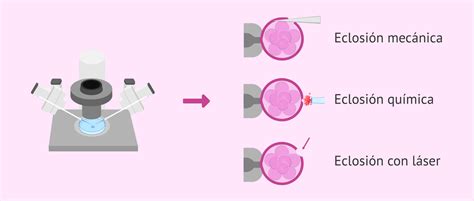
¿Cuándo se Recomienda la Eclosión Asistida?
La eclosión asistida puede ser particularmente útil en los siguientes casos:
- Mujeres entre 35 y 40 años: Algunos estudios sugieren beneficios en este grupo de edad.
- Embriones con zona pelúcida engrosada o elongada: Cuando la zona pelúcida es anormalmente gruesa o alargada, dificulta la eclosión natural.
- Embriones de ovocitos congelados: Los ovocitos congelados a veces presentan un endurecimiento de su membrana externa.
- Fracaso repetido de implantación: En casos donde ha habido múltiples intentos fallidos de implantación embrionaria.
Es importante notar que, en mujeres mayores de 40 años, la eclosión asistida podría no mejorar significativamente los resultados de implantación embrionaria.
Colapso Embrionario y su Impacto en la Implantación
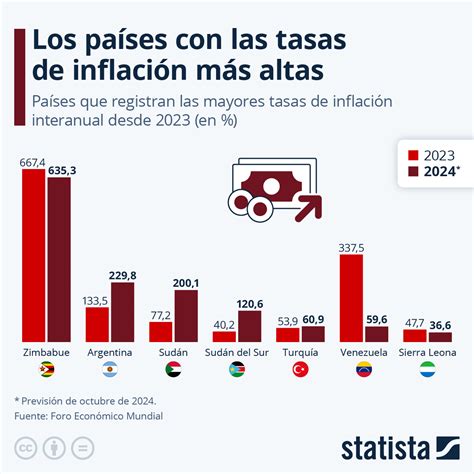
Estudios recientes, utilizando sistemas Time-Lapse, han revelado que aproximadamente el 20% de los embriones experimentan colapso durante su desarrollo embrionario. El colapso implica una pérdida temporal de volumen del embrión, lo cual puede afectar negativamente su potencial reproductivo.
La inteligencia artificial y los incubadores Time-Lapse permiten detectar de manera automática y precisa este fenómeno de colapso. Esta tecnología es crucial para identificar embriones con un menor potencial reproductivo.
A pesar del efecto perjudicial del colapso, la eclosión asistida (AH) ha demostrado optimizar el potencial reproductivo de estos embriones. Un estudio mencionado indica un incremento significativo en las tasas de gestación en embriones colapsados a los que se les realizó AH tras desvitrificarlos, igualando sus posibilidades de éxito a las de embriones que no colapsaron. Por ello, el AH se perfila como una técnica valiosa para mejorar las tasas de gestación e implantación en la rutina de los laboratorios de fecundación in vitro (FIV).
Desarrollo embrionario hasta blastocito
Fallos de Implantación Embrionaria: Causas y Soluciones
El fallo de implantación embrionaria se diagnostica cuando una paciente no logra el embarazo tras un número determinado de ciclos de FIV (con óvulos propios o de donante), siempre que se hayan transferido embriones de buena calidad, no haya habido problemas técnicos durante la transferencia y no existan anomalías uterinas evidentes.
Causas del Fallo de Implantación
Las causas pueden ser multifactoriales, incluyendo:- Causas Embrionarias: Alteraciones genéticas en el embrión o en los gametos parentales (óvulo o espermatozoide). También pueden presentarse problemas en la zona pelúcida que impidan la eclosión.
- Causas Uterinas: Infecciones crónicas del endometrio (endometritis), alteraciones endocavitarias (pólipos, miomas, tabiques, adherencias), o anomalías en la ventana de implantación (desplazamiento temporal de la receptividad endometrial).
- Causas Sistémicas: Trombofilias (alteraciones en la coagulación), o trastornos del sistema inmunológico que lleven al rechazo del embrión.
Soluciones para el Fallo de Implantación
Se han desarrollado diversas estrategias para abordar los fallos de implantación:- Cultivo largo hasta blastocisto: Permite una mejor selección embrionaria y una mayor sincronización embrión-endometrio.
- Test Genético Preimplantacional (PGT): Análisis genético del embrión para descartar anomalías cromosómicas, especialmente en mujeres de edad materna avanzada.
- Tratamiento con heparina: Indicado para mujeres con trombofilia o trastornos de coagulación.
- Test de Receptividad Endometrial (Test ERA): Determina el momento óptimo para la transferencia embrionaria al identificar posibles desplazamientos de la ventana de implantación.
- Ovodonación y donación de semen: Opciones cuando la calidad de los gametos propios es un factor limitante.
- Gestación subrogada: Una opción en casos de fallos de implantación inexplicables y recurrentes que no responden a otros tratamientos (actualmente ilegal en España).
La implantación embrionaria es un proceso complejo que requiere la sincronización endometrial y un embrión sano. De forma natural, el embrión llega al útero en estadio de blastocisto, 5 o 6 días después de la fecundación. El cultivo prolongado hasta blastocisto en el laboratorio permite una mayor selección embrionaria y, por ende, una mayor tasa de implantación, además de reducir el número de embriones "sobrantes" y la exposición del embrión a condiciones in vitro.
En casos de infertilidad sin causa aparente, donde los progenitores no presentan patologías, se puede investigar la calidad del embrión. Una membrana externa engrosada (zona pelúcida) puede dificultar la salida del embrión e impedir su adhesión al útero, frenando su evolución. La eclosión asistida, realizada por embriólogos mediante un diminuto orificio en la zona pelúcida antes de la transferencia, facilita la eclosión y aumenta las posibilidades de implantación, especialmente en casos de fracaso repetido de implantación o con embriones de ovocitos congelados.
Tipos de Hatching Asistido
- Hatching mecánico: Realización de un orificio con una aguja.
- Hatching láser asistido: Utilización de láser para un corte más preciso en la zona pelúcida.
- Hatching químico: Disolución de la zona pelúcida con soluciones ácidas.
El hatching mecánico fue el precursor de estas técnicas, pero ha sido en gran medida reemplazado por métodos más avanzados.
El estrés puede influir en el proceso de implantación, aunque su impacto exacto aún se está estudiando. El tratamiento más efectivo para lograr una implantación exitosa es aquel que genera embriones de buena calidad, sin circunstancias que disminuyan sus posibilidades de implantar, y una correcta transferencia al útero.
tags: #blastocisto #eclosion #demasiado #pronto