La placenta, un órgano vital durante el embarazo, no solo provee oxígeno y nutrientes al feto, sino que también es un intermediario crucial en la adaptación del feto a su entorno, respondiendo a factores como el estrés materno.
Marcas Epigenéticas y Estrés Materno
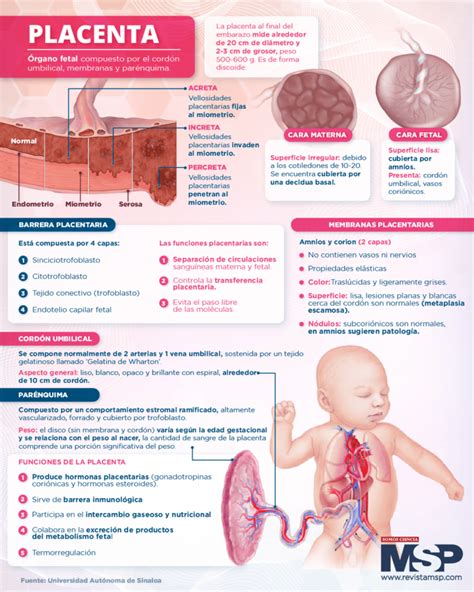
Investigaciones recientes lideradas por Lourdes Fañanás de la Universidad de Barcelona y Elisabeth Binder del Instituto Max Planck de Psiquiatría han revelado que el estrés materno puede dejar "marcas epigenéticas" en genes placentarios específicos. Estas modificaciones, que no alteran la secuencia genética en sí, sí influyen en el funcionamiento de los genes.
En un estudio piloto con 45 mujeres embarazadas primerizas y sanas, se midieron los niveles de cortisol y síntomas depresivos durante el embarazo. Tras el parto, se analizaron las placentas utilizando una técnica avanzada de secuenciación. Este método permitió identificar modificaciones en genes clave para la regulación del cortisol, como HSD11B2, NR3C1 y FKBP5. Este trabajo fue reconocido como la mejor publicación científica del mes de noviembre de 2024 por su enfoque innovador en la salud prenatal y mental, abriendo puertas a futuras investigaciones y posibles intervenciones de apoyo a embarazadas en situaciones vulnerables.
Placenta y Riesgo de Trastornos Psiquiátricos
Un equipo internacional, con participación de la Universidad del País Vasco (UPV/EHU) y el Instituto de Investigación Sanitaria Biobizkaia, ha establecido asociaciones entre modificaciones placentarias y el riesgo de desarrollar esquizofrenia, trastorno bipolar y depresión mayor. El estudio subraya el papel fundamental de la placenta en el desarrollo neuropsiquiátrico.
La investigación demostró que ciertas modificaciones epigenéticas en la placenta, específicamente la metilación del ADN, pueden influir en la expresión de genes relacionados con trastornos psiquiátricos. Esto sugiere que el riesgo genético para estas condiciones podría manifestarse incluso en la etapa prenatal.
¿Qué es la Epigenética?
La epigenética estudia los cambios en la expresión génica que no implican alteraciones en la secuencia del ADN. A diferencia de la genética, que describe las "recetas" escritas en el ADN, la epigenética se refiere a las anotaciones (subrayados, post-its) que indican qué "recetas" deben leerse y con qué frecuencia. Estos mecanismos moleculares incluyen la metilación del ADN y las modificaciones de histonas.
Estos cambios epigenéticos, influenciados por la genética y factores ambientales como la alimentación, el estrés o la exposición a contaminantes, no son permanentes y juegan un papel crucial en el desarrollo, la adaptación y la predisposición a enfermedades. Algunas de estas modificaciones pueden incluso ser heredadas.
¿Qué es la epigenética y por qué es importante?
Metilación del ADN y Trastornos Psiquiátricos
Los resultados del estudio indican que la esquizofrenia, el trastorno bipolar y la depresión mayor son las enfermedades neuropsiquiátricas con mayor relación documentada con la metilación del ADN placentario. Otros trastornos como el TDAH o el autismo muestran asociaciones menos significativas.
La profesora Nora Fernández-Jiménez de la UPV/EHU destaca que estos hallazgos refuerzan la hipótesis del origen de la esquizofrenia y otros trastornos en el neurodesarrollo, con la placenta desempeñando un rol esencial.
Medicina Personalizada y Prevención
El descubrimiento de la influencia de la metilación del ADN placentario en el riesgo genético abre nuevas vías para la prevención y el tratamiento de trastornos psiquiátricos. Identificar factores de riesgo en la etapa prenatal permitiría intervenciones tempranas y el diseño de estrategias preventivas personalizadas, como señala Ariadna Cilleros-Portet, investigadora postdoctoral en el Hospital Mount Sinai de Nueva York.
Comprender dónde y cuándo actúa cada factor genético en la patología es fundamental para la toma de decisiones terapéuticas, ya que no todos los genes asociados a un trastorno pueden ser tratados directamente en la edad adulta.
Impacto de Factores Ambientales en la Epigenética Placentaria
El entorno intrauterino moldea el desarrollo del bebé a través de mecanismos epigenéticos. Diversos factores maternos y ambientales pueden influir en estas marcas genéticas:
- Nutrición Materna: La dieta durante el embarazo es un factor epigenético clave. Nutrientes como el ácido fólico y los ácidos grasos omega-3 son esenciales para la metilación del ADN. Una nutrición deficiente puede generar "marcas" epigenéticas con posibles influencias a largo plazo en el metabolismo y la salud inmunológica del niño.
- Estrés y Ansiedad Materna: El estrés crónico o la ansiedad severa elevan los niveles de cortisol y adrenalina, que pueden cruzar la placenta. Esto puede programar epigenéticamente el sistema de respuesta al estrés del bebé, aumentando la vulnerabilidad a la ansiedad y problemas de regulación emocional.
- Bienestar y Felicidad Materna: Momentos de calma y conexión liberan hormonas como la oxitocina y endorfinas, creando un ambiente intrauterino positivo que favorece el desarrollo cerebral óptimo, fortalece el sistema inmunitario y fomenta la resiliencia del bebé.
- Exposición a Sustancias y Químicos: El consumo de tabaco, alcohol, drogas o la exposición a químicos ambientales durante el embarazo pueden generar cambios epigenéticos significativos en el feto, aumentando el riesgo de problemas de salud.
- Ejercicio Moderado: La actividad física materna contribuye a un ambiente intrauterino saludable, mejorando la circulación sanguínea y ayudando a regular el estrés del bebé.
Tabaco y Metilación del ADN Placentario
Estudios han investigado los cambios epigenéticos asociados al tabaquismo materno durante el embarazo. Se ha observado una diferente metilación del ADN en la sangre del cordón umbilical relacionada con la detoxificación de componentes del tabaco, y algunos efectos de la exposición in utero han persistido hasta la infancia, asociándose incluso con bajo peso al nacer.
Una investigación dentro del Proyecto INMA examinó la asociación entre fumar durante el embarazo y la metilación del ADN en la placenta. Se identificaron nuevas regiones con cambios asociados al tabaquismo y se apuntó a varios mecanismos subyacentes. Un descubrimiento notable fue la menor metilación en una región previamente relacionada con el crecimiento fetal, el bajo peso al nacer y el peso de la placenta, lo que subraya el impacto del tabaquismo en cambios placentarios específicos.
Restricción del Crecimiento Intrauterino (RCIU) y Epigenética
La Restricción del Crecimiento Intrauterino (RCIU) es una condición perinatal que afecta la trayectoria de crecimiento fetal, asociándose con un mayor riesgo cardiovascular, metabólico y de obesidad en la vida posnatal. Se observan cambios importantes en la función placentaria, particularmente en la molécula de óxido nítrico.
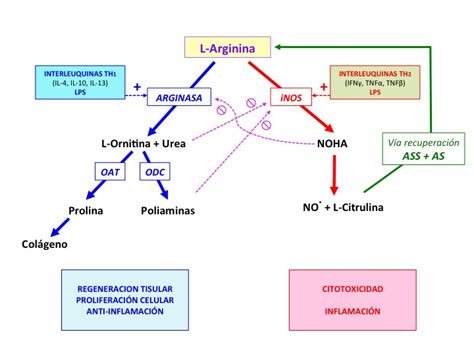
La síntesis de óxido nítrico está sujeta a control y competencia con la arginasa por el sustrato L-arginina. Esta competencia se evidencia en diversas enfermedades vasculares y en el endotelio de los vasos umbilicales de fetos con RCIU. A nivel epigenético, la metilación en regiones específicas de los promotores de genes como el de la sintasa del óxido nítrico regula su expresión.
Programación Intrauterina (DOHaH)
La asociación entre estímulos ambientales durante el desarrollo embrionario y fetal y la salud en la vida adulta explica la prevalencia de enfermedades crónicas no transmisibles. El concepto de "programación fetal", ahora conocido como "Origen Temprano de la Salud y Enfermedad" (DOHaD), postula que las condiciones perinatales adversas (malnutrición, hipoxia, tabaquismo, contaminantes) pueden inducir cambios fisiológicos y epigenéticos que configuran la salud a largo plazo.
La programación intrauterina puede ser entendida como el establecimiento de una respuesta alterada a nivel celular o sistémico como resultado de estímulos anormales durante periodos críticos del desarrollo. Estos estímulos inducen respuestas adaptativas fetales que pueden persistir, mediadas por mecanismos epigenéticos.
Función Placentaria en la RCIU
Una función placentaria adecuada es crucial para el desarrollo fetal. La disfunción placentaria es la principal causa de RCIU, parto prematuro y preeclampsia. La placenta ajusta constantemente el flujo sanguíneo para garantizar el crecimiento fetal. El óxido nítrico (NO), un vasodilatador clave sintetizado por la sintasa del NO endotelial (eNOS), juega un papel fundamental en la regulación del tono vascular placentario.
En embarazos con RCIU, la función vascular placentaria está deteriorada, con disminución del flujo placentario y aumento de la resistencia vascular en las arterias umbilicales. Las células endoteliales de la vena umbilical de fetos con RCIU presentan una expresión y actividad alterada de eNOS y del transportador de aminoácidos catiónicos-1 (hCAT1).
Regulación de la Síntesis de Óxido Nítrico
La síntesis de NO por las NOS (óxido nítrico sintasas) es un proceso complejo regulado por diversos mecanismos. La eNOS, principal fuente de NO vascular, está controlada por interacciones proteína-proteína, localización celular, modificaciones postraduccionales y la disponibilidad de sustrato y cofactores.
Fosforilación de la eNOS
Las modificaciones postraduccionales de la eNOS, como la fosforilación en residuos de serina y treonina, son mecanismos clave de regulación. La fosforilación en Thr-495 inhibe la eNOS a largo plazo, mientras que en Ser-1177 la activa. Estos estados de fosforilación, regulados por diversas quinasas y fosfatasas, reflejan la actividad de la enzima in vivo.
Arginasa-2 y su Contraste con la eNOS
Las arginasas, enzimas que metabolizan la L-arginina, pueden regular la síntesis de NO modulando la función vascular. La arginasa-2, expresada en células endoteliales humanas, compite con la eNOS por el sustrato L-arginina, contrarrestando su actividad. Su expresión puede ser inducida por hipoxia.
Metiloma Placentario y Riesgo de Obesidad Infantil
La evidencia de que el riesgo de padecer enfermedades metabólicas, como la obesidad, puede originarse antes del nacimiento a través de modificaciones epigenéticas va en aumento. Un estudio del Instituto de Investigación Biomédica de Girona (Idibgi) analizó la metilación del ADN en muestras de placenta para identificar marcas asociadas con un mayor riesgo de obesidad infantil.
Los resultados mostraron que los niveles de metilación del gen IRS1, tanto en la placenta como en la sangre de los niños, están asociados con varios indicadores de riesgo metabólico. Esto sugiere que el gen IRS1 podría ser un marcador epigenético precoz para identificar a niños con mayor riesgo de trastornos metabólicos.
El Metiloma Placentario como Firma Epigenética
El metiloma de la placenta, el conjunto de patrones de metilación del ADN placentario, es una firma epigenética única caracterizada por dominios parcialmente metilados, conservada entre mamíferos y con similitudes a los observados en cáncer. Investigaciones han empleado células madre trofoblásticas humanas para estudiar estas características.
Se descubrió la ausencia de la proteína DNMT3L, esencial para la metilación del ADN, en las células madre trofoblásticas. La introducción ectópica de DNMT3L en estas células restauró los dominios parcialmente metilados característicos del metiloma placentario, abriendo nuevas perspectivas para entender su función y relación con complicaciones del embarazo.
Aplicaciones Clínicas y Futuras Líneas de Investigación
La investigación en cambios epigenéticos en la placenta y su impacto en la descendencia es un campo en crecimiento. El estudio de cohortes longitudinales de madres embarazadas y sus hijos permite analizar la metilación del ADN en la placenta y su correlación con la salud infantil a largo plazo.
La posibilidad de desarrollar nuevas pruebas neonatales basadas en la placenta o la sangre del bebé para identificar precozmente a niños con riesgo de desarrollar enfermedades metabólicas, cardiovasculares y ciertos tipos de cáncer es un objetivo clave. La financiación de proyectos en esta línea de investigación subraya su importancia para la detección temprana y la prevención personalizada.
tags: #influencia #epigenetica #placenta