Introducción a la Salud Materno-Infantil y sus Desafíos
Las alteraciones del perímetro craneal (PC) representan uno de los muchos aspectos que el pediatra debe supervisar a lo largo del desarrollo del niño menor de dos años. Es durante esta etapa crucial de la vida cuando se requiere una vigilancia exhaustiva del crecimiento y la forma del cráneo, abordando conceptos como la macrocefalia y la microcefalia. Las anomalías en el crecimiento cerebral, ya sean congénitas o adquiridas, pueden manifestarse de forma aislada o como parte de un síndrome congénito. La detección temprana del dismorfismo craneal en Atención Primaria (AP) es fundamental. Su incidencia ha aumentado, en parte, debido a la implementación de campañas para prevenir el síndrome de muerte súbita del lactante (SMSL) en los años 90. Este dismorfismo a menudo requiere derivación especializada debido a la dificultad para distinguir entre causas posturales y sinostóticas de la deformidad.
La orientación inicial del dismorfismo craneal, determinando si es postural o sinostótica, se basa en una anamnesis detallada, exploración física y, si es necesario, derivación a neuropediatría o neurocirugía. La medición del perímetro craneal (PC) en la consulta pediátrica es tan importante como la del peso y la talla. Desde el nacimiento, el pediatra debe realizar una exploración sistemática del cráneo, incluyendo la palpación de suturas y fontanelas. Para medir el PC se utiliza una cinta flexible no distensible, buscando la mayor circunferencia desde la frente hasta el occipucio (circunferencia fronto-occipital). Dada la posibilidad de errores de medida, se recomienda realizar hasta tres mediciones.
La evolución dinámica del PC a lo largo de la edad es un factor pronóstico importante. Un cambio significativo en la desviación estándar (DS) en poco tiempo indica una mayor preocupación que un ascenso más gradual. La catalogación de macro o microcefalia varía según la fuente bibliográfica o la etnia del paciente, utilizando diferentes percentiles o valores de DS. Los pacientes con mayor desviación de la normalidad tienen una mayor probabilidad de presentar alteraciones neurológicas. Las mediciones de los primeros meses tienen un valor pronóstico limitado, ya que es durante el primer año de vida cuando se establece el valor genético del PC, acorde con el de los padres. Es importante recordar que el PC es una aproximación al volumen cefálico, especialmente el componente encefálico.
Se considera macrocefalia un PC superior a 2.5 DS. Entre sus causas se incluyen:
- Hipertensión endocraneal (HTEC) o hipertensión intracraneal (HIC), que constituye una emergencia de importancia variable según la velocidad y magnitud de su instalación.
- Aumento del parénquima cerebral (megalencefalia), que puede deberse a malformaciones primarias, como grandes circunvoluciones (patrón simple o polimicrogiria), o a alteraciones de elementos del contenido encefálico, como la sustancia blanca, por fenómenos disruptivos (infecciones, isquemia intrauterina, exposición a tóxicos) o fenómenos neurodegenerativos precoces.
- Hidrocefalia externa benigna o derrame pericerebral, muy frecuente y generalmente sin consecuencias en el neurodesarrollo. A menudo se observa una historia familiar de macrocefalia benigna. En pacientes con macrocefalia, desarrollo psicomotor y examen neurológico normales, se recomienda medir el PC de los progenitores y valorar la gráfica de evolución. La primera opción diagnóstica es la macrocefalia benigna familiar, secundaria a derrame pericerebral.
- Condiciones asociadas a holoprosencefalia, con etiología compleja que involucra factores ambientales (ej., diabetes materna) y cromosomopatías.
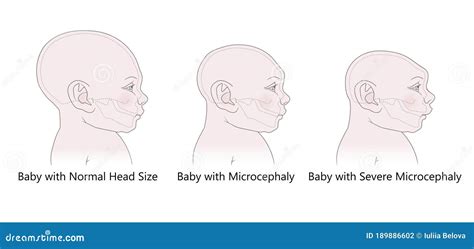
El concepto de microcefalia no está plenamente consensuado, pero se considera un riesgo importante por debajo del percentil 3 (Pc 3), especialmente desde el punto de vista pronóstico, que depende de la causa. Algunos autores la refieren a un PC inferior o igual a -2 DS o al Pc 3. Las causas pueden ser:
- Alteración de elementos del contenido encefálico, especialmente de la sustancia blanca, por fenómenos disruptivos (infecciones, isquemia intrauterina, exposición a tóxicos) o fenómenos neurodegenerativos precoces.
- Microcefalia primaria hereditaria (anteriormente microcefalia vera), caracterizada por un patrón giral simplificado y/o leve aumento del tamaño ventricular, y enfermedades de herencia autosómica recesiva que resultan en una reducción de la proliferación de neuroblastos.
Es crucial diferenciar entre lesiones estáticas que destruyen el parénquima cerebral o bloquean su crecimiento (causas adquiridas como encefalopatía hipóxico-isquémica, lesiones relacionadas con la prematuridad, infecciones congénitas, y causas genéticas) y aquellas que producen lesiones progresivas, generalmente con más manifestaciones clínicas.
Dismorfismos Craneales: Causas Posturales y Sinostóticas
Las alteraciones en la forma del cráneo son frecuentes en la revisión del niño sano. El cráneo infantil está compuesto por siete huesos planos mayores, separados por suturas craneales mayores y menores, lo que permite la adaptación durante el parto y el crecimiento posterior. Los dismorfismos craneales pueden ser de causa postural o de causa sinostótica.
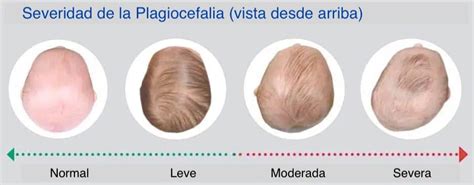
Plagiocefalia Pos tural
En la plagiocefalia postural, las suturas craneales permanecen abiertas, lo que significa que estos pacientes no presentan un riesgo aumentado de HIC. El término plagiocefalia proviene del griego "plagio" (oblicuo) y "kephalos" (cabeza), refiriéndose a deformidades craneales caracterizadas por asimetría u oblicuidad. Las plagiocefalias posicionales suelen afectar la parte posterior del cráneo. La incidencia de plagiocefalia postural aumentó significativamente tras la campaña "back to sleep" iniciada por la Academia Americana de Pediatría (AAP) en 1992 para reducir el SMSL. Estudios indican una incidencia que varía entre el 22.1% y el 37% de los recién nacidos.
Otras causas de plagiocefalia postural incluyen:
- Posición constante de "bienestar" del lactante.
- Uso prolongado de carritos y sillas, que obligan al bebé a apoyar la cabeza de la misma forma.
- Tortícolis congénita.
- Hipotonía.
- Estrabismo.
- Malformación de la unión occipito-cervical.
El diagnóstico es fundamentalmente clínico, basado en la morfología craneal y los antecedentes. La dolicocefalia, como deformidad postural, se observa típicamente en recién nacidos pretérmino de bajo peso, con cabezas alargadas y estrechas, macrocefalia relativa y ausencia de tono en la musculatura cervical. La sutura sagital permanece abierta y la deformidad suele corregirse espontáneamente alrededor de los 3-4 meses de edad si el desarrollo psicomotor es normal.
Craneosinostosis
La craneosinostosis es la fusión prematura de una o más suturas craneales, lo que impide el crecimiento normal del cráneo y puede generar aumento de la presión intracraneal, además de deformidades craneofaciales significativas. El diagnóstico clínico se basa en la palpación de suturas y fontanelas; si se detecta alguna sutura aparentemente cerrada, se sospecha craneosinostosis. La medición de valores antropométricos y el uso de índices cefalométricos ayudan a valorar el grado de alargamiento o aplanamiento del cráneo. En lactantes menores de 8-12 meses, se recomienda el uso de ecografías realizadas por radiólogos expertos.
Tipos de Craneosinostosis
- Escafocefalia: Es la forma más común (50% de las craneosinostosis), más prevalente en varones. La fusión precoz de la sutura sagital produce un cráneo alargado y estrecho. Puede presentar abombamientos frontales y occipitales compensadores y no mejora con el tiempo. Puede haber riesgo de HTEC, requiriendo seguimiento por neurocirugía y oftalmología.
- Plagiocefalia anterior sinostótica: Afecta una o ambas suturas coronales (aproximadamente 25% de las craneosinostosis), más prevalente en mujeres. Implica el cierre unilateral de la sutura coronal y otras suturas craneales, causando alteraciones frontoorbitarias, oblicuidad nasal y desviación de la raíz nasal. El peñasco temporal se malposiciona, adelantando y descendiendo el pabellón auricular.
- Plagiocefalia posterior sinostótica: Sinostosis de una sutura lambdoidea (2% de las craneosinostosis). Se asocia a un abombamiento parietal contralateral y un mínimo abombamiento frontal. El pabellón auricular del lado afectado puede estar normal o desplazado posteriormente. La cabeza adopta una forma trapezoidal vista desde el cénit.
- Trigonocefalia: Craneosinostosis asociada a malformaciones cerebrales y retraso mental. Se caracteriza por una frente en quilla, disminución del diámetro bitemporal, aumento del diámetro biparietal e hipotelorismo (cráneo triangular). Puede haber una cresta metópica visible o palpable sin alteraciones cognitivas o HTEC, siendo la intervención por motivos estéticos.
- Braquicefalia anterior: Por craneosinostosis de ambas suturas coronales, resultando en una cabeza ancha y aplanada posteriormente.
El tratamiento de las dismorfias craneales de causa sinostótica siempre requiere valoración neuroquirúrgica. En casos refractarios a las medidas iniciales, se puede emplear ortesis craneal (casco).
Avances en Medicina Reproductiva y Genética
La Unidad de Reproducción del HLA Clínica Montpellier, integrada en el Grupo UR Internacional, destaca por su laboratorio propio de Genética Reproductiva, enfocado en la investigación y aplicación de técnicas de vanguardia para mejorar los resultados en reproducción asistida. La combinación de tratamientos de Fecundación In Vitro (FIV) con procesos genéticos pioneros permite optimizar las probabilidades de éxito.
Técnicas de Diagnóstico Genético
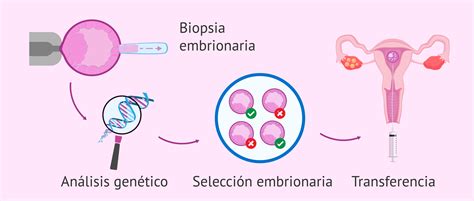
- SECURESELECT: Un innovador estudio genético que emplea cribado cromosómico no invasivo. Analiza ADN fetal libre en el medio de cultivo de los embriones para determinar su estado cromosómico con una concordancia del 80%. Los embriones se cultivan hasta el estadio de blastocisto (día 5-6) tras un lavado y transferencia a un nuevo medio.
- SECUREFIV: Combina FIV con Diagnóstico Genético Preimplantacional (DGP) mediante biopsia embrionaria para descartar alteraciones cromosómicas.
- SECURE NATAL: Test genético prenatal no invasivo en sangre materna, realizable a partir de la semana 10 de gestación.
- SECURE MATCH: Estudio genético para identificar si ambos miembros de la pareja son portadores de enfermedades genéticas recesivas, minimizando el riesgo de descendencia afectada.
La aplicación de nuevas tecnologías, como el incubador Embryoscope con sistema time-lapse, permite un registro detallado de la evolución embrionaria.
Obstetricia Moderna: Desafíos y Avances Tecnológicos
La Dra. Adelina Salazar, ginecóloga de HLA Clínica Montpellier, aborda los desafíos y avances en la obstetricia española. España registra más de 330,000 nacimientos anuales, con una edad materna media superior a los 32 años. Aproximadamente el 20% de los partos son por cesárea y el 5% de los embarazos se consideran de alto riesgo. Los retos incluyen la formación especializada y el incremento de la edad materna, que requiere un enfoque clínico específico.
Existe una mayor conciencia sobre la salud en mujeres embarazadas, impulsada por el acceso a la información. Las pacientes priorizan la alimentación saludable, el ejercicio físico y la suplementación vitamínica, evitando sustancias nocivas. Temas como la salud mental y la depresión posparto han ganado visibilidad, facilitando el acceso a atención especializada. La Dra. Salazar enfatiza la importancia de una comunicación clara, accesible y personalizada, fomentando la toma de decisiones informadas y la construcción de un plan de nacimiento conjunto.
Avances Tecnológicos en Obstetricia
- Ecografía 3D/4D: Permite visualizar el desarrollo fetal con gran detalle, facilitando la detección precoz de anomalías.
- Diagnóstico Prenatal No Invasivo: Basado en el análisis del ADN fetal libre en sangre materna, identifica alteraciones genéticas de forma segura.
- Cirugía Fetal: En desarrollo, ofrece tratamiento para patologías congénitas antes del nacimiento.
- Dispositivos Portátiles de Monitorización Fetal: Permiten el seguimiento remoto en tiempo real, útil para embarazos de alto riesgo o con dificultades de acceso a centros sanitarios.
El seguimiento personalizado del embarazo comienza con una historia clínica completa y un plan de trabajo adaptado, considerando antecedentes médicos, factores de riesgo y expectativas de la futura madre. La cualificación del personal y el acompañamiento continuo son fundamentales para detectar complicaciones tempranas, resolver dudas y fomentar un vínculo de apoyo. Los controles prenatales regulares y la educación maternal son cruciales para garantizar un embarazo seguro y un postparto con confianza.
Gestión del Embarazo y Posibles Complicaciones
El descubrimiento de un embarazo marca el inicio de un proceso que requiere atención y seguimiento adecuados. La Dra. Adelina Salazar recomienda la consulta ginecológica temprana, basándose en la fecha de la última menstruación, para evaluar el tiempo de gestación e iniciar el control prenatal. Un embarazo saludable combina atención prenatal, estilo de vida saludable y ausencia de complicaciones médicas serias. Es esencial mantener hábitos alimenticios adecuados, adecuar la actividad deportiva y asistir a todas las consultas prenatales programadas.
Complicaciones Durante el Embarazo
- Primer Trimestre: Náuseas, vómitos, hiperémesis gravídica, sangrado genital, hematomas, deficiencia de cuerpo lúteo, amenaza de aborto, inflamación o infecciones genitales. Se requiere evaluación y tratamiento especializado. Infecciones como las del tracto urinario, toxoplasmosis y de transmisión sexual son más comunes y peligrosas, requiriendo tratamientos seguros para el embarazo.
- Segundo Trimestre: Sangrado genital por placenta previa (requiere reposo absoluto y ecografías). Anemia, debido a la mayor demanda de hierro, se trata con suplementos y dieta rica en hierro. Diabetes gestacional, que afecta el metabolismo de la glucosa, se controla con dieta y ejercicio.
- Tercer Trimestre: Preeclampsia, caracterizada por hipertensión arterial y daño orgánico (riñones, hígado) después de la semana 20. Síntomas incluyen hinchazón, dolor de cabeza severo, visión borrosa y aumento rápido de peso. Requiere controles frecuentes de presión arterial y análisis de orina. En casos graves, puede ser necesario inducir el parto. Desprendimiento prematuro de placenta, que interrumpe el suministro de oxígeno y nutrientes al feto, puede requerir hospitalización y cesárea de emergencia. Parto prematuro (antes de la semana 37), con síntomas como contracciones regulares, dolor de espalda, presión pélvica y cambios en el flujo vaginal. Puede requerir reposo o medicamentos para detener las contracciones.
La identificación temprana de un embarazo de alto riesgo permite implementar medidas especiales de manejo proactivo. La clave reside en el monitoreo constante y la gestión de cualquier complicación.
Opciones de Parto y Preparación
La planificación de un parto seguro considera las necesidades y circunstancias de la mujer. Las principales opciones incluyen:
- Parto vaginal natural o con analgesia epidural.
- Parto asistido.
- Parto por cesárea: Una opción segura cuando el parto vaginal presenta riesgos. Puede programarse y evita el riesgo de desgarros perineales graves, aunque la recuperación es más prolongada.
La preparación para el parto implica cuidados médicos, educación y preparación física y emocional. Las clases de preparación al parto explican técnicas de respiración, manejo del dolor y lo que se puede esperar durante y después del proceso.
Evaluación de la Fertilidad Masculina y Genética Espermática
La presente invención se enmarca en la medicina reproductiva, centrándose en la evaluación del perfil de expresión génica de los espermatozoides para identificar biomarcadores que predigan la capacidad fecundante. Tradicionalmente, la selección de donantes de esperma se basa en análisis microscópicos (recuento, motilidad, morfología), pero estos parámetros básicos no siempre reflejan la función espermática y su valor predictivo es cuestionable. La infertilidad inexplicable, a pesar de la buena calidad del semen, sugiere la presencia de defectos moleculares.
Los espermatozoides contienen transcritos funcionalmente viables que pueden ser transferidos al oocito durante la fecundación, influyendo en el desarrollo embrionario temprano. Estos ARNm almacenados representan una "huella genética" de la espermatogénesis. Estudios han identificado diferencias en la expresión de ciertos transcritos entre hombres fértiles e infértiles, incluso con parámetros seminales normales.
Las Técnicas de Reproducción Asistida (TRA) han revolucionado el tratamiento de la infertilidad. La inseminación terapéutica con semen de donante (ITD) es una opción para la infertilidad masculina severa. Sin embargo, se observan diferencias en las tasas de embarazo entre donantes con parámetros seminales normales, lo que sugiere la existencia de subfertilidad masculina de etiología desconocida. Aún no se ha encontrado un método preciso para predecir la fecundidad del semen que complemente los análisis convencionales.
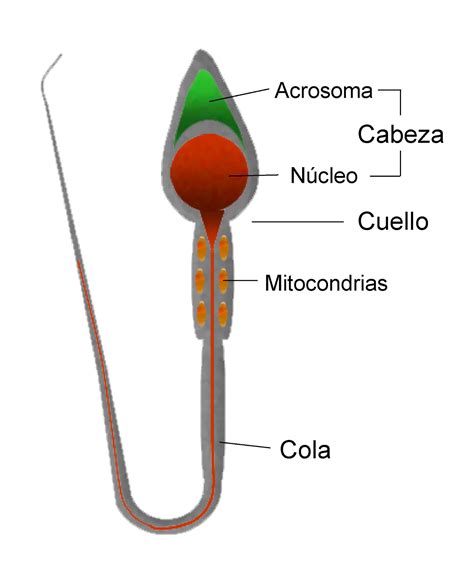
Biomarcadores Genéticos para la Fertilidad Espermática
La presente invención propone un método in vitro para predecir la capacidad fecundante de los espermatozoides mediante el análisis del perfil de expresión de un grupo específico de genes. Estos biomarcadores pueden:
- Complementar el análisis de semen convencional para predecir la capacidad fecundante en hombres con parámetros seminales normales.
- Seleccionar muestras de bancos de semen con condiciones apropiadas para reproducción asistida.
- Proporcionar información realista sobre las posibilidades de éxito en parejas con infertilidad de causa desconocida.
Se ha desarrollado un clasificador molecular del estado de fertilidad de los donantes de semen, basado en el perfil de expresión de un grupo de genes. Un modelo multiplex con los genes EIF5A, RPL13, RPL23A y RPS27A ha demostrado un 97% de sensibilidad y un 90% de especificidad para discriminar muestras con baja tasa de embarazo por inseminación intrauterina (IIU), superando la precisión de los parámetros de semen convencionales.
El método de la invención es particularmente adecuado para predecir la capacidad fecundante en técnicas de inseminación intrauterina, pero también es aplicable a otras técnicas de reproducción asistida. Los hallazgos contribuyen a la selección de marcadores genéticos valiosos para mejorar el éxito de las TRA y aumentar las tasas de embarazo.
tags: #prueba #fetal #grivado #clinica #montpellier