La investigación en el campo de la fertilidad y la reproducción asistida ha avanzado significativamente gracias a los estudios con ratones transgénicos. Estos modelos animales permiten explorar mecanismos genéticos y hormonales complejos, así como desarrollar nuevas técnicas con potencial impacto en la medicina reproductiva humana.
Producción de Hormona Folículo Estimulante (FSH) en Ratones Transgénicos
Los programas de fecundación in vitro (FIV) a menudo requieren el uso de la Hormona Estimulante del Folículo (FSH), una glicoproteína heterodimérica secretada por la glándula pituitaria, esencial para el desarrollo de las células germinales y la síntesis de hormonas esteroideas en las gónadas masculinas y femeninas. Obtener estas hormonas resulta muy costoso.
Actualmente, la FSH humana se produce mediante ingeniería genética en cultivos de células de mamíferos y se utiliza en clínica humana, principalmente en programas de fecundación in vitro. Aunque las células de mamíferos son capaces de producir esta proteína con las modificaciones post-traduccionales adecuadas, la cantidad obtenida es baja y los costes de mantenimiento de los fermentadores muy elevados.
Una alternativa, que actualmente constituye una herramienta muy útil para la obtención de proteínas terapéuticas, es la utilización de animales transgénicos como biorreactores.
Objetivo y Metodología del Estudio Austriaco
Un estudio, con la participación de M. Ballester, A. Sánchez, J. Santaló, J.M. Folch y E. Ibáñez, publicado en "Molecular Biotechnology" en septiembre de 2006, tuvo como objetivo principal obtener ratones transgénicos que expresaran la FSH humana en su glándula mamaria. En este trabajo, se insertaron las dos subunidades (α y β) del gen que codifica la FSH humana dentro de un casete de expresión, obteniendo dos construcciones independientes para cada subunidad.
A continuación, se generaron los ratones transgénicos mediante la técnica de microinyección a pronúcleo, obteniéndose un total de 9 ratones transgénicos fundadores, de los cuales 4 transmitieron los dos transgenes a su descendencia. Posteriormente, se realizó el estudio de expresión del ARNm de ambos transgenes en la glándula mamaria de ratones en lactación de las 4 líneas establecidas, obteniéndose la expresión de las dos subunidades (α y β) en todas las hembras analizadas.
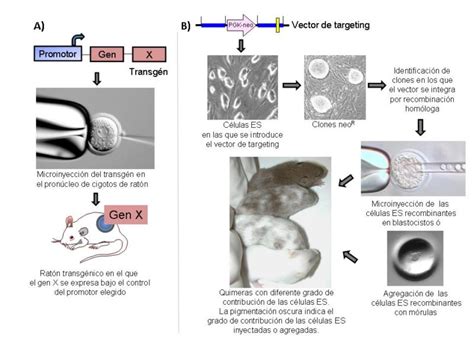
Estos resultados verifican la capacidad de las regiones reguladoras del gen de la βLG caprina de dirigir la expresión de proteínas recombinantes a la glándula mamaria de ratones transgénicos. Por último, se realizó el análisis de expresión de estas subunidades en la leche de ratones transgénicos en lactación, obteniéndose niveles muy bajos de expresión.
Estudio Austriaco sobre la Fertilidad en Ratones Alimentados con Maíz Transgénico
Un estudio financiado por los Ministerios de Agricultura y Sanidad de Austria, presentado en un seminario científico en Viena, identificó graves amenazas para la salud por el consumo de organismos modificados genéticamente (OMG). Este estudio es uno de los pocos realizados a largo plazo sobre los efectos de los transgénicos en la alimentación.
La investigación concluye que la fertilidad de los ratones alimentados con maíz modificado genéticamente se vio seriamente dañada, con una descendencia menor que los ratones alimentados con maíz convencional. Este maíz está aprobado para alimentación humana y animal en la Unión Europea y se ha cultivado de forma experimental en más de 30 municipios españoles.
Resultados y Conclusiones del Estudio
El Dr. Jürgen Zentek, Profesor de Medicina Veterinaria en la Universidad de Viena y coordinador del estudio, resumió los hallazgos: los ratones alimentados con maíz transgénico tuvieron menos descendencia en la tercera y cuarta generación, y estas diferencias fueron estadísticamente significativas. Por el contrario, los ratones alimentados con maíz no transgénico se reprodujeron de forma más eficiente.
“Los alimentos transgénicos parecen actuar como un agente de control de la natalidad, conduciendo de forma potencial a la infertilidad", comentó el Dr. Zentek. Los investigadores austriacos llevaron a cabo varios ensayos de alimentación a largo plazo con ratones durante 20 semanas. Uno de estos estudios consistió en una Evaluación de la Reproducción mediante Cría Continua (RACB, por sus siglas en inglés), en el que la misma generación de padres tuvo varias camadas de ratones.
Los progenitores fueron alimentados con una dieta que incluía un 33% de una variedad de maíz transgénico (NK 603 x MON 810), o bien a base de un maíz parecido, pero no transgénico. Esta variedad de maíz transgénico, propiedad de la multinacional Monsanto, es tolerante a un herbicida y resistente a algunos insectos. Ha sido aprobada para su cultivo en varios países, como EE.UU. o Argentina y en la Unión Europea [1] está aprobado para uso en alimentación humana y animal. En España, este maíz ha sido además cultivado de forma experimental al aire libre en más de 30 municipios los últimos tres años [2]. Estos ensayos tienen el grave riesgo de contaminar los cultivos de maíz destinados a la alimentación.
La variedad NK 603 x MON 810 es un híbrido de dos variedades transgénicas. “Este estudio es un ejemplo más de que no se puede garantizar la seguridad de los cultivos transgénicos. La toxicidad para la reproducción que presenta este maíz transgénico es un resultado totalmente inesperado", señala Amigos de la Tierra. [1] En 2005, la Agencia Europea de Seguridad Alimentaria (EFSA, por sus siglas en inglés) dio luz verde a este maíz. Sin realizar ningún estudio independiente, basándose solo en los datos de Monsanto, la EFSA afirmó “se considera improbable que el maíz NK603 x MON810 tenga ningún efecto adverso en la salud humana y animal”.
Alimentos Transgénicos
El Papel del Colesterol y la Proteína NPC2 en la Fertilidad Masculina de Ratones
En un trabajo conjunto realizado por la Dra. Silvana Zanlungo del Departamento de Gastroenterología y la Dra. Dolores Busso del Departamento de Nutrición, Diabetes y Metabolismo, se descifró que los espermatozoides de ratones deficientes en la proteína NPC2 tienen menos colesterol y una menor capacidad fertilizante in vitro.
Para ejecutar el estudio, extrajeron espermatozoides de ratones deficientes de NPC2 y los compararon con los obtenidos de ratones silvestres del mismo bagaje genético. “Medimos su contenido de colesterol y caracterizamos su morfología y función”, señaló Zanlungo. Contaron con la ayuda de Steffen Hartel y Susana Vargas de la Universidad de Chile para medir la motilidad, y de Ricardo Moreno de la Facultad de Ciencias Biológicas.
La importancia de esta investigación radica en la comprensión de cómo la deficiencia de la proteína NPC2 afecta la fertilidad masculina y la capacidad de los espermatozoides para fertilizar.
Cromosoma X y Fertilidad Masculina en Ratones
Un estudio financiado por los NIH, dirigido por Alyssa N. Kruger, doctoranda de la Facultad de Medicina de la Universidad de Michigan, y sus colegas, publicado en "Current Biology" en 2019, señala que el cromosoma X del ratón contiene dos amplicones -regiones en las que se copia un solo gen varias veces- que parecen controlar la fertilidad masculina y las proporciones del sexo de la descendencia.
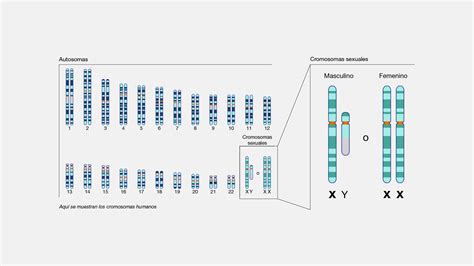
La eliminación de uno de los amplicones de los ratones favoreció a la descendencia masculina en una proporción de 60 a 40, y la eliminación de ambos suprimió la capacidad de producir espermatozoides. Entre los 23 pares de cromosomas humanos, las mujeres tienen dos cromosomas X, y los hombres tienen un cromosoma X y un cromosoma Y. En los humanos y en la mayoría de los otros mamíferos, los machos determinan el sexo de la descendencia. Los óvulos contienen un cromosoma X, mientras que los espermatozoides contienen un cromosoma X o un cromosoma Y.
Impacto de la Eliminación de Amplicones en la Fertilidad
Los investigadores crearon ratones en los que se habían eliminado ambos amplicones, lo que resultó en ratones machos infértiles. También desarrollaron un grupo de ratones que carecía del amplicón slx y otro grupo que carecía del slxl1. Cada grupo se desarrolló normalmente y produjo cantidades normales de espermatozoides.
Los ratones sin estas alteraciones genéticas tuvieron una descendencia constituida por, aproximadamente, 50 por ciento machos y 50 por ciento hembras. Sin embargo, los ratones que carecían de slxl1 engendraron aproximadamente un 60 por ciento de descendencia masculina y un 40 por ciento de descendencia femenina, a pesar de que produjeron el mismo número de espermatozoides con cromosoma X y espermatozoides con cromosoma Y.
Debido a que la eliminación de slxl1 da como resultado menos descendencia femenina, los investigadores creen que este amplicón puede controlar el desarrollo de espermatozoides con cromosoma X. "Esto nos sugiere que este gen afecta la aptitud relativa del espermatozoide X en contraposición a la del espermatozoide Y, pero no sabemos cómo", afirmó la Sra. Kruger. "Tal vez los espermatozoides con cromosoma Y nadan más rápido o en una línea más recta".
Avances en la Reproducción Uniparental en Mamíferos
La ciencia ha logrado avances notables en la reproducción de mamíferos, incluyendo la creación de descendencia a partir de dos padres del mismo sexo o incluso de un solo progenitor.
Ratones de Dos Padres Macho
Un equipo de científicos chinos especializados en células madre logró crear, mediante edición genética, el primer ratón de dos padres macho que ha llegado a la edad adulta, un hallazgo publicado en la revista científica "Cell". En este caso, los científicos chinos se decantaron por el proceso de genes de impronta, por el cual se expresa solo la copia de un gen de una persona (ya sea de la madre o del padre), mientras que la otra copia es suprimida.
Los investigadores modificaron individualmente 20 genes de impronta clave mediante diversas técnicas, descubriendo que no solo permitían crear animales bipaternos, que a veces llegaban a la edad adulta, sino que también daban lugar a células madre con una pluripotencia más estable. “Estos resultados demuestran que las anomalías en la impronta son el principal obstáculo para la reproducción unisexual de los mamíferos", afirmó Guan-Zheng Luo, coautor del estudio y profesor de la universidad Sun Yat-sen de Guangzhou, China.
"Este enfoque puede mejorar significativamente los resultados del desarrollo de células madre embrionarias y animales clonados, abriendo un camino prometedor para el avance de la medicina regenerativa", agregó el científico en un comunicado de la universidad Sun Yat-sen.
Limitaciones de la Técnica
Entre las limitaciones al avance de esta técnica, los investigadores han reconocido que solo el 11,8% de los embriones viables fueron capaces de desarrollarse hasta el nacimiento, y no todas las crías que nacieron llegaron a la edad adulta debido a defectos de desarrollo. La mayoría de los ratones de dos padres que llegaron a la edad adulta tenían un crecimiento alterado y una esperanza de vida más corta.
Lluís Montoliu, investigador en el Centro Nacional de Biotecnología (CNB-CSIC) y en el CIBERER-ISCIII, indicó que, de prosperar esta técnica, “promovería una verdadera revolución en las clínicas de reproducción asistida. Y las parejas de dos hombres o dos mujeres podrían ser los dos padres biológicos de sus hijos”. De este modo, uno de los miembros de la pareja aportaría el esperma o el óvulo y el otro miembro de la pareja aportaría células troncales pluripotentes que, siguiendo alguno de los dos procedimientos (el del equipo japonés o el del equipo chino) acabaría produciendo óvulos que podrían ser fecundados in vitro.
“Si dejamos volar la imaginación, suponiendo (lo cual es mucho suponer) que lográramos superar la consanguinidad máxima, que es viable en ratones, pero no en humanos, tanto hombres como mujeres, de forma individual, como familias monoparentales, podrían tener hijos cuya dotación genética solamente provendría de ellos o ellas mismas”, agregó el investigador.
Por el momento, estas aplicaciones en reproducción asistida humana siguen siendo ciencia ficción. En el presente, las directrices éticas para la investigación con células madre de la Sociedad Internacional de Investigación con Células Madre no permiten la edición del genoma hereditario con fines reproductivos ni el uso de gametos derivados de células madre humanas para la reproducción, ya que no se consideran seguros.
Ratones de Dos Madres Macho
Crear un mamífero -en este caso, un ratón- de dos padres del mismo sexo no es nuevo. Un equipo de investigación del centro Francis Crick de Londres, dirigido por el japonés Katsuhiko Hayashi, describió un procedimiento en la revista "Nature" en el año 2023 para convertir células pluripotentes (embrionarias o inducibles) masculinas en femeninas.
Hayashi y su equipo explicaron en la Tercera Cumbre Internacional sobre la Edición Genética en Humanos cómo pudieron convertir una célula troncal masculina en femenina. A partir de ahí, desarrollaron células ováricas para acabar obteniendo óvulos provenientes de células masculinas. Esos óvulos podían emplearse para una fecundación in vitro con esperma de otro ratón macho y obtener así embriones, que se gestaban en una ratona y daban lugar a ratoncitos aparentemente normales y fértiles, cuyos padres eran dos ratones macho.
Los resultados abrían la puerta a obtener ratones cuyo padre y madre fueran el mismo individuo, un ratón macho, que aportaría esperma normalmente y óvulos obtenidos a partir de, por ejemplo, células de su piel, para obtener embriones por fecundación in vitro. El reto era que los ratones bipaternos creados por este método se desarrollaban hasta cierto punto y luego cesaban su crecimiento.
Descendencia de una Sola Hembra (Partenogénesis)
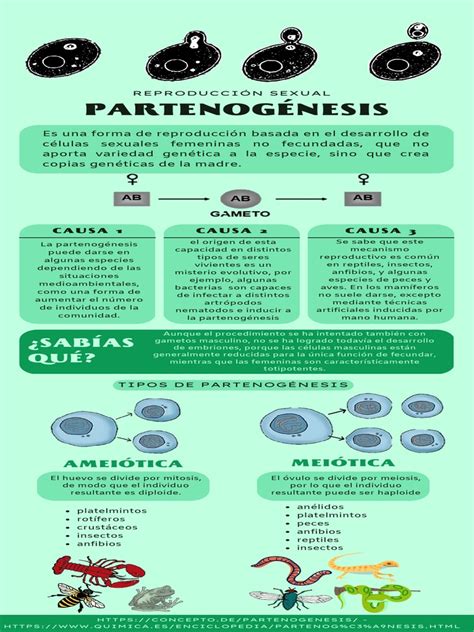
Por primera vez se ha conseguido obtener descendencia a partir de una sola hembra en mamíferos. El abordaje ha implicado una combinación de dos técnicas: la partenogénesis y la edición genética. La partenogénesis, que en griego significa “creación virgen”, es una forma de reproducción asexual que sucede de forma natural en algunas plantas y animales, pero no en mamíferos, y consiste en que el ovocito femenino sin fecundar duplica su material genético y comienza a desarrollarse como un embrión.
En mamíferos, la inducción artificial de la partenogénesis no había sido exitosa (hasta ahora) debido al fenómeno de la impronta genética, según el cual hay determinados genes inactivados en el gameto femenino y otros inactivados en el gameto masculino. Esta inactivación selectiva se consigue mediante determinados grupos químicos que actúan sobre el ADN, por lo que es una forma de regulación epigenética (del griego epi, en o sobre, -genética).
La combinación de estos dos patrones característicos del sexo es necesaria para que el individuo resultante de la fecundación sea viable. En la partenogénesis, la dotación genética viene solo de la hembra, por lo que falta la impronta genética masculina. Esta carencia había impedido hasta ahora que los pseudoembriones obtenidos por partenogénesis, llamados partenotes, pudieran evolucionar hasta el nacimiento.
Es aquí donde entra la edición genética, que se ha aplicado en este experimento para superar esta dificultad y lograrlo finalmente. Los científicos han utilizado una técnica similar a CRISPR que, en lugar de cambiar unas letras del ADN por otras, realiza cambios químicos sobre esas letras, activando o desactivando ciertos genes. Así, tras activar la partenogénesis en ovocitos de ratón, se aplicó esta herramienta de edición genética para integrar artificialmente en el genoma el patrón de impronta masculino. Así, los ovocitos empezaron a desarrollarse como un embrión.
Eficacia y Consideraciones Éticas
En un primer experimento, 192 embriones obtenidos por este medio se implantaron posteriormente en hembras de ratón subrogadas para continuar su desarrollo logrando nacer finalmente solo tres de ellos. Solo uno sobrevivió tras nacer, el cual llegó a la edad adulta y pudo reproducirse de forma normal.
Aunque la eficacia del proceso ha sido extremadamente baja, el estudio supone una prueba de concepto de que el nacimiento de individuos generados por partenogénesis en mamíferos es posible, es decir, puede obtenerse descendencia a partir de una sola madre, sin necesidad de un padre. Debe aclararse que la descendencia obtenida por este método será exclusivamente de hembras.
En 2004 ya se había conseguido obtener ratones sin necesidad de esperma ni reproducción sexual, pero en este caso se usaron dos ovocitos, uno que funcionaba como tal y otro que imitaba la aportación genética de un espermatozoide, abordaje que se perfeccionó en 2018 y permitió obtener crías de ratón a partir de células reprogramadas genéticamente procedentes de machos y hembras que se combinaron con ovocitos enucleados.
Cabe remarcar que este trabajo se ha desarrollado exclusivamente en ratones. Ningún embrión humano se ha utilizado en la investigación ni se espera que esta aplicación pueda ser usada en humanos por el momento ni en un futuro próximo. “Este trabajo es un primer paso, muy preliminar, hacia la autonomía reproductiva de la mujer”, opina Xavier Vendrell, portavoz de la Asociación Española de Genética Humana y especialista en salud reproductiva. “Trasladar estos resultados a los humanos no es ni mucho menos automático. En España, por ejemplo, sería ilegal mantener embriones de este tipo más allá de los tres días de edad. Pero es que además el programa de impronta genética humano es mucho más complejo que el del ratón.
Al margen de estas dificultades, el riesgo de que en un futuro este abordaje pueda trasladarse al ser humano, hace pertinente que nos cuestionemos la motivación del estudio. A este respecto, el artículo publicado está escasamente justificado, apenas cuenta con una línea en la discusión que afirma que “el éxito de la partenogénesis en los mamíferos abre muchas oportunidades en la agricultura, la investigación y la medicina”. A nuestro juicio, un artículo con semejantes implicaciones merecería una mayor explicación de cuáles son esos posibles beneficios que pudieran derivarse de estas investigaciones, así como alguna referencia a las cuestiones éticas que plantearía la aplicación del procedimiento en humanos, algo que no se menciona en ningún momento.
En nuestra opinión, es inexcusable alertar de los problemas éticos que implicaría generar seres humanos por partenogénesis. Por un lado, los estudios implicarían la obtención y destrucción de cientos o miles de embriones humanos, lo que nos parece éticamente inaceptable. A este respecto, conviene aclarar que, hasta ahora, la imposibilidad de progresión en su desarrollo de los pseudoembriones obtenidos por partenogénesis, debida a las grandes diferencias genéticas que los distinguen de los embriones obtenidos por fecundación sexual, relacionadas con la ausencia de la impronta masculina, habían propiciado que no fueran considerados verdaderos embriones humanos, lo que los hacía éticamente aceptables en experimentación. Pero tras este nuevo paso, por el que estas diferencias han sido en parte superadas, deberían ser considerados como verdaderos embriones, lo que añade nuevas dificultades éticas al experimento.
Además, en este caso no podrían utilizarse embriones sobrantes de tratamientos de fecundación in vitro, sino que deberían generarse específicamente para las investigaciones, lo que amplía el abanico de público que podría oponerse y de legislaciones que no permitirían estos estudios. Esta oposición podría ser incluso mayor, abarcando a algunas posiciones utilitaristas, si no se demuestran unos beneficios potenciales de suficiente entidad. Por otro lado, las niñas que nacieran fruto de esta técnica se verían privadas de padre, no solo socialmente sino también biológicamente, ya que la madre sería genéticamente madre y padre de esa niña. Esto plantea serias cuestiones sobre el bien del menor y su protección.