La infertilidad es un problema creciente en las sociedades occidentales, lo que ha llevado a un aumento en la demanda de técnicas de reproducción asistida, principalmente la fecundación in vitro (FIV). A pesar de los avances, la eficiencia global de la FIV sigue siendo baja, y uno de los factores más críticos para su éxito es la selección de embriones. El desarrollo de métodos fiables para identificar embriones con mayor potencial de implantación es uno de los principales desafíos en la reproducción humana asistida.
Métodos de Selección Embrionaria
A lo largo de la historia de la FIV, se han explorado diversos métodos no invasivos para la selección de embriones, buscando biomarcadores de implantación. Las tecnologías ómicas (genómica, transcriptómica, proteómica, metabolómica) han mostrado resultados prometedores, pero aún no se han estandarizado. El diagnóstico genético preimplantacional para el cribado de aneuploidías se ha consolidado, aunque su aplicación generalizada sigue siendo objeto de debate. Más recientemente, la tecnología time-lapse y los modelos de selección embrionaria basados en inteligencia artificial ofrecen nuevas perspectivas. Sin embargo, la selección morfológica ha sido y continúa siendo el método no invasivo más utilizado en los programas de reproducción asistida a nivel mundial.
Selección basada en la Morfología del Embrión
La selección morfológica convencional se basa en observaciones puntuales del embrión para valorar aspectos relevantes para la implantación. Estas observaciones implican la interrupción de las condiciones de cultivo controladas, lo que puede afectar a los embriones. Además, la eficacia de este método es limitada debido a la escasa correlación entre la morfología embrionaria y su potencial de implantación, así como a la variabilidad entre observadores.
Aspectos Relevantes de la Morfología del Embrión Preimplantatorio
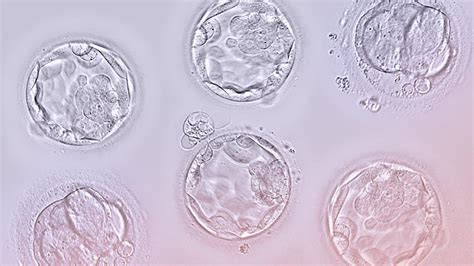
Tras la fecundación, el embrión experimenta divisiones celulares sucesivas. Hasta el estadio de 8 células, las blastómeras son distinguibles y totipotentes. A partir de ahí, comienza la compactación, donde las células aumentan el contacto entre sí y pierden la totipotencia, marcando el inicio de la transcripción del ADN y la polarización embrionaria. Posteriormente, progresa hacia el estadio de blastocisto, diferenciándose en la masa celular interna (que dará lugar al embrión) y el trofectodermo (que originará la placenta).
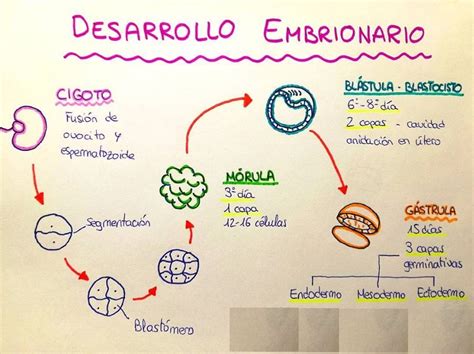
Los aspectos morfológicos evaluados incluyen la división temprana (25-27 horas postinseminación) y, entre los días 2 y 3 de desarrollo, el número y simetría de las células, el ritmo de división, el grado de fragmentación, la multinucleación y la presencia de vacuolas. Otros aspectos, como la apariencia del citoplasma o la zona pelúcida, se consideran de forma secundaria. En el cuarto día de cultivo, se evalúa el grado de compactación, y en el quinto día, la expansión del blastocele y la cohesión de las células del trofectodermo y la masa celular interna.
La clasificación de embriones hasta el día 3 (D+3) se basa en categorías que van de la A (máxima calidad y potencial de implantación) a la D (peor calidad y pronóstico). Aspectos morfológicos asociados a mal pronóstico reproductivo, como la fragmentación excesiva o la presencia de múltiples núcleos, pueden indicar una menor probabilidad de éxito. Sin embargo, la relación entre muchas de estas anomalías y el potencial de implantación no siempre es clara.
Diagnóstico Genético para el Cribado de Aneuploidías
El diagnóstico genético preimplantacional (DGP) se ha utilizado para detectar enfermedades monogénicas hereditarias y translocaciones cromosómicas. También se emplea en parejas sanas para seleccionar embriones euploides, especialmente en casos de edad materna avanzada. Inicialmente, el cribado de aneuploidías (PGS) implicaba la biopsia de una blastómera en día 3 y el análisis de cromosomas mediante hibridación in situ fluorescente (FISH).
La publicación de estudios que sugerían que el PGS en día 3 con FISH no solo no mejoraba, sino que podía disminuir, las tasas de embarazo en mujeres de edad avanzada, marcó un punto de inflexión. Se plantearon dudas sobre el efecto deletéreo de la biopsia en embriones de día 3 y las limitaciones del análisis de célula única, incluido el mosaicismo embrionario.
La estandarización de nuevas técnicas de análisis genético (PCR cuantitativa, hibridación genómica comparada, secuenciación masiva) y las mejoras en el cultivo y criopreservación de blastocistos han dado lugar a una nueva modalidad: el PGT-A (Preimplantation Genetic Testing for Aneuploidy). Los embriones biopsiados en día 5 pueden transferirse en día 6 o criopreservarse para su transferencia posterior.
WEBINAR | Selección Embrionaria
Aunque las tasas de gestación en FIV parecen ser superiores con el PGT-A en ciertos grupos de pacientes, su validación universal aún está en debate. La Sociedad Americana de Medicina Reproductiva ha señalado varios puntos en contra de su aplicación generalizada, incluyendo la extrapolación de resultados de pacientes con buen pronóstico a la mayoría, el sesgo en los estudios randomizados, la variabilidad de las metodologías de PGT-A, el diagnóstico de mosaicismo y la necesidad de estudios prospectivos que consideren las tasas de gestación acumulada por ciclo iniciado.
Conservación de Embriones Humanos
En la mayoría de los ciclos de FIV, se obtienen embriones sobrantes que, si son de buena calidad, se vitrifican para su preservación. La vitrificación es una técnica de criopreservación que combina la deshidratación progresiva de los embriones y un rápido descenso de temperatura, sustituyendo el agua por medios que protegen las estructuras celulares. Una vez conservados en nitrógeno líquido a -196°C, los embriones pueden permanecer indefinidamente sin que se produzcan reacciones fisiológicas.
La legislación española, concretamente la Ley 14/2006, regula el destino de los embriones sobrantes. Las opciones incluyen:
- Utilización propia: Para intentos fallidos o para tener un segundo hijo, evitando nuevas estimulaciones ováricas y punciones foliculares.
- Donación con fines reproductivos: Implica una adopción de embriones, requiriendo el cumplimiento de requisitos similares a los de los donantes.
- Donación con fines de investigación: Requiere un consentimiento informado específico sobre el proyecto de investigación.
- Cese de su conservación sin otra utilización: Solo aplicable cuando especialistas ajenos al centro certifican que la mujer no reúne los requisitos para la reproducción asistida.
El consentimiento informado debe ser renovado como mínimo cada dos años. La donación para adopción o investigación es menos común, en parte debido a las limitaciones de edad para la donación y la falta de respuesta de algunos pacientes a la renovación del consentimiento.
Los "embriones abandonados" surgen cuando los pacientes no renuevan su consentimiento. Tras dos renovaciones consecutivas sin respuesta y habiendo demostrado los esfuerzos para contactar, la clínica puede disponer de ellos, manteniendo la confidencialidad, el anonimato y la gratuidad.
Transferencia de Embriones Congelados vs. Frescos
La criotransferencia (transferencia de embriones congelados) resulta un proceso sencillo y económico para los pacientes, evitando muchas de las molestias de un ciclo fresco, como las inyecciones hormonales, la anestesia o los controles ecográficos frecuentes. La preparación del endometrio se puede realizar de forma natural o mediante terapia hormonal.
Aunque existe un pequeño riesgo de pérdida de embriones durante el proceso de criopreservación, las tasas de supervivencia y éxito de la vitrificación han mejorado significativamente, alcanzando hasta un 95% en algunos casos. Diversos estudios indican que no hay efectos negativos sobre las tasas de supervivencia e implantación de embriones almacenados durante varios años. De hecho, algunos trabajos sugieren que los ciclos de criotransferencia pueden incluso mejorar las tasas de gestación al lograr endometrios mejor preparados para la implantación.
En resumen, la transferencia de embriones criopreservados, especialmente cuando han superado el proceso de vitrificación con altas tasas de supervivencia, ofrece resultados comparables a los de embriones frescos, proporcionando una alternativa cómoda y eficaz para aumentar las posibilidades de embarazo.
tags: #conservacion #y #seleccion #embriones #humanos