El síndrome de hiperestimulación ovárica (SHO) es una complicación que puede surgir durante los tratamientos de reproducción asistida, particularmente en la fecundación in vitro (FIV). Se caracteriza por una respuesta exagerada de los ovarios a la medicación hormonal administrada, lo que puede dificultar todo el proceso reproductivo.
¿Qué es y cuándo aparece el SHO?
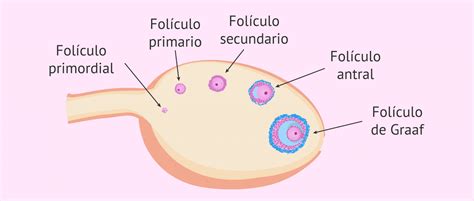
El SHO es una alteración que se manifiesta en tratamientos de reproducción asistida, siendo más común en ciclos de FIV debido a las dosis hormonales más elevadas en comparación con la inseminación artificial (IA). En un tratamiento de FIV, la paciente recibe dosis hormonales para incrementar el número de folículos que maduran, buscando obtener más de un óvulo viable. Si la respuesta ovárica es más pronunciada de lo esperado, los ovarios pueden aumentar de tamaño excesivamente y acumular líquido, desencadenando el SHO.
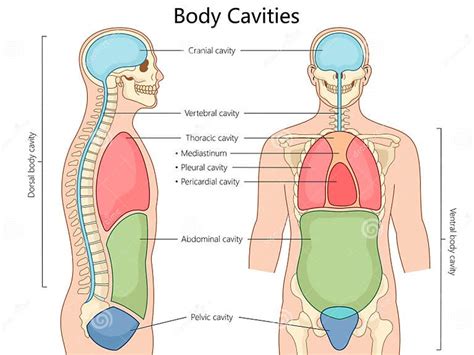
La consecuencia más significativa del SHO es la liberación de un volumen anormal de líquido hacia la cavidad abdominal y pulmonar. Un médico debe controlar esta condición mediante seguimiento ecográfico transvaginal y análisis de los niveles de estradiol en sangre para prevenir complicaciones graves.
Causas del Síndrome de Hiperestimulación Ovárica
Las causas exactas de esta reacción a la estimulación hormonal no se conocen completamente. Sin embargo, se sabe que el SHO está relacionado con la administración de gonadotropina coriónica humana (hCG), utilizada para desencadenar la ovulación. Esta hormona, administrada unas 36 horas antes de la punción ovárica, promueve cambios en los folículos y la maduración de los óvulos para optimizar la fecundación.
Previamente a la inyección de hCG, la paciente recibe gonadotropinas y análogos de la GnRH durante aproximadamente 10-12 días para estimular el crecimiento folicular. La hCG también promueve la liberación de sustancias que aumentan la permeabilidad de los vasos sanguíneos, provocando una fuga excesiva de fluidos fuera del torrente circulatorio. Esto puede comprometer la función de los sistemas hepático, hematológico, renal y respiratorio.
Es importante destacar que el SHO no aparece inmediatamente después de la administración de hCG, sino que sus síntomas se manifiestan varios días o semanas después.
Clasificación del SHO
La clasificación del SHO se realiza según su gravedad:
Clasificación por Gravedad
- Leve: Caracterizado por niveles elevados de estradiol y progesterona, y un ligero aumento del tamaño de los ovarios.
- Moderado: Además de los cambios hormonales y el aumento ovárico, la paciente experimenta malestar y distensión abdominal.
- Grave: Presenta un diámetro ovárico exagerado, niveles hormonales alterados, aumento diario de peso debido a acumulación de líquido en cavidades abdominal y torácica, y posibles problemas renales, hepáticos y trombóticos.
Existe también una clasificación según el tiempo de manifestación:
Clasificación por Tiempo de Manifestación
- Precoz: Aparece entre 3 y 7 días después de la administración de hCG.
- Tardío: Se manifiesta entre 12 y 17 días después de la inyección de hCG. Este tipo suele ocurrir cuando hay gestación, ya que el saco embrionario también produce hCG.
Ante cualquier síntoma durante la estimulación ovárica o tras la punción folicular, es fundamental consultar al médico para evaluar la severidad.
Síntomas del SHO
El SHO afecta aproximadamente al 0,6-10% de las mujeres sometidas a estimulación ovárica. Las mujeres con SHO leve o moderado suelen presentar:
- Hinchazón y dolor leve en el abdomen.
- Aumento de peso.
- Náuseas o vómitos.
- Diarrea.
En casos raros, el SHO se agrava (incidencia del 0,5-2%). Los síntomas graves incluyen los anteriores, además de aumento de la frecuencia cardíaca, dificultad para respirar, disminución de la frecuencia de micción y alteración de valores renales y hepáticos. El diagnóstico precoz es crucial para evitar complicaciones potencialmente mortales.
Complicaciones del SHO
Las complicaciones del SHO se deben principalmente a la acumulación de líquido en cavidades corporales:
- Encharcamiento de los pulmones: Puede causar problemas respiratorios.
- Torsión ovárica: El exceso de líquido abdominal puede hacer que el ovario gire sobre sí mismo.
- Desequilibrio electrolítico: La fuga de líquido del torrente sanguíneo puede alterar los niveles de sales.
- Descenso de la frecuencia y volumen de micciones: La pérdida de líquido puede llevar a insuficiencia renal.
Otros riesgos incluyen la rotura de quistes ováricos con sangrado interno y aborto espontáneo si ocurre el embarazo.
Factores de Riesgo para el SHO
Aunque cualquier mujer en tratamiento de hiperestimulación ovárica está en riesgo, ciertos factores aumentan la probabilidad de desarrollar SHO:
- Edad: Mujeres jóvenes (menores de 30 años) con ovarios más sensibles a las gonadotropinas.
- Síndrome del ovario poliquístico (SOP): Mayor propensión debido a la presencia de múltiples quistes ováricos.
- Gestación previa: Mayor predisposición en mujeres que han estado embarazadas anteriormente.
- Embarazo múltiple: La duplicación de hCG en gestaciones gemelares empeora la evolución del síndrome.
Algunos estudios sugieren una relación con un bajo índice de masa corporal, aunque hay discrepancia en la comunidad científica.
Aspectos Indicativos de Riesgo de SHO
Aunque la predicción exacta es difícil, ciertos signos pueden alertar al médico sobre un riesgo elevado:
- Estradiol sérico elevado: Niveles superiores a 2500 pg/ml o un aumento rápido durante la estimulación ovárica.
- Imagen ecográfica del "signo del collar": Distribución de folículos alrededor del ovario.
- Episodios previos de SHO: Sugiere susceptibilidad a las hormonas del tratamiento.
En caso de gestación, los niveles de hCG aumentarán, empeorando el SHO. Ante la sospecha de desarrollo del síndrome, se puede evitar la implantación en el mismo ciclo.
Prevención de la Aparición del SHO
Existen diversas estrategias para prevenir o mitigar el SHO:
Menores Dosis de Gonadotropinas
En mujeres con alto riesgo (jóvenes, con SOP o bajo IMC), se recomienda iniciar la estimulación con dosis bajas de gonadotropinas para evaluar la respuesta.
Inducción de la Ovulación con Agonistas de la GnRH
Sustituir la hCG por agonistas de la GnRH es una forma eficiente de prevenir el SHO, aunque puede disminuir la tasa de implantación y embarazo por déficit de la fase lútea.
Cancelación del Ciclo
En casos de desarrollo folicular muy rápido o niveles de estradiol excesivamente altos, se puede cancelar el ciclo para prevenir el SHO. Se debe advertir sobre la posibilidad de ovulación espontánea y la necesidad de abstinencia sexual.
Criopreservación Embrionaria
En casos de sospecha de SHO, vitrificar los embriones y transferirlos en un ciclo posterior evita el agravamiento del síndrome al no haber producción endógena de hCG por gestación.

Tratamiento del Síndrome de Hiperestimulación Ovárica
El tratamiento depende de la gravedad del SHO. Los casos leves y moderados pueden manejarse de forma ambulatoria, mientras que los graves requieren hospitalización.
Tratamiento de SHO Leve y Moderado
- Ingesta abundante de líquidos, especialmente bebidas con electrolitos.
- Reposo con piernas elevadas para prevenir trombosis.
- Evitar alcohol y cafeína.
- No realizar ejercicio intenso.
- Abstenerse de relaciones sexuales.
- Tomar analgésicos para el dolor.
Tratamiento en SHO Graves
La hospitalización es crucial para un control exhaustivo. Se administran líquidos intravenosos y, en casos severos, puede ser necesaria una paracentesis (punción para extraer líquido acumulado).
Se realiza un seguimiento riguroso de:
- Funciones hepáticas.
- Factores anticoagulantes.
- Función renal.
- Complicaciones pulmonares.
- Equilibrio hidroelectrolítico.
Las complicaciones que requieren cirugía incluyen rotura de quistes, torsión ovárica o gestación ectópica.
Relación entre las emociones y las enfermedades. Entrevista al Doctor Puig.
Epigenética y su Relación con la Reproducción Asistida
La epigenética estudia los cambios heredables en la expresión génica que no alteran la secuencia de ADN. Estos cambios pueden ser influenciados por factores ambientales (dieta, estilo de vida) y factores internos (edad, desarrollo embrionario). La epigenética regula la actividad génica mediante mecanismos como la metilación del ADN y la modificación de histonas, afectando la lectura de los genes y la susceptibilidad a enfermedades.
Estos cambios epigenéticos pueden transmitirse intergeneracionalmente y son cruciales para comprender cómo los factores ambientales y los procesos internos influyen en el desarrollo fetal.
Usos de la Epigenética
- Identificación de biomarcadores: Para detectar enfermedades o predecir riesgos.
- Desarrollo de terapias: Investigación de nuevos tratamientos, como inhibidores de la histona desacetilasa (HDAC) para el cáncer.
- Investigación del desarrollo: Estudio de cómo los factores ambientales afectan el desarrollo fetal y la susceptibilidad a enfermedades crónicas.
- Identificación de patrones de herencia: Explicación de la herencia de rasgos que no siguen las leyes de la genética clásica.
Epigenética y Embarazo: Desarrollo Prenatal
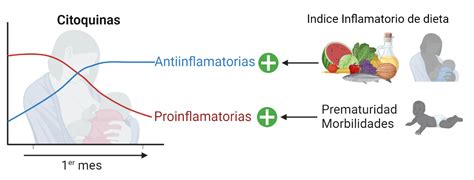
Durante el desarrollo prenatal, la epigenética juega un papel fundamental. La dieta materna puede afectar la metilación del ADN y la modificación de histonas en el feto, influyendo en el desarrollo de órganos. Dietas inadecuadas o la exposición a químicos pueden inducir cambios epigenéticos que aumentan el riesgo de enfermedades crónicas.
El estrés materno también puede tener efectos epigenéticos significativos, afectando la regulación del eje hipotalámico-pituitario-adrenal (HPA) en el feto.
Impacto de la Epigenética en la Fertilidad Femenina y Masculina
La epigenética regula la calidad de óvulos y espermatozoides, y su capacidad para generar embriones sanos:
- Fertilidad Femenina: Los cambios epigenéticos afectan la calidad de los óvulos (maduración, competencia para la fertilización) y la regulación del ciclo menstrual.
- Fertilidad Masculina: Influye en la calidad y funcionalidad de los espermatozoides (espermatogénesis, motilidad, integridad del ADN) y su capacidad de fertilización.
Relación con la Reproducción Asistida
La epigenética puede influir en la salud y el desarrollo de embriones y niños concebidos mediante técnicas de reproducción asistida. La manipulación de gametos o embriones en laboratorio puede alterar su epigenética, afectando su desarrollo futuro. Patrones epigenéticos específicos se han asociado con mayores tasas de implantación y éxito en FIV.
Epigenética y Ovodonación
En la ovodonación, la secuencia genética proviene de la donante de óvulos y el gameto masculino. Sin embargo, el ambiente uterino materno, modelado por la madre gestante, puede inducir cambios epigenéticos que influyen en la expresión génica del bebé. Factores como la dieta, el estrés y la exposición a toxinas durante el embarazo tienen un impacto significativo.
Este fenómeno ayuda a explicar por qué muchos niños nacidos por ovodonación presentan similitudes físicas y de comportamiento con sus madres gestantes, a pesar de no compartir ADN. La epigenética juega un papel crucial en la vinculación entre madre e hijo, más allá de la herencia genética.
Asumiendo el Duelo Genético en la Ovodonación
Comprender el poder de la epigenética es clave para superar el "duelo genético" asociado a la ovodonación. La intensa vinculación que se establece entre la madre y el embrión, tanto emocional como celular, refuerza el vínculo a lo largo de la vida. La tecnología Fenomatch utiliza biométrica avanzada para ayudar a seleccionar donantes con mayor parecido facial, reduciendo el estrés y optimizando el proceso.

Investigaciones sobre Epigenética y Reproducción
Estudios recientes investigan cómo la edad materna, los tratamientos de fertilidad y las técnicas de reproducción asistida afectan los mecanismos epigenéticos en ovocitos y embriones tempranos. Investigaciones en modelos animales sugieren que, si bien las técnicas de reproducción asistida pueden afectar la metilación del ADN, la edad materna avanzada no parece influir significativamente en ciertos errores de metilación en embriones preimplantacionales.
La investigación continúa para comprender y optimizar los tratamientos de reproducción asistida, especialmente en casos de baja reserva ovárica. Se explora la posibilidad de reprogramar el ovario con fármacos para revertir patrones de modificación que conducen a una foliculogénesis inadecuada.
Epigenética y el Síndrome de Hiperestimulación Ovárica
El SHO ocurre cuando las medicaciones de estimulación ovárica inducen una respuesta exagerada, liberando sustancias que provocan fuga de líquido de los vasos sanguíneos. Aunque la mayoría de los ciclos de FIV resultan en un SHO leve sin repercusión, el SHO grave es poco común pero potencialmente mortal. La estimulación ovárica en FIV requiere un control riguroso de las dosis y del inductor de la ovulación.
La epigenética, al influir en la expresión génica y la respuesta celular a estímulos hormonales, podría tener un papel en la susceptibilidad de una mujer al SHO o en la respuesta a los tratamientos. La investigación en esta área podría revelar nuevos enfoques para personalizar los protocolos de estimulación ovárica y reducir el riesgo de SHO, optimizando la obtención de ovocitos y mejorando las tasas de embarazo.
tags: #epigenetica #de #la #hiperestimulacion #ovarica