El trasplante de células madre representa uno de los campos más prometedores de la medicina moderna. Estas células, únicas por su capacidad de autorrenovación y diferenciación, abren un abanico de posibilidades para el tratamiento de enfermedades que actualmente se consideran incurables. Aunque la terapia con células madre adultas ha demostrado su eficacia en la práctica clínica, el estudio y el potencial de las células madre embrionarias (CME) continúan siendo un área intensa de investigación, a pesar de los importantes desafíos éticos y científicos que presentan.
Introducción a las Células Madre
Las células madre, también conocidas como células troncales, son células indiferenciadas e inmaduras que poseen dos propiedades esenciales: la autorrenovación, que les permite dividirse de forma ilimitada manteniendo su estado indiferenciado, y la diferenciación, que les confiere la habilidad de generar diversos tipos de células especializadas, tanto morfológica como funcionalmente (óseas, sanguíneas, epidérmicas, neuronales, etc.). Se encuentran en casi todos los tejidos del cuerpo y son cruciales para el mantenimiento y la reparación de los tejidos después de una lesión.
Clasificación y Origen de las Células Madre
Las células madre se clasifican según su capacidad de diferenciación o su origen, lo que determina su versatilidad y sus aplicaciones potenciales en la medicina regenerativa.
Según su Potencialidad
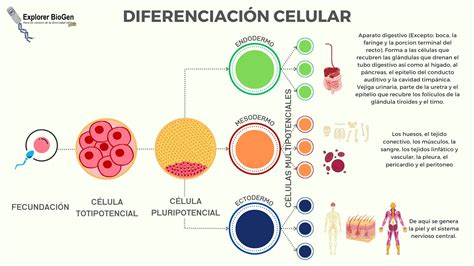
- Células madre totipotentes: Son capaces de producir tanto tejido embrionario (un embrión completo) como extraembrionario (placenta y anexos placentarios). Se encuentran en las primeras etapas del desarrollo embrionario, como el cigoto y las blastómeras.
- Células madre pluripotentes: Tienen la capacidad de diferenciarse en cualquiera de los tejidos existentes en un organismo adulto, procedentes de cualquiera de las tres capas embrionarias, incluyendo las células germinales, pero no pueden formar un organismo completo. Las CME son el ejemplo más estudiado.
- Células madre multipotentes: Son capaces de diferenciarse en distintos tipos celulares, pero siempre restringiendo su potencial a tejidos derivados de una única capa embrionaria (mesodérmicos, ectodérmicos o endodérmicos). También se les denomina células madre órgano-específicas.
- Células madre unipotentes (u oligopotenciales): Presentan la menor potencialidad, ya que solo pueden especializarse en un único linaje celular.
Según su Origen
Desde el punto de vista de su origen, las células troncales se dividen principalmente en embrionarias y adultas, aunque se han identificado otros tipos importantes.
Células Madre Embrionarias (CME)
Las células madre embrionarias (CME) se obtienen a partir de la masa celular interna del blastocisto, un embrión preimplantatorio de 4 a 14 días de edad, o de las crestas gonadales fetales. Son células pluripotentes, lo que significa que pueden proliferar de forma continua sin diferenciarse, siendo prácticamente inmortales, y son capaces de convertirse en cualquier tipo de célula del organismo. Esto incluye tejidos somáticos (corazón, hígado, hueso, pulmón, cerebro) y células germinales (oocitos y espermatozoides).
La posibilidad de obtener y utilizar terapéuticamente las CME humanas ha generado enormes expectativas en la terapia celular. Se han realizado diversos estudios, siendo el aislamiento y cultivo de CME de ratones en 1981, y de humanas en 1998, hitos fundamentales. Sin embargo, su obtención a menudo implica la destrucción del embrión, lo que genera un intenso debate ético y legal que dificulta su implementación médica.

Células Madre Adultas (CMA)
Las células madre adultas (CMA) se encuentran en pequeñas cantidades en la mayoría de los tejidos adultos, como la médula ósea, el torrente sanguíneo, el músculo esquelético, la epidermis, el intestino, el testículo y el hígado, así como en el cordón umbilical. Poseen las características de autorrenovación y diferenciación, aunque su capacidad proliferativa y potencial de diferenciación se considera significativamente menor que la de las CME. Generalmente son multipotenciales, es decir, capaces de diferenciarse en un número limitado de tejidos.
A diferencia de las CME, las CMA no generan problemas de tumores y evitan la destrucción de embriones humanos. Investigaciones recientes sugieren que algunas CMA pueden tener una plasticidad mayor de lo que se pensaba inicialmente, un fenómeno conocido como "versatilidad" o "transdiferenciación", aunque este concepto no está exento de controversia científica.
Células Pluripotentes Inducidas (iPS)
Las células pluripotentes inducidas (iPS) son células adultas normales que han sido reprogramadas genéticamente para adquirir propiedades similares a las células madre embrionarias. Descubiertas por John B. Gurdon y Shinya Yamanaka (Premio Nobel 2012), esta técnica implica la introducción de genes específicos de células madre (como Oct3/4, Sox2, Klf4 y c-Myc) en células somáticas. Las iPS ofrecen la ventaja de evitar los problemas éticos asociados a las CME y reducen el riesgo de rechazo inmunitario al poder generarse a partir de las propias células del paciente.
Sin embargo, la reprogramación es un proceso complejo y aún se investiga sobre la seguridad de las iPS, dado que las secuencias exógenas pueden permanecer en el genoma y potencialmente inducir anomalías o la formación de tumores, especialmente con el uso de oncogenes como c-Myc. La eliminación de este transgén y la mejora de los métodos de transducción buscan producir iPS más seguras.
Células Madre Perinatales
Los investigadores han identificado células madre en el líquido amniótico y en la sangre del cordón umbilical. Estas células madre pueden diferenciarse en células especializadas y se conocen como "células madre adultas" en el contexto del cordón umbilical, aunque provengan de un recién nacido. Entre ellas se encuentran las "Pequeñas Parecidas Células Embrionarias" (VSEL), que comparten propiedades de las CME sin la controversia, y las Células Madre Mesenquimales (MSC), prometedoras en medicina regenerativa. Las Células Madre Hematopoyéticas (HSC) del cordón umbilical se utilizan en trasplantes para enfermedades como la anemia de células falciformes, la leucemia, el linfoma y el mieloma.
Las células madre del cordón umbilical de un bebé ofrecen una compatibilidad del 100% con el propio bebé, eliminando el riesgo de rechazo si se necesitaran en el futuro. Además, tienen un mayor índice de compatibilidad con familiares.
Trasplante de Células Madre: Contexto General y Tipos
Los trasplantes de células madre, a menudo denominados trasplantes de médula ósea, se utilizan principalmente para restaurar las células madre formadoras de sangre que han sido destruidas por dosis altas de quimioterapia o radioterapia en el tratamiento de ciertos cánceres y otros trastornos sanguíneos. Son más comunes en cánceres que afectan las células sanguíneas, como la leucemia, el linfoma, el mieloma múltiple y los síndromes mielodisplásicos. También se aplican para el neuroblastoma, el sarcoma de Ewing, tumores encefálicos recurrentes en niños, tumores de células germinativas y cáncer de testículo. Además, se usan para tratar trastornos de la sangre como la anemia aplásica, la enfermedad de células falciformes y algunas enfermedades autoinmunitarias.
Función del Trasplante de Células Madre
En general, los trasplantes de células madre no actúan directamente contra el cáncer, sino que restauran la capacidad del cuerpo para producir células sanguíneas nuevas después de tratamientos agresivos. Sin embargo, en el caso de la leucemia, un trasplante de células madre alogénico (de un donante) puede actuar directamente contra el cáncer debido a un efecto llamado "injerto contra tumor" o "injerto contra leucemia". Este efecto se produce cuando los glóbulos blancos del donante atacan cualquier célula cancerosa residual en el cuerpo del paciente.
Proceso General del Trasplante
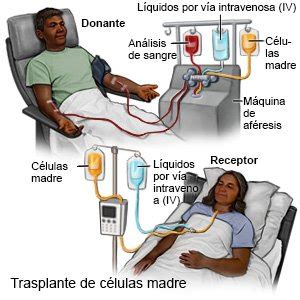
El proceso de un trasplante de células madre comienza con un tratamiento de quimioterapia de dosis alta y, a veces, radioterapia, que puede durar una o dos semanas. Luego de unos días de descanso, el paciente recibe las células madre formadoras de sangre a través de una infusión intravenosa, similar a una transfusión de sangre. El día de la infusión se conoce como "día cero" y el procedimiento puede durar de 1 a 5 horas. Después de recibir las células madre, comienza la fase de recuperación, durante la cual se monitorean los recuentos sanguíneos.
Las células madre formadoras de sangre para estos trasplantes se extraen principalmente del torrente sanguíneo, pero también pueden obtenerse de la médula ósea o del cordón umbilical de un recién nacido. Una vez infundidas, las células madre viajan hasta la médula ósea, donde reemplazan las células destruidas por el tratamiento.
Tipos de Trasplantes de Células Madre
- Autógeno (autotrasplante): El paciente recibe sus propias células madre, extraídas y almacenadas antes del tratamiento. Las células trasplantadas serán compatibles, y se destruyen algunas células cancerosas sin destruir todas las células formadoras de sangre.
- Alogénico: Las células madre provienen de otra persona, que puede ser un pariente consanguíneo o un donante no emparentado, siempre que las células sean muy compatibles con las del paciente. Para determinar la compatibilidad, se realiza una prueba de antígenos leucocitarios humanos (HLA).
- Singénico: Las células madre se obtienen de un gemelo idéntico al paciente, lo que garantiza una compatibilidad genética perfecta.
- Trasplantes en tándem: Un tipo de trasplante autógeno donde el paciente recibe un ciclo de quimioterapia de dosis alta, seguido de un trasplante de células madre, y luego repite el proceso.
Desafíos y Potencial del Trasplante de Células Madre Embrionarias
Es fundamental señalar que, en la actualidad, las aplicaciones clínicas de la terapia celular se limitan predominantemente a las células madre adultas o las células de cordón umbilical. Las células madre embrionarias aún no se utilizan en estudios clínicos con pacientes debido a importantes limitaciones. La investigación con CME se centra en comprender su biología y superar estos obstáculos para un futuro uso terapéutico.
Limitaciones Actuales de las CME en Trasplantes
A pesar de su enorme potencial, las CME presentan desafíos significativos que han impedido su aplicación clínica directa hasta el momento:
- Riesgo de tumores: La misma capacidad proliferativa e inmortalidad de las CME puede llevar a la producción de tumores, como teratomas y teratocarcinomas, en modelos animales. Controlar la diferenciación y evitar la formación de células no deseadas es un reto crucial.
- Rechazo inmune: El trasplante de CME entre dos sujetos inmunológicamente incompatibles provocaría una fuerte respuesta de rechazo por parte del sistema inmunitario del receptor, lo que requeriría una medicación inmunosupresora con sus consiguientes efectos adversos.
- Complejidad en el control de la diferenciación: Controlar con precisión cómo se diferencian las CME en tipos específicos de células especializadas, en grandes cantidades y de forma fiable, es un desafío científico importante.
Líneas de Investigación con CME
A pesar de las limitaciones, la investigación con CME es un campo vibrante con un enorme potencial:
- Comprensión del desarrollo embrionario: Las CME son herramientas valiosas para estudiar cómo se desarrolla el cuerpo desde las primeras fases embrionarias hasta la formación de órganos complejos, y cómo contribuyen los genes específicos a las funciones y enfermedades celulares.
- Creación de células especializadas in vitro: Los investigadores están aprendiendo a inducir la diferenciación de CME en tipos específicos de células adultas (como neuronas, células cardíacas, células productoras de insulina) exponiéndolas a diferentes moléculas de señalización y condiciones de crecimiento en el laboratorio. Esto permite estudiar enfermedades y probar nuevos fármacos sin necesidad de tejido de pacientes.
- Potencial para la medicina regenerativa: Las CME ofrecen la esperanza de generar células sanas para reemplazar tejidos dañados o afectados por enfermedades neurodegenerativas (Parkinson, Alzheimer), diabetes tipo 1, esclerosis lateral amiotrófica, insuficiencia cardíaca, ceguera y esclerosis múltiple, entre otras.
- Trasplantes prenatales para trastornos sanguíneos congénitos: Se están estudiando formas de mejorar el injerto de células madre en fetos con trastornos congénitos de células madre sanguíneas (como la anemia de células falciformes o la talasemia). El sistema inmunológico fetal inmaduro podría aceptar células trasplantadas sin necesidad de fármacos inmunosupresores, promoviendo el crecimiento y la diferenciación de las células trasplantadas. En esta aplicación, se exploran "nuevas células madre embrionarias" que podrían ser más adecuadas para diferenciarse en células sanguíneas en el entorno fetal, así como enfoques para mejorar su supervivencia en los órganos fetales productores de sangre.
¿Qué son las células madre? 2025
Riesgos y Consideraciones de los Trasplantes de Células Madre (generalmente CMA)
Aunque los trasplantes de células madre ofrecen beneficios significativos, especialmente con CMA, también conllevan riesgos y complicaciones que pueden ser a corto o largo plazo.
Problemas a Corto Plazo
- Náuseas y vómitos
- Fatiga y agotamiento
- Pérdida del apetito
- Úlceras en la boca
- Caída del cabello (alopecia)
- Reacciones en la piel
- Aumento del riesgo de infección y sangrado
Problemas a Largo Plazo
- Esterilidad
- Cataratas (opacidad del cristalino del ojo que causa pérdida de visión)
- Nuevos cánceres secundarios (el cáncer se disemina a otras partes del cuerpo)
- Daño a órganos vitales como el hígado, el riñón, el pulmón o el corazón
- Debilidad en los huesos o músculos
Enfermedad de Injerto contra Huésped (EICH)
En el caso de trasplantes alogénicos (con células de un donante), existe la posibilidad de desarrollar la enfermedad de injerto contra huésped (EICH). Esta complicación grave ocurre cuando los glóbulos blancos del donante (el injerto) atacan las células del cuerpo del paciente (el huésped) al considerarlas extrañas. La EICH puede dañar la piel, el hígado, los intestinos y muchos otros órganos. Puede ser aguda (dentro de los primeros 3 meses después del trasplante) o crónica (3 o más meses después).
El tratamiento general de la EICH implica corticoesteroides u otros medicamentos que inhiben el sistema inmunitario. Para disminuir el riesgo, es crucial que las células madre del donante sean lo más compatibles posible. Los médicos también pueden administrar medicamentos para inhibir el sistema inmunitario del paciente o tratar las células madre donadas para extraer los glóbulos blancos (células T) que causan la EICH.
Aspectos Prácticos y Económicos del Trasplante de Células Madre
Los trasplantes de células madre son procedimientos complejos y muy costosos. Requieren una estancia hospitalaria prolongada en centros de tratamiento especializados y la atención de múltiples proveedores de salud. Después del alta, los pacientes necesitan controles de seguimiento frecuentes por parte de un médico con experiencia en trasplantes, que pueden durar varios meses e implicar visitas al hospital dos o tres veces por semana para transfusiones, reemplazo de minerales o seguimiento.
Si el paciente vive lejos del centro de tratamiento, deberá incurrir en costos adicionales de transporte y alojamiento. Además, los efectos secundarios graves pueden requerir tratamientos costosos. Es importante consultar con el seguro médico para determinar la cobertura, ya que la mayoría de los planes cubren algunos costos para ciertos tipos de cáncer.
La posibilidad de trabajar durante el proceso de trasplante y recuperación, que puede llevar muchos meses e incluir hospitalizaciones, dependerá del tipo de empleo y de la fatiga o dificultad de concentración. Es recomendable coordinar con el empleador la posibilidad de trabajar a distancia o ajustar horarios, ya que la ley a menudo obliga a las empresas a adaptarse a las necesidades de los pacientes con cáncer.
Dilema Ético y Legal de la Investigación con Células Madre Embrionarias
La obtención de células madre embrionarias, que provienen de embriones en etapa temprana, ha generado un significativo debate ético y moral. Estos embriones suelen ser aquellos creados mediante fertilización in vitro que no fueron implantados en el útero de una mujer y que son donados para investigación con el consentimiento informado de los donantes. Instituciones como los Institutos Nacionales de Salud han establecido pautas para la investigación con células madre humanas, definiendo cómo pueden usarse y las recomendaciones para su donación.
La controversia se intensifica al considerar que las CME, al ser extraídas, impiden que el embrión se desarrolle en un ser humano completo. Esto lleva a muchos a preguntarse por qué no se utilizan células madre adultas en su lugar. Si bien el progreso en la reprogramación celular y las células iPS ha mejorado la investigación, las CMA podrían no ser tan versátiles y duraderas como las CME. Además, las CMA son más propensas a tener irregularidades debido a factores ambientales o errores adquiridos durante la duplicación.
Clonación Terapéutica
La clonación terapéutica, también conocida como transferencia nuclear de células somáticas, es una técnica que busca crear líneas de células madre versátiles sin depender de óvulos fecundados. Consiste en extraer el núcleo de un óvulo no fecundado y reemplazarlo con el núcleo de una célula somática de un donante. El óvulo reprogramado se divide y forma un blastocisto, del cual se puede obtener una línea de células madre genéticamente idéntica al donante (un clon).
Algunos investigadores creen que las células madre derivadas de la clonación terapéutica podrían ser más beneficiosas que las obtenidas de óvulos fecundados, ya que es menos probable que sean rechazadas al ser trasplantadas de nuevo al donante. Además, permitiría estudiar con precisión cómo se desarrolla una enfermedad específica en un contexto genéticamente idéntico al paciente. Aunque ha tenido éxito en otras especies (como la oveja Dolly en 1997), la clonación terapéutica en seres humanos aún no ha sido realizada con éxito y sigue siendo un área de intensa investigación.
tags: #trasplante #de #celulas #madre #embrionarias