La producción de semillas sintéticas, también conocidas como semillas artificiales, representa una innovación significativa en el campo de la agricultura y la biotecnología vegetal. Esta tecnología, que se basa en la aplicación de embriones somáticos, ofrece una nueva perspectiva para la propagación de plantas, especialmente aquellas con dificultades reproductivas o características élite.
Origen y Desarrollo del Concepto de Semilla Sintética
El concepto de semilla sintética tiene sus raíces en los descubrimientos pioneros sobre los embriones somáticos, descritos por primera vez en 1958 por Jakob Reinert y por F.C. Steward y sus colaboradores. Sin embargo, fue Toshio Murashige quien, en un simposio celebrado en Ghent (Bélgica) en 1977, impulsó notablemente su utilización para la propagación a gran escala de plantas. Murashige formalizó la idea de la producción de semillas sintéticas, definiéndolas como un simple embrión somático encapsulado.
Una distinción clave de la semilla sintética frente a la semilla verdadera radica en el origen del embrión. En la semilla sintética, el embrión es somático, es decir, producido a través del fenómeno de embriogénesis somática, a diferencia del embrión cigótico de la semilla natural. Además, si la semilla sintética incluye endospermo y cubierta, estos son de naturaleza artificial.

Características y Ventajas de la Semilla Sintética
La semilla sintética, cuando se expone a condiciones ambientales adecuadas, tiene la capacidad de germinar y desarrollarse en una planta completa. Esta tecnología abre un abanico de posibilidades en la agricultura, pudiendo aplicarse a la propagación de plantas que naturalmente no producen semillas, o a la multiplicación de poliploides con características élite y líneas vegetales con problemas de propagación.
La tecnología de semilla sintética puede tener un impacto considerable en la producción de cultivos, tanto en aquellos de propagación vegetativa como en los que se propagan por semilla. Para la propagación vegetativa, permite la siembra directa de variedades clonadas y sirve como un medio eficiente para el mantenimiento de germoplasma élite. De esta manera, la semilla sintética se perfila como una tecnología que posibilita el escalamiento extensivo necesario para la producción comercial de clones de alto valor genético.
Las principales ventajas del uso de la semilla artificial incluyen:
- Facilidad de manipulación.
- Facilidad de transportación.
- Potencial para el almacenamiento prolongado.
- Posibilidad de escalamiento para producción masiva.
- Bajos costos de producción y subsecuente propagación.
En muchos aspectos, el protocolo para la producción de semilla sintética imita el desarrollo cigótico y la siembra de semillas naturales, ya que el objetivo primordial de esta tecnología es producir análogos de semillas naturales.
Aplicación en Especies Amenazadas: El Caso de Laelia anceps ssp. dawsonii
La orquídea silvestre Laelia anceps ssp. dawsonii es un ejemplo destacado de la aplicación de la tecnología de semilla sintética con fines de conservación. Las atractivas características de esta orquídea han llevado a su sobreexplotación para su comercialización como planta de maceta y flor cortada, lo que la ha situado en peligro de extinción, incluida en la Norma Oficial Mexicana NOM-059-ECOL-2001.
A esta problemática se suma su baja tasa de propagación natural. Al igual que la mayoría de las orquídeas, sus semillas carecen de endospermo y presentan una baja capacidad de germinación (1-5%), que además está ligada a la obligatoria asociación micorrízica. El desarrollo de metodologías eficientes para su propagación es, por tanto, una estrategia crucial para su conservación y uso sustentable, y para reducir la presión sobre las poblaciones silvestres.
Si bien los embriones somáticos (ESs) aún no son tan robustos y vigorosos como los embriones cigóticos, lo que ha dificultado la producción rutinaria de grandes cantidades de semillas sintéticas plantables directamente en campo, se han realizado avances significativos. La tecnología de semilla sintética, especialmente en especies como la alfalfa (Medicago sativa L.), ha demostrado ser muy prometedora. A pesar de los avances en embriogénesis somática para diversas especies en la última década, no se han desarrollado nuevas cubiertas para semillas sintéticas desde los inicios de la década de 1980, cuando se utilizaron por primera vez el polioxietileno y el alginato de sodio.
El uso de la tecnología de semilla artificial para el rescate y la conservación de Laelia anceps ssp. dawsonii aún estaba en fases de desarrollo. Sin embargo, la existencia de un protocolo para su propagación a través de la embriogénesis somática (Lee et al., 2007) proporcionaba una base sólida para la producción masiva y la obtención de material ideal para la encapsulación. El estudio en cuestión se centró en analizar los factores que influyen en el mantenimiento de la viabilidad durante el almacenamiento y la germinación de embriones somáticos encapsulados de esta especie, con el objetivo de establecer un sistema de rescate y conservación.

Materiales y Métodos en la Producción de Semilla Sintética
La investigación sobre Laelia anceps ssp. dawsonii implicó la encapsulación de embriones somáticos en estado de plúmula dentro de una matriz de alginato en complejo con cloruro de calcio. Posteriormente, se estudió el efecto de factores físicos y químicos, como la temperatura y el tiempo de almacenamiento, la concentración de alginato, y las concentraciones de sales MS y BAP, sobre el porcentaje y el tiempo de germinación de los embriones encapsulados.
Encapsulación de los Embriones Somáticos
Los embriones somáticos de Laelia anceps ssp. dawsonii se obtuvieron a partir de callo embriogénico desarrollado en embriones cigóticos maduros. El medio de cultivo utilizado fue MS (Murashige y Skoog, 1962) suplementado con 2 mg·litro⁻¹ de ácido naftalen-acético (ANA), 6-bencilaminopurina (BAP) y ácido indol-3-acético (AIA) por cada componente. Este proceso tomó aproximadamente tres meses desde la siembra in vitro.
Los embriones somáticos seleccionados para la encapsulación y producción de semilla sintética se encontraban cercanos al estado de plúmula, carentes de raíz, y fueron cosechados a los 40 días de su desarrollo in vitro.
Preparación de la Matriz de Encapsulación
La matriz de encapsulación consistió en una combinación de alginato de sodio (Sigma) y cloruro de calcio dihidratado (CaCl₂·2H₂O). Se prepararon dos soluciones principales:
- Alginato de sodio en concentraciones del 2%, 3% y 4%, disuelto en soluciones de sales MS al 100%, 50% y 37.5%, sin cloruro de calcio.
- Cloruro de calcio dihidratado (CaCl₂·2H₂O) a una concentración de 75 mM, disuelto en soluciones de sales MS al 100%, 50% y 37.5%, a las cuales se añadió la concentración normal de cloruro de calcio dihidratado.
Proceso de Encapsulación
Los embriones somáticos fueron colectados de las cajas de Petri y, en condiciones asépticas, suspendidos en la solución de alginato de sodio. Posteriormente, se transfirieron gota a gota a la solución de cloruro de calcio contenida en un matraz Erlenmeyer de 500 ml, utilizando una micro pipeta. El matraz se colocó en un agitador rotatorio a 150 rpm durante 30 minutos para favorecer la formación de una estructura esférica en la semilla sintética.
Tras la encapsulación, se decantó el cloruro de calcio y se realizaron dos lavados con agua destilada esterilizada. Las semillas sintéticas resultantes se almacenaron en cajas de Petri esterilizadas y selladas, manteniéndolas refrigeradas a 3.0 ± 1 °C.
Condiciones de Incubación y Evaluación
Los experimentos para determinar la viabilidad, desarrollo, porcentaje y tiempo de germinación se llevaron a cabo en cajas de Petri con papel filtro humedecido con agua destilada esterilizada. Las cajas se sellaron y colocaron en una incubadora con un fotoperiodo de 16 horas y un flujo fotónico de 33.78 μm·m⁻²·s⁻¹, a diferentes temperaturas según el experimento.
Efecto de la Concentración de Alginato de Sodio y BAP
Para determinar la consistencia óptima de la matriz de encapsulación, se probaron concentraciones de alginato de sodio del 2%, 3% y 4%, en combinación con BAP a 0.5, 1.0 y 2.0 mg·litro⁻¹. Se utilizó un diseño experimental completamente aleatorio con arreglo factorial y 15 repeticiones por tratamiento.
El medio de cultivo empleado para la evaluación fue MS suplementado con 5 ml·litro⁻¹ de solución de vitaminas MS, 100 mg·litro⁻¹ de myo-inositol y 1.0 mg·litro⁻¹ de ANA. Se evaluó el porcentaje de germinación y el tiempo requerido para la aparición de la primera hoja y la primera raíz en 15 semillas sintéticas por tratamiento, utilizando un microscopio estereoscópico para registrar el incremento de masa embrionaria y los cambios de coloración.
Efecto de la Concentración de Sales Minerales, Temperatura y Tiempo de Almacenamiento
Para optimizar la conservación y viabilidad de las estructuras encapsuladas, se estableció un experimento completamente aleatorio con arreglo factorial 3x3x2. Se probaron tres concentraciones de sales MS (100%, 50% y 37.5%), tres temperaturas de incubación (4 °C, 20 °C y 25 °C) y dos tiempos de almacenamiento (15 y 30 días).
Las evaluaciones de desarrollo y viabilidad de los embriones somáticos se realizaron observando el proceso de germinación a los 15 y 30 días de su desarrollo in vitro bajo las condiciones de cada tratamiento, utilizando un microscopio estereoscópico para el registro fotográfico y el recuento de la aparición del primer primordio foliar.
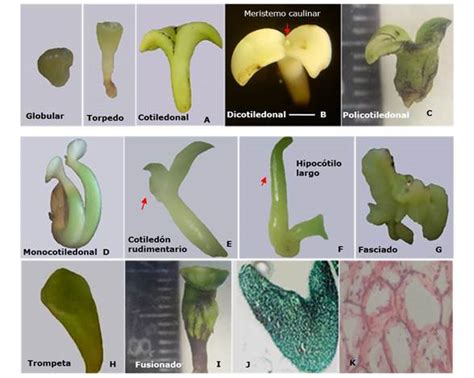
Producción de semilla sintética en plantas
Resultados Clave y Observaciones
En las pruebas realizadas, se observó que el 100% de germinación se logró cuando las semillas sintéticas fueron encapsuladas con un 3% de alginato de sodio en complejo con CaCl₂·2H₂O a 75 mM. Al utilizar sales MS al 100% y 50% en la matriz de encapsulación, suplementando con 2.0 mg·litro⁻¹ de BAP, se alcanzó un porcentaje de germinación del 64.54% y 62.77%, respectivamente, sin diferencias significativas entre estas dos concentraciones de sales MS.
Estos resultados subrayan la importancia de la composición de la matriz de encapsulación y la concentración de nutrientes y reguladores del crecimiento para el éxito en la producción de semillas sintéticas viables y germinables, especialmente en especies de interés para la conservación.