La evaluación de los ovocitos después de la inseminación in vitro, típicamente entre 16 y 22 horas post-inseminación, constituye el procedimiento estándar para determinar la fecundación. La presencia de dos pronúcleos (2PN) centrados en el citoplasma y dos corpúsculos polares (2CP) en el espacio perivitelino al día siguiente de la inseminación (D+1) se considera indicativo de una fecundación correcta. No obstante, pueden presentarse otras situaciones, a menudo resultado de procesos anómalos.
La presencia de 3PN+2CP usualmente ocurre en la fecundación in vitro convencional (FIV) y suele tener un origen masculino (diándrico), siendo causada por la penetración de dos espermatozoides (dispermia). Una polipenetración por más de dos espermatozoides (>3PN+2CP) es menos común, pero puede ocurrir si el bloqueo contra la polispermia falla de manera significativa. Las causas de la polipenetración pueden estar relacionadas con la inmadurez o la hipermadurez de los ovocitos, especialmente tras períodos de co-incubación prolongados.
En el caso de la inyección intracitoplasmática de espermatozoides (ICSI), donde se introduce un único espermatozoide, la presencia de más de dos pronúcleos generalmente tiene un origen femenino (digínico). La observación de 3PN+2CP en estos casos suele deberse a la no extrusión del segundo corpúsculo polar y a la fragmentación o división del primer corpúsculo polar, que puede confundirse con la presencia de dos corpúsculos polares. La extrusión del segundo corpúsculo polar (2º CP) suele ocurrir cerca de la ubicación del primer corpúsculo polar, en el polo animal del ovocito (Antzak and Van Blerkom, 1999).
Diferenciación de Corpúsculos Polares y Gránulos Corticales
El primer corpúsculo polar se distingue del segundo corpúsculo polar por la presencia de gránulos corticales (GC), microtúbulos y material nuclear en forma de cromosomas en su interior (Fig. 1). Los orgánulos citoplasmáticos presentes en el primer corpúsculo polar son los mismos que se encuentran en el citoplasma del ovocito. Frecuentemente, este corpúsculo se observa dividido o fragmentado.
En ovocitos con 3PN resultantes de polispermia, se observan esporádicamente algunos gránulos corticales residuales en la periferia del citoplasma. Si la inseminación se realizó de forma precoz (ovocitos inmaduros), es común observar los gránulos corticales en regiones más internas del citoplasma, formando pequeñas agrupaciones (Fig. 2). En contraste, en el ovocito maduro, los GC se encuentran dispuestos en la periferia, debajo de la membrana plasmática.
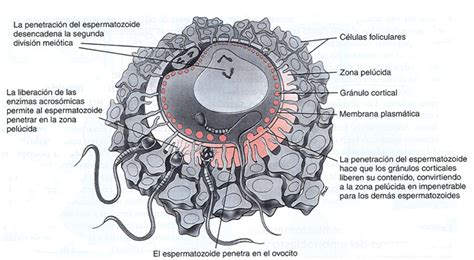
La formación de los GC ocurre en las etapas tempranas de la maduración ovocitaria, aunque el momento exacto varía entre especies (Berg and Wessel, 1997). Se originan a partir del complejo de Golgi, que sufre hipertrofia y forma vesículas de contenido electrodenso. Estas vesículas migran hacia la periferia celular gracias a la red de microfilamentos citoplasmáticos (Dimaggio et al., 1997, Wessel et al., 2002). La migración de los GC y la maduración ovocitaria son procesos paralelos en la mayoría de las especies.
Reacción Cortical y sus Implicaciones
Como consecuencia de la fecundación, se produce la reacción cortical, un mecanismo diseñado para prevenir la polispermia. Durante este proceso, la membrana que rodea a los GC se fusiona con la membrana plasmática (oosoma), y el contenido de los gránulos se vierte al espacio perivitelino. Esto inicia reacciones químicas que endurecen la zona pelúcida (ZP), haciéndola menos susceptible a las enzimas proteolíticas del acrosoma espermático. Los cambios en la matriz extracelular provocan una separación física y bioquímica entre el ovocito y los espermatozoides externos.
Estudios recientes mediante microscopía electrónica y citoquímica sugieren la existencia de diferentes tipos de GC en el ovocito humano, cada uno con funciones potenciales distintas: modificación de la ZP para evitar la reacción acrosómica, modificación de la membrana ovocitaria para prevenir la fusión con otros espermatozoides, e incluso participación en procesos previos a la fusión de membranas (Jimenez-Movilla et al., 2004; Liu et al., 2003).
La falta o escasez de GC adyacentes a la membrana en ovocitos polipenetrados indica que la reacción cortical ya ha ocurrido antes de la fijación de la muestra para estudio ultraestructural. Generalmente, se observan los dos corpúsculos polares en el espacio perivitelino, más o menos degenerados o fragmentados dependiendo del tiempo transcurrido antes de la fijación.
Orgánulos Citoplasmáticos y Anomalías
En el citoplasma, se aprecia una mayor concentración de orgánulos citoplasmáticos alrededor de los pronúcleos. Los orgánulos más abundantes son las mitocondrias, que suelen ser redondas u ovoides con pocas crestas, y las vesículas de retículo endoplasmático liso (REL). Es frecuente observar asociaciones de grandes vesículas de REL con mitocondrias redondas dispuestas a su alrededor, similar a lo que ocurre en ovocitos y cigotos no evolutivos. También se observan ocasionalmente agrupaciones de gran tamaño de pequeñas vesículas de retículo endoplasmático liso (AREL) (Fig. 3), que algunos autores asocian con ovocitos envejecidos (Sathananthan and Gunasheela, 2007).

Al microscopio óptico, las AREL pueden parecer grandes vacuolas, pero se diferencian por su aspecto translúcido y, según se observa al microscopio electrónico de transmisión (MET), por la ausencia de una membrana delimitadora. Dependiendo de su tamaño y posición, pueden confundirse con un pronúcleo. La existencia de AREL podría estar relacionada con niveles elevados de estradiol en el día de administración de la hCG y se ha asociado con bajas tasas de embarazo (Otsuki et al., 2004). Estos autores sugieren que un patrón anómalo en la formación y distribución del REL podría implicar anomalías en la regulación del Ca2+ y, consecuentemente, afectar el desarrollo embrionario.
Estructuras Nucleares y Citoplasmáticas en Cigotos
En el interior de los pronúcleos, se observan pequeños grumos de cromatina y precursores nucleolares densos y compactos, polarizados hacia la zona donde convergen los tres pronúcleos (Fig. 4). Los paquetes de láminas anilladas citoplasmáticas también están presentes en los cigotos (Fig. 5). Presentan características ultraestructurales similares a las de la envoltura nuclear, con numerosos poros complejos en sus cisternas. También pueden encontrarse en el interior del núcleo en forma de fragmentos simples, preferentemente convergiendo hacia la zona de confluencia de los pronúcleos. Esta característica se considera un signo de apoptosis, al igual que una baja concentración de poros en la membrana nuclear, típica de estados no evolutivos (Rawe et al., 2003).
La presencia de pequeños complejos de Golgi indica actividad celular, ya que en ovocitos maduros detenidos en metafase II es raro observar vesículas o cisternas de Golgi. Mediante un estudio secuencial y minucioso del citoplasma del cigoto, se pueden observar restos de los axonemas espermáticos, con sus nueve pares de microtúbulos, los dos microtúbulos centrales y las nueve fibras densas, mientras que no es posible identificar las mitocondrias de las piezas intermedias. Generalmente, los restos espermáticos se encuentran muy cerca de los pronúcleos (Fig. 6). Se han descrito raramente observaciones que aseguren la presencia de restos de diferentes espermatozoides, aunque algunas imágenes parecen sugerirlo (Van Blerkom et al., 1984; Boada and Ponsà 1987; Boada 1992; Sathananthan et al., 1999).
Anomalías en la División Celular y su Impacto
La presencia de más de un centrosoma espermático, una estructura crucial para las primeras divisiones mitóticas como centro organizador de microtúbulos, puede llevar a una segregación tripolar o desorganizada de los cromosomas. La mayoría de los embriones con tres pronúcleos no evolucionan, mostrando signos de degeneración como fragmentación citoplasmática, aumento de vesículas de REL que evolucionan a vacuolas con mitocondrias asociadas, y posición excéntrica de los pronúcleos.
Su capacidad de división es inferior a la de los cigotos correctamente fecundados. Sin embargo, si se dividen, los cambios observados no difieren de los que ocurren en cigotos 2PN: migración de los pronúcleos, interdigitación de las envolturas nucleares y posición convergente de la cromatina y otras estructuras nucleares. Cuando se bloquean y no se dividen, sus características morfológicas son similares a las de los cigotos 2PN que no avanzan en el desarrollo embrionario.
El momento de la división de los cigotos con tres pronúcleos suele alterarse (Van Blerkom, 1989), observándose normalmente retrasos (Sathananthan et al., 1999). La división de cigotos 3PN frecuentemente genera blastómeros multinucleados. Se ha observado que los cigotos 3PN pueden alcanzar el estado de blastocisto e incluso implantar, existiendo casos documentados de fetos y recién nacidos triploides (69XXX o 69XXY) (Edwards, 1986). Estudios citogenéticos de embriones polipenetrados demuestran que, en muchos casos, se trata de mosaicos con coexistencia de blastómeros normales y anómalos (Munné and Cohen, 1998; Sathananthan et al, 1999).
Confusiones Diagnósticas y Pseudopronúcleos
Es importante destacar que las observaciones realizadas con estereomicroscopio o microscopio invertido, si no se llevan a cabo con suficiente detalle, pueden dar lugar a confusiones. Un cigoto fecundado normalmente (2PN+2CP) que presente grandes AREL, o una o más vesículas de tamaño similar a los pronúcleos, podría interpretarse erróneamente como un cigoto con tres o más pronúcleos. En estos casos, una observación más detallada o por un embriólogo experimentado permitiría distinguir el pseudopronúcleo (PPN) de los verdaderos pronúcleos.
Los PPN se diferencian de los PN por la ausencia de precursores nucleolares y de las modificaciones típicas de la membrana en las regiones de convergencia de los pronúcleos (Van Blerkom, 1987). Esta situación suele explicarse por la no segregación del segundo corpúsculo polar y es más frecuente en casos de ICSI, aunque también puede ocurrir en FIV convencional. En estos casos, se trataría de una fecundación correcta por un solo espermatozoide, con la no extrusión del segundo corpúsculo polar, lo que resultaría en un segundo pronúcleo de origen femenino (diginia).
Cigotos 3PN+1CP y 1PN+2CP
Las características ultraestructurales de los cigotos 3PN+1CP son similares a las de los 3PN+2CP, con la diferencia de que en el primer caso solo se podrían encontrar restos de un espermatozoide en el interior del ovocito. Podría tratarse de una activación partenogenética sin extrusión del segundo corpúsculo polar y formación de dos pronúcleos femeninos (Kaufman, 1983), o ser el resultado de una fecundación normal por un espermatozoide, pero con la no extrusión del segundo corpúsculo polar, lo que resultaría en un pronúcleo femenino con dotación diploide y un cariotipo fetal triploide. Los fetos triploides de origen digínico suelen presentar retraso del crecimiento, macrocefalia y placenta no quística (Carceller et al., 2004). Únicamente el estudio cromosómico o molecular del material nuclear permitiría determinar el origen de estos casos, los cuales no deberían ser transferidos debido al riesgo de patologías fetales.
Generalmente, los cigotos 1PN+2CP se originan por activación partenogenética sin extrusión del segundo corpúsculo polar y formación de un solo pronúcleo femenino (Kaufman, 1983). Otras explicaciones, como una fecundación normal con ausencia de formación de uno de los pronúcleos y no extrusión del segundo corpúsculo polar, son menos probables.
La viabilidad de los cigotos 1PN+2CP varía según su origen. Otsu y colaboradores (2004) postulan que si el pronúcleo mide 29 μm o más, es probable que sea diploide, mientras que si su tamaño es menor, el cigoto es cromosómicamente anormal en la mayoría de los casos. Frecuentemente, los 1PN+2CP en ICSI son producto de una activación partenogenética (Kaufman, 1983; Balakier et al 1993) y raramente (7%) logran alcanzar el estado de blastocisto (Campos et al., 2007).
En general, la existencia de embriones diploides procedentes de cigotos 1PN+2CP, fenómeno más frecuente en FIV convencional que en ICSI, puede tener diversos orígenes. Suele interpretarse como resultado de una fecundación normal con asincronía en la formación de los dos pronúcleos, dificultando su visualización simultánea (Sultan et al., 1995; Payne et al., 1997), o como consecuencia de la fusión del pronúcleo masculino y femenino, dando lugar a un único pronúcleo diploide de gran tamaño (Levron et al., 1995).
En FIV convencional, la observación de cigotos con solo 1PN+2CP se considera normal e interpretada como asincronía en la aparición de los dos pronúcleos. Payne et al. (1997) observaron sincronía en la formación de los dos pronúcleos en el 63% de los casos. Para la formación del pronúcleo masculino es necesaria la descondensación de la cromatina espermática, altamente compactada por protaminas nucleares, mediante la acción de histonas ovocitarias. Para detectar posibles casos de asincronía, en los cigotos 1PN+2CP se recomienda una segunda observación para confirmar la presencia o ausencia del segundo pronúcleo.
A pesar de que un número considerable de cigotos 1PN+2CP son cromosómicamente normales, si las observaciones se realizan en el momento adecuado y no se observan los 2PN+2CP, debe considerarse que la microscopía óptica por sí sola no puede descartar un posible origen partenogenético. Por lo tanto, ante una puntuación embrionaria similar, se prefieren para la transferencia aquellos embriones en los que se hayan observado los dos pronúcleos.
Cigotos "No Fecundados" y su Potencial Evolutivo
La ausencia de observación de pronúcleos, pero con presencia de dos corpúsculos polares, frecuentemente se clasifica erróneamente como "no fecundado" (NF+2CP). Este estado admite diversas interpretaciones, aunque estudios genéticos han demostrado que en el 40% de los casos se trata de cigotos diploides con una tasa de desarrollo a blastocisto de hasta el 56%. Esto sugiere que podrían ser embriones con una velocidad de división diferente (Campos et al., 2007).
Para esclarecer esta situación, se recomienda una segunda observación horas después. Si se observa división, la explicación más probable es que la fecundación haya sido muy temprana y/o la velocidad de división muy rápida, de modo que en el momento de la evaluación inicial los pronúcleos ya no fueran visibles y el cigoto estuviera preparándose para la primera división embrionaria. Si no se observa división ni a las 25-27 horas post-inseminación (EC D+1) ni al día siguiente (D+2), la explicación más probable...
✨🧬 Así es el proceso de FECUNDACIÓN - Fertilización Paso a paso
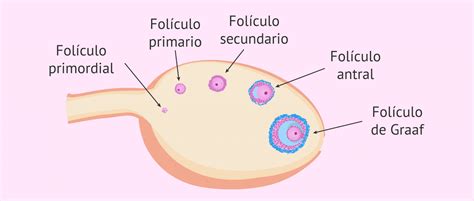
Visión Específica de la Corteza Ovárica y Folículos
La corteza ovárica se presenta parcialmente revestida por restos del epitelio germinal, sostenido por la albugínea fibrosa. Se observan numerosos folículos primordiales, cada uno compuesto por un ovocito rodeado de células capsulares aplanadas. Los folículos primarios, tanto unilaminares como multilaminares, consisten en un ovocito con su zona pelúcida y una o varias capas de células poligonales de la granulosa, separadas por una lámina basal de las células de la teca.
Los folículos secundarios o antrales presentan estas mismas estructuras, pero más desarrolladas, e incluyen un espacio vacío que configura el antro folicular. En la teca se distingue una capa interna de células poligonales muy vascularizadas y una capa externa de células más fusiformes. El folículo maduro o terciario, de gran tamaño, contiene un ovocito excéntrico rodeado por el cúmulo oóforo, una gran cavidad antral revestida por células de la granulosa y, externamente, las células de la teca.
En resumen, el ovocito primario es una célula germinal femenina que se origina a partir de una ovogonia. Durante la meiosis I, da lugar al ovocito de tipo II y al primer corpúsculo polar. La morfología y el estado de los pronúcleos, corpúsculos polares y otros orgánulos citoplasmáticos son indicadores clave para evaluar la correcta fecundación y detectar posibles anomalías en el proceso.
tags: #ovocito #primario #vesicula #germinal #microscopio