La sepsis neonatal es una infección invasiva, generalmente de origen bacteriano, que ocurre durante el período neonatal. Los signos y síntomas son variados, inespecíficos y pueden incluir disminución de la actividad espontánea, succión menos enérgica, apnea, bradicardia, inestabilidad térmica, dificultad respiratoria, vómitos, diarrea, distensión abdominal, inquietud, convulsiones e ictericia. El diagnóstico se basa en el examen físico y el cultivo bacteriano. El tratamiento inicial suele consistir en ampicilina junto con gentamicina o cefotaxima, ajustándose posteriormente a antibióticos específicos contra los microorganismos causantes tan pronto como sea posible.

Epidemiología y Factores de Riesgo
La sepsis neonatal ocurre en aproximadamente 1 a 4 de cada 1000 nacimientos. Diversos factores aumentan el riesgo de padecerla, entre los que se incluyen:
- Rotura de membranas previa al trabajo de parto (prematura): Especialmente si ocurre ≥ 18 horas antes del nacimiento.
- Infección materna o fiebre intraparto: Incluyendo la colonización por estreptococo del grupo B (EGB) y la infección intraamniótica.
- Parto pretérmino: Nacimiento antes de las 37 semanas de gestación.
- Recién nacidos con bajo peso al nacer: Particularmente aquellos con peso extremadamente bajo.
- Puntuación de Apgar baja y/o necesidad de reanimación neonatal.
- Sexo masculino.
Además, un bajo estatus socioeconómico se ha asociado con una mayor incidencia y mortalidad a causa de la sepsis neonatal.
Etiología de la Sepsis Neonatal
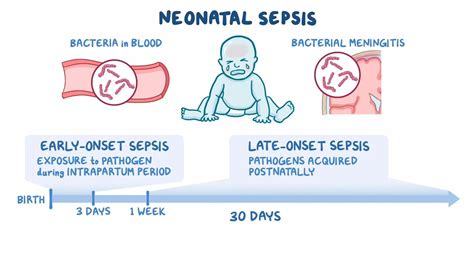
La sepsis neonatal puede clasificarse según su momento de aparición:
Sepsis Neonatal de Inicio Precoz (≤ 3 días desde el nacimiento)
Generalmente, la sepsis de inicio temprano se debe a microorganismos adquiridos durante el parto (intraparto). La mayoría de los recién nacidos presentan síntomas dentro de las 6 horas posteriores al nacimiento.
Los agentes etiológicos más comunes son el estreptococo del grupo B (EGB) y microorganismos entéricos gramnegativos, destacando Escherichia coli (E. coli). Los cultivos vaginales o rectales de mujeres embarazadas a término muestran tasas de colonización por EGB de aproximadamente el 18%, y hasta el 50% de sus hijos pueden colonizarse. La densidad de colonización en el recién nacido influye significativamente en el riesgo de enfermedad invasiva de inicio temprano, siendo mayor en casos de colonización intensa.
Aunque solo un pequeño porcentaje de recién nacidos colonizados desarrollan enfermedad invasiva por EGB, la mayoría de estos casos se manifiestan en las primeras 6 horas de vida. También se ha identificado sepsis por Haemophilus influenzae no tipificable, especialmente en prematuros.
Otros patógenos implicados incluyen bacilos entéricos gramnegativos (ej. especies de Klebsiella), microorganismos grampositivos como Listeria monocytogenes, enterococos (ej. E. faecalis, E. faecium), estreptococos grupo D (ej. Streptococcus bovis), estreptococos alfa-hemolíticos y estafilococos. Menos frecuentemente, se aíslan S. pneumoniae, H. influenzae tipo b y Neisseria meningitidis. La gonorrea no tratada durante el embarazo puede causar sepsis neonatal por N. gonorrhoeae.
Ciertas infecciones virales, como el herpes simple diseminado, enterovirus, adenovirus y virus sincitial respiratorio, también pueden manifestarse con un cuadro de sepsis de inicio temprano o tardío.
Sepsis Neonatal de Aparición Tardía (> 3 días)
La sepsis de inicio tardío suele adquirirse del ambiente (infección neonatal hospitalaria). Los estafilococos son responsables de aproximadamente el 30% al 60% de los casos, a menudo asociados al uso de dispositivos intravasculares, como catéteres vasculares centrales. E. coli se está convirtiendo en una causa importante de sepsis de inicio tardío, particularmente en recién nacidos de peso extremadamente bajo. El aislamiento de Enterobacter cloacae o Cronobacter sakazakii en sangre o líquido cefalorraquídeo puede indicar contaminación de la alimentación. Brotes de neumonía o sepsis hospitalaria por Pseudomonas aeruginosa pueden sugerir contaminación de equipos respiratorios.
Aunque la detección universal y la profilaxis antibiótica intraparto contra EGB han reducido la sepsis de inicio temprano por este microorganismo, la tasa de sepsis de inicio tardío por EGB no ha variado, lo que apoya la hipótesis de que la enfermedad de inicio tardío se contagia principalmente del ambiente.
La participación de anaerobios, como Bacteroides fragilis, en la sepsis de inicio tardío no está completamente esclarecida, aunque se han atribuido muertes a bacteriemia por Bacteroides.
Las especies de Candida son causas cada vez más importantes de sepsis de inicio tardío, especialmente en lactantes con muy bajo peso.
Fisiopatología de la Sepsis Neonatal
Sepsis Neonatal de Inicio Precoz
Diversos factores maternos, obstétricos y perinatales aumentan el riesgo, especialmente de sepsis de inicio temprano. Entre ellos se encuentran la rotura prelabor de membranas (PROM) ≥ 18 horas antes del nacimiento, la infección intraamniótica materna (a menudo manifestada como fiebre materna, leucocitosis, taquicardia, dolor uterino y/o líquido amniótico maloliente), la colonización por estreptococos del grupo B y el parto pretérmino.
La transmisión de patógenos virales (rubéola, citomegalovirus), protozoos (Toxoplasma gondii) y treponemas (Treponema pallidum) puede ocurrir por diseminación hemática y transplacentaria de infecciones maternas. Algunos patógenos bacterianos (ej. L. monocytogenes, Mycobacterium tuberculosis) pueden alcanzar al feto transplacentariamente, pero la mayoría se adquieren por vía ascendente en el útero o durante el parto por contacto con el líquido vaginal infectado.
La intensidad de la colonización materna se correlaciona con el riesgo de enfermedad invasiva en el recién nacido. Sin embargo, hijos de madres con colonización de baja densidad pueden presentar colonización de alta densidad, aumentando su riesgo. El líquido amniótico contaminado promueve el crecimiento de EGB y E. coli. Los microorganismos pueden llegar al torrente sanguíneo por aspiración o deglución fetal de líquido amniótico contaminado, causando bacteriemia.
La vía ascendente de infección explica la alta incidencia de rotura prematura de membranas en infecciones neonatales, la importancia de la inflamación de los anexos (amnionitis), el mayor riesgo de infección en el gemelo más cercano al canal de parto y las características bacteriológicas de la sepsis de inicio temprano, que reflejan la flora vaginal materna.
Sepsis Neonatal de Aparición Tardía
El factor de riesgo más importante para la sepsis de inicio tardío es el parto pretérmino. Otros factores de riesgo incluyen:
- Uso prolongado de catéteres intravasculares.
- Enfermedades asociadas (que pueden ser marcadores de procedimientos invasivos).
- Exposición a antibióticos (que seleccionan cepas resistentes).
- Hospitalización prolongada.
- Contaminación de equipos o soluciones intravenosas o enterales.
Los microorganismos grampositivos (ej. estafilococos coagulasa-negativos y Staphylococcus aureus) pueden provenir del ambiente o de la piel del paciente. Las bacterias entéricas gramnegativas suelen derivar de la flora endógena del paciente, que puede alterarse por antibioticoterapia previa o por transferencia de microorganismos resistentes a través de las manos del personal sanitario o equipos contaminados. Por ello, situaciones como el hacinamiento, el cuidado inadecuado y el lavado de manos inconstante por parte del personal sanitario aumentan las tasas de infección hospitalaria.
Los factores de riesgo para sepsis por especies de Candida son el uso prolongado (> 10 días) de catéteres IV centrales, nutrición parenteral, administración previa de antibióticos (especialmente cefalosporinas de tercera generación) y patología abdominal.
Los focos iniciales de infección pueden ser las vías urinarias, los senos paranasales, el oído medio, los pulmones o el aparato digestivo, desde donde pueden diseminarse a las meninges, riñones, huesos, articulaciones, peritoneo y piel.
Síntomas y Signos de Sepsis Neonatal
Los primeros signos de sepsis neonatal suelen ser inespecíficos y sutiles, dificultando la diferenciación entre microorganismos. Los signos tempranos más frecuentes incluyen:
- Disminución de la actividad espontánea.
- Succión menos enérgica.
- Anorexia.
- Apnea.
- Bradicardia.
- Inestabilidad térmica (hipotermia o hipertermia).
La fiebre se observa en menos del 10% de los recién nacidos, pero cuando es sostenida (ej. > 1 hora), suele indicar infección. Puede presentarse inestabilidad térmica en lugar de fiebre. Otros signos y síntomas son dificultad respiratoria, hallazgos neurológicos (convulsiones, inquietud), ictericia (especialmente dentro de las primeras 24 horas de vida sin incompatibilidad de grupo sanguíneo y con una concentración de bilirrubina directa más alta de lo esperado), vómitos, diarrea y distensión abdominal.
Los signos específicos de un órgano infectado pueden indicar la localización primaria o metastásica:
- Infección por EGB de inicio temprano: Puede debutar con dificultad respiratoria que es difícil de distinguir del síndrome de dificultad respiratoria. Complicaciones obstétricas como parto prematuro, rotura prematura de membranas o infección intraamniótica son frecuentes. La mayoría de los casos se manifiestan dentro de las 6 horas del nacimiento, con puntuación de Apgar disminuida. La meningitis es menos común.
- Infección por EGB de inicio tardío (> 3 días a 12 semanas): Suele cursar con meningitis. Generalmente no se asocia con factores de riesgo perinatales o colonización materna demostrable, pudiendo contagiarse después del parto.
- Onfalitis: Eritema periumbilical, exudado o hemorragia del ombligo sin diátesis hemorrágica sugieren infección que impide la obliteración de los vasos umbilicales.
- Meningitis/Encefalitis/Absceso cerebral: Coma, convulsiones, opistótonos o protrusión de la fontanela.
- Osteomielitis o artritis séptica: Disminución del movimiento espontáneo de una extremidad, tumefacción, calor, eritema o dolor a la palpación sobre una articulación.
- Peritonitis o enterocolitis necrosante: Distensión abdominal sin causa aparente, especialmente si se acompaña de diarrea sanguinolenta y leucocitos en heces.
- Herpes simple diseminado: Vesículas cutáneas, úlceras bucales y hepatoesplenomegalia (particularmente con coagulación intravascular diseminada).
Diagnóstico de la Sepsis Neonatal
El diagnóstico temprano de la sepsis neonatal es crucial y requiere el conocimiento de los factores de riesgo y una alta sospecha clínica, especialmente en recién nacidos de bajo peso. La Neonatal Early-Onset Sepsis Risk Prediction es una calculadora de riesgo clínico para lactantes ≥ 34 semanas de edad gestacional al nacer, validada para entornos de altos recursos.
Evaluación Clínica y Paraclínica
En recién nacidos con signos clínicos de sepsis, se debe realizar:
- Hemograma completo con recuento diferencial y frotis.
- Marcadores inflamatorios: Proteína C Reactiva (PCR), procalcitonina (PCT).
- Hemocultivo: Es el método diagnóstico principal. Los avances en su procesamiento han reducido el tiempo de detección. Se recomienda un volumen de sangre adecuado (al menos 1-2 ml) para maximizar la sensibilidad.
- Urocultivo: Generalmente no es necesario para la evaluación de la sepsis de aparición temprana, pero puede ser útil en casos de sospecha clínica o sepsis de inicio tardío.
- Punción lumbar (PL): Indicada si es clínicamente viable y existe alta sospecha de sepsis, especialmente si hay clínica sospechosa de meningitis. Idealmente se realiza antes del inicio del tratamiento antibiótico, pero no debe retrasar el mismo si el neonato está inestable.
- Radiografía de tórax: En recién nacidos con síntomas respiratorios.
Las técnicas moleculares basadas en la determinación de ADN/ARN bacteriano están siendo cada vez más empleadas por su rapidez y sensibilidad, aunque su coste y disponibilidad pueden ser limitados.
Los hallazgos anormales en la serie blanca (leucocitos, neutrófilos inmaduros/totales) y los reactantes de fase aguda como la PCR y PCT tienen un valor predictivo positivo limitado para la sepsis neonatal, y no deben usarse aisladamente para el diagnóstico. Sin embargo, valores normales seriados de PCR en las primeras 48 horas de vida hacen muy poco probable la presencia de sepsis (buen valor predictivo negativo).
El diagnóstico definitivo de sepsis se confirma por el aislamiento de un patógeno en el cultivo.
Prevención de la Sepsis Neonatal
Prevención de la Sepsis por EGB
La estrategia actual se basa en la identificación de gestantes colonizadas por EGB (10-30%) y la administración de profilaxis antibiótica intraparto (PAI) a las portadoras o a aquellas con factores de riesgo si se desconoce el estado de colonización. La PAI se considera completa si se administra al menos una dosis de penicilina, ampicilina o cefazolina ≥4 horas antes del parto.
Se recomienda el estudio para detectar el estado de portadoras mediante cultivo vagino-rectal en:
- Todas las gestantes entre la semana 36+0 y 37+6 de gestación.
- Si el cultivo se realizó más de cinco semanas antes del parto y es negativo.
- Si hay inicio de trabajo de parto antes de las 37+0 semanas.
- Si se produce rotura pretérmino, prematura (pre-parto) de membranas.
No es necesario el cultivo en gestantes con un hijo anterior con infección neonatal por EGB o si se ha detectado EGB en orina en la gestación actual, ya que en ambos casos está indicada la PAI.
La PAI no es efectiva para la prevención de la sepsis tardía por EGB.
Calculadora de Riesgo de Sepsis
Esta herramienta, basada en modelos de predicción multivariante, combina factores de riesgo perinatales y datos clínicos neonatales para estimar el riesgo individual de sepsis. Su uso ha demostrado una reducción significativa en el uso innecesario de antibióticos y pruebas analíticas.
Tratamiento de la Sepsis Neonatal
El tratamiento empírico inicial de la sepsis neonatal suele basarse en la combinación de gentamicina con ampicilina. Esta combinación es efectiva contra EGB, la mayoría de los estreptococos, enterococos y L. monocytogenes. Ante la sospecha clínica, se inicia tratamiento antibiótico empírico mientras se esperan los resultados de los cultivos.
La elección del antibiótico y la duración del tratamiento se ajustan según los resultados microbiológicos, la respuesta clínica del paciente y los patrones de resistencia locales. En casos de sepsis confirmada, el tratamiento suele prolongarse durante 7 a 21 días, dependiendo del patógeno y la localización de la infección.
La retirada precoz de la antibioterapia a las 36-48 horas si el hemocultivo es negativo es una estrategia recomendada para minimizar la exposición innecesaria a antibióticos y sus potenciales efectos adversos.