La embriología clínica se encuentra en una fase temprana de desarrollo, ofreciendo avances impresionantes y promesas de un futuro con amplias y difíciles de calcular posibilidades. Las manipulaciones sobre el embrión humano joven se han vuelto posibles gracias a la confluencia de dos subespecialidades médicas de reciente creación: la Medicina de la Reproducción (Procreática) y la Genética Médica.
Gracias a la Medicina de la Reproducción, se ha profundizado la comprensión de los mecanismos físicos de la transmisión de la vida humana, multiplicando el conocimiento sobre la biología y las enfermedades del embrión. Por su parte, la Genética Médica, especialmente la Genética Molecular, ha aportado y seguirá aportando significativamente para entender la constitución del ser humano, cómo se construyen nuestros rasgos característicos, las ventajas y debilidades hereditarias, y cómo corregir errores genéticos.
Sin embargo, estos progresos técnicos han venido acompañados de una creciente responsabilidad ética. Tanto la Embriología Clínica como la Genética Médica son ahora plenamente conscientes de la enorme capacidad de manipular al ser humano que han adquirido.
Oportunidades y Técnicas en la Embriología Clínica
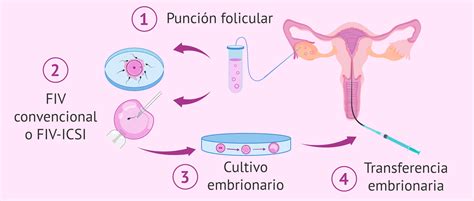
Las oportunidades que ofrece la Embriología Clínica están, en su mayoría, ligadas a la fecundación in vitro (FIVET). En los años transcurridos desde el nacimiento de la primera "niña probeta", la reproducción asistida se ha divulgado y vulgarizado considerablemente. Hoy en día, la producción de embriones in vitro requiere instalaciones relativamente sencillas y cierta destreza y experiencia.
Las técnicas para obtener ovocitos mediante estimulación ovárica, su cultivo y maduración in vitro, así como su fecundación con semen capacitado para producir zigotos (embriones unicelulares), se han simplificado.
Intervenciones Genéticas en Embriones
Los embriones jóvenes pueden ser objeto de diversas intervenciones genéticas, incluyendo pruebas diagnósticas para determinar la presencia de anormalidades cromosómicas y genéticas. Ante el diagnóstico de una enfermedad, existen dos conductas divergentes posibles.
Además, la exploración de nuevas posibilidades técnicas para transferir genes -es decir, incluir en el genoma de las células un fragmento de ADN que corresponde a un gen- abre una vía cada vez más amplia a la terapia génica. La terapia de los defectos génicos es una realidad incipiente, aunque aún con mucho por aprender antes de ser plenamente integrada en el arte médico.
Las células embrionarias, los blastómeros y las células madre de diversos tejidos revelan propiedades fascinantes en estudios experimentales, tanto in vitro como in vivo. Se van conociendo las sustancias moduladoras que actúan como factores de crecimiento y diferenciación, y que modifican, a veces de manera sorprendente, la conducta espontánea de estas células.
Diagnóstico y Terapia Génica del Embrión: Estado Actual y Normativas
Para abordar el diagnóstico y terapia génica del embrión, es necesario considerar dos grupos de datos: el estado actual del diagnóstico y terapia génicos del embrión, y las normas deontológicas y jurídicas vigentes.
Aplicaciones del Diagnóstico Genético en Embriones
En principio, la aplicación del diagnóstico genético al embrión in vitro podría darse en dos tipos de situaciones:
- Detección de alteraciones genéticas de incidencia relativamente elevada, que se producen sin antecedentes familiares de enfermedad genética.
- Enfermedades de transmisión hereditaria conocida, con antecedentes inmediatos en la familia.
En el primer caso, se trata de un cribado genético, aplicado sistemáticamente a la población general o a sectores de mayor riesgo, como la detección de la trisomía 21 (síndrome de Down) en embarazadas de edad avanzada. En ambos casos, el estudio genético puede realizarse durante la gestación, a menudo asociado a la interrupción del embarazo en casos de deficiencia embrionaria (aborto de indicación eugenésica).
Análisis Genético Preimplantacional
También es posible analizar genéticamente al embrión antes de su implantación en el útero. Esto se puede realizar durante la fase in vitro de la FIVET, aunque presenta dificultades éticas significativas desde ciertas perspectivas morales.
Mediante simple observación microscópica del zigoto, se pueden diagnosticar alteraciones genéticas groseras. Por ejemplo, la presencia de tres pronúcleos en el citoplasma ovular, indicativo de una situación de gravedad biológica extrema, puede deberse a la penetración de dos espermatozoides o a la no eliminación del segundo corpúsculo polar.
Se han intentado intervenciones de microcirugía para liberar al embrión triploide del núcleo sobrante. Esta operación exige gran pericia y fortuna, y hasta ahora pocos han logrado completarla con éxito. El trauma de la introducción de la micropipeta y la aspiración del núcleo, junto con la necesidad de extraer específicamente uno de los dos pronúcleos sobrantes, hacen que el margen de error sea mínimo. Una equivocación podría resultar en la formación de estructuras tumorales (teratomas o mola hidatidiforme androgénica). Aunque los pronúcleos paterno y materno difieren en aspecto, el error no puede descartarse con plena seguridad. Las perspectivas de esta microcirugía no son halagüeñas.
El problema de la triploidía es menos significativo en la reproducción humana ordinaria, pero aumenta en la reproducción asistida, donde el 5% de los ovocitos fecundados in vitro presentan tres o más pronúcleos.
Esperanzas en el Diagnóstico Genético Molecular
Donde se depositan más esperanzas es en la aplicación de técnicas de diagnóstico genético mediante el análisis del cariotipo o el uso de sondas génicas. Esto permitirá distinguir entre zigotos normales y aquellos afectados por una enfermedad genética.
Las alteraciones cromosómicas son frecuentes en el zigoto. Se han observado anomalías cromosómicas en un porcentaje considerable de ovocitos no fecundados y en embriones (entre el 23% y el 40%).
Procedimiento del Diagnóstico Genético Preimplantatorio (DGP)
El programa de trabajo para el diagnóstico génico del embrión preimplantatorio implica:
- Cultivar el zigoto in vitro hasta la fase de embrión de cuatro, ocho o más células.
- Perforar la membrana pelúcida con una micropipeta cortante o aplicando solución de Tyrode ácida (técnica agresiva para el embrión humano).
- Extraer, mediante aspiración, extrusión o división mecánica, uno o varios blastómeros.
Este procedimiento exige una extraordinaria habilidad de micromanipulación. Si el embrión se encuentra en fase de blastocisto, se pueden extraer células del trofectodermo, que formarán la placenta. Si el diagnóstico requiere tiempo, el embrión puede ser congelado a muy baja temperatura.
A menudo, es conveniente cultivar las células extraídas para trabajar con un mayor número de ellas. Las técnicas de diagnóstico genético preimplantatorio actuales funcionan como un sistema de cribado: si el embrión cumple los requisitos de normalidad, se procede a su transferencia intrauterina. Aquellos que no los cumplen, son privados de la oportunidad de desarrollarse.

La Cuestión de la Terapia Génica en Embriones
Surge la pregunta: ¿por qué no curar al embrión en lugar de descartarlo? La terapia del embrión preimplantatorio es un proyecto a futuro. El simple hecho de congelar y descongelar embriones intactos conlleva la muerte de más de la mitad de ellos.
Consenso Ético y Jurídico sobre la Modificación Genética
Existe un consenso casi universal en la comunidad científica y la sociedad sobre la distinción entre dos áreas:
- Terapia génica de células somáticas: No presenta reparos éticos especiales.
- Modificación genética de células germinales (gametos, zigotos y embriones jóvenes): Está prohibida por ley o sujeta a una moratoria indefinida.
Este consenso se basa en el temor prudente y razonable de daños transmisibles a la progenie, y el rechazo a la posibilidad de que la terapia génica se utilice para fines de mejora de la raza o producción de "superhombres". Esto otorga tiempo para madurar la respuesta a preguntas fundamentales sobre el estatus ético del embrión humano.
Perspectivas Jurídicas y Regulatorias
Diversos documentos abordan la manipulación genética. La resolución del Parlamento Europeo A 2-327/88 prohibió experimentos que modificaran arbitrariamente el programa genético humano, impuso sanciones penales por la transferencia de genes a gametos humanos, y abogó por una definición del rango jurídico del embrión que garantizara su identidad genética.
La legislación alemana es particularmente enérgica en la prohibición de intervenciones genéticas sobre embriones humanos.
Las Consideraciones Éticas sobre las Nuevas Tecnologías Reproductivas de la American Fertility Society adoptan una postura intermedia, que ha evolucionado con el tiempo. La única barrera a la experimentación sobre embriones humanos parecía ser el temor a demandas por "wrongful life" (vida errónea).
Legislación en España
En España, la Ley 35/1988, de Reproducción Asistida, es moderadamente permisiva, autorizando la investigación en preembriones in vitro viables con fines diagnósticos, terapéuticos o preventivos, siempre que no se modifique el patrimonio genético no patológico. Esto sugiere la tolerancia a intervenciones que beneficien médicamente al embrión actuando sobre sus genes anormales. Sin embargo, la ley separa las normas de diagnóstico y tratamiento de las de investigación, creando dificultades para la aplicación clínica de hallazgos experimentales.
Se prohíbe la utilización de gametos o preembriones investigados para originar preembriones con fines de procreación, y la transferencia de gametos o preembriones sin garantías biológicas o de viabilidad, limitando drásticamente la aplicación terapéutica de la experimentación.
Perspectiva Médica y Deontológica
En España, el Código de Ética y Deontología Médica de la Organización Médica Colegial establece que al ser humano embriofetal enfermo se le debe tratar con las mismas directrices éticas que a otros pacientes, incluido el consentimiento informado de los progenitores. La continuidad de la vida humana exige una continuidad del respeto ético y la asistencia médica.
La naciente Medicina Embriofetal, como especialidad, se rige por criterios éticos comunes a toda la Medicina. No es tolerable la eliminación de vidas poco valiosas ni el cribado genético o la destrucción sistemática de embriones o fetos enfermos, como ocurre en la "reducción selectiva". El embrión y el feto enfermo deben beneficiarse del progreso médico.
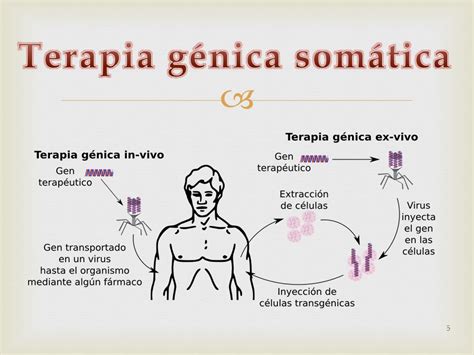
Terapia Génica Somática vs. Terapia Génica Germinal
La mayoría de los investigadores coinciden en los potenciales beneficios de aplicar la terapia génica a personas nacidas con mutaciones genéticas que les causan enfermedades graves, considerando esto un imperativo moral. Existen numerosos ensayos clínicos en desarrollo para esta estrategia.
La terapia génica somática, aplicada a personas nacidas, modifica genes que no afectan a la línea germinal y, por tanto, las alteraciones genéticas desaparecen con la muerte del individuo y no se transmiten a la descendencia. Es posible realizarla en la mayoría de los países con las tecnologías adecuadas.
La terapia génica germinal, en cambio, modifica el genoma de un embrión, afectando al individuo que nacerá y transmitiendo esas modificaciones a sus descendientes. Afecta a todas las células del individuo, incluidas las de la línea germinal.
Regulación Internacional de la Terapia Génica Germinal
La terapia génica germinal está estrictamente prohibida en países como España, que firmaron el Convenio de Oviedo, el cual impide la modificación genética del genoma de la descendencia (art. 13).
Un estudio de 2020 sobre 106 países reveló que la mayoría no tiene normas específicas para regular la modificación genética de embriones humanos en laboratorio. De los que sí tienen legislación específica, 23 países prohíben estas técnicas, mientras que 11 las permiten. En 75 de los 96 países analizados, está explícitamente prohibido iniciar una gestación con embriones humanos modificados genéticamente, aunque existen excepciones en cinco países.
Ningún país permite explícitamente la edición genética heredable en humanos.
La edición genética es centro de fuertes debates éticos en el mundo
Debate y Recomendaciones sobre Edición Genética Heredable
A pesar de las prohibiciones, la terapia génica germinal ha sido objeto de intensos debates y publicaciones. Informes de la Academia Nacional de Ciencias de EE. UU. (2017, 2020) han delimitado criterios para la edición genética heredable en embriones humanos con fines reproductivos, cuando sea posible garantizar que los cambios se limiten a los genes deseados y no afecten a otros, algo aún no logrado.
En 2021, la Organización Mundial de la Salud emitió recomendaciones para la edición genética heredable de embriones humanos con fines reproductivos.
Diagnóstico Genético Preimplantatorio (DGP) y sus Límites
El DGP es una tecnología utilizada desde hace décadas para la detección de patologías hereditarias monogénicas. Funciona analizando el ADN de embriones obtenidos por FIV.
En general, poseemos dos copias de la mayoría de los genes, una heredada del padre y otra de la madre. Mientras una copia sea funcional, no suele haber problemas (herencia autosómica recesiva). La enfermedad aparece solo si ambas copias están mutadas.
- Mutaciones recesivas: Son las más frecuentes y causan enfermedades raras como la fenilcetonuria o la fibrosis quística. Si ambos progenitores son portadores de mutaciones recesivas en el mismo gen, existe un 25% de probabilidad en cada embarazo de concebir un hijo con ambas copias mutadas y, por ende, la enfermedad. En estos casos, el DGP permite seleccionar embriones sanos.
- Mutaciones dominantes: Basta una sola copia mutada de un gen para desarrollar la enfermedad. Son más peligrosas y menos frecuentes. Ejemplos son la enfermedad de Huntington o la acondroplasia. Si uno de los progenitores está afectado, el DGP puede seleccionar embriones sanos (sin la copia mutada).

Circunstancias en las que el DGP no es Útil
Existen dos únicas circunstancias en las que el DGP no sería útil:
- Herencia autosómica recesiva: Si ambos progenitores están afectados (portan las dos copias mutadas del gen), todos sus hijos nacerán con las dos copias mutadas y manifestarán la enfermedad. No habrá embriones sanos para seleccionar.
- Herencia autosómica dominante: Si un progenitor está afectado y porta las dos copias del gen mutadas, todos sus hijos recibirán al menos una copia mutada y desarrollarán la enfermedad. No habrá embriones sanos seleccionables mediante DGP.
En estas dos situaciones, la terapia génica germinal sobre embriones podría ser teóricamente considerada.
Evaluación de la Necesidad y Viabilidad de la Edición Génica Germinal
La posible utilización de técnicas de edición genética en embriones humanos con fines reproductivos y heredables (terapia génica germinal) solo tendría sentido en los dos escenarios especiales descritos anteriormente.
Sin embargo, la frecuencia de estos escenarios es extremadamente baja. Investigaciones de 2019 indican que, en el caso de mutaciones autosómicas dominantes donde un progenitor porta dos copias mutadas, la situación es prácticamente inexistente, con muy pocas descripciones de personas afectadas y en edad reproductiva. Esto sugiere que la discusión sobre la necesidad de edición génica germinal podría estar sobredimensionada en la práctica.
Proyectos y Empresas en el Campo de la Edición Genética
Existen proyectos y empresas que buscan ampliar las aplicaciones de la edición genética más allá de la prevención de enfermedades graves, orientándose hacia la detección de habilidades cognitivas, intelectuales, características físicas o comportamientos deseables.
- PolygenX (Heliospect Genomics): Pretende mejorar la salud y el bienestar humanos mediante predicción genómica, analizando datos de DGP para predecir características de los hijos (incluyendo coeficiente intelectual, longevidad, características físicas). Esta práctica, aunque no legal en Europa (salvo Reino Unido), se presenta en EE. UU. como asesoramiento genético.
- Manhattan Genomics: Propone modificar el núcleo celular para un futuro sin niños con enfermedades prevenibles y con caracteres deseables, utilizando técnicas como CRISPR/Cas9 para corregir enfermedades hereditarias en embriones. Defiende el desarrollo cuidadoso y transparente de esta tecnología.
- Preventive: También apuesta por la edición génica con CRISPR/Cas9 en embriones humanos, evaluando la seguridad de esta tecnología para prevenir el nacimiento de bebés con enfermedades graves.
Estas iniciativas a menudo cuentan con el respaldo de sectores elitistas y posturas favorables a las nuevas tecnologías.
Riesgos y Limitaciones de la Edición Genética en Embriones
La modificación genética de embriones humanos implica un doble riesgo:
- Inseguridad de las técnicas: No garantizan éxito total y pueden producir efectos colaterales no deseados, alterando regiones del genoma distintas a las dianas moleculares y generando errores en la línea germinal transmisibles a futuras generaciones.
- Complejidad de los caracteres: Dificultad para comprender no solo las secuencias génicas, sino también los factores epigenéticos y ambientales que influyen decisivamente en caracteres complejos.
Rasgos como la inteligencia, la longevidad o la empatía no están determinados exclusivamente por los genes. El desarrollo intelectual y la conducta se forjan bajo la influencia del entorno, la educación, las relaciones personales y otros factores externos. Los factores epigenéticos también contribuyen a la individualidad humana.
Fomentar el esfuerzo personal, la educación y una vida saludable resulta más eficaz para tener hijos sanos y con mayores capacidades que intentar modificar los genes.
Consideraciones Bioéticas Fundamentales
Es éticamente inaceptable instrumentalizar a los embriones humanos, considerándolos vidas humanas en una fase temprana de desarrollo. Las prácticas que implican su selección o eliminación, o la aplicación de técnicas inseguras, no pueden tener una valoración moral positiva.
El Episodio de He Jiankui y la Moratoria
El experimento de He Jiankui en 2018, que resultó en el nacimiento de dos niñas a partir de embriones genéticamente modificados (alterando el gen CCR5 para resistencia al VIH), supuso un salto imprudente, desoyendo la moratoria sobre la edición genética germinal y los riesgos conocidos.
Este evento generó un debate sobre la necesidad de crear un observatorio internacional interdisciplinario para encauzar este tipo de investigaciones.
Voces como las de Julian Savulescu, Peter Singer y George Church se han alzado a favor de la edición de la línea germinal con fines de mejoramiento humano, oponiéndose a la moratoria.
Eugenesia y Dignidad Humana
La selección y manipulación del perfil genético humano constituye una forma de eugenesia. Esta "neoeugenesia" o "eugenesia liberal", al igual que la eugenesia social del siglo XX, valora a las personas en función de sus características genéticas. La diferencia radica en que ahora se seleccionan los hijos, permitiendo la eliminación de miles de embriones, cada uno representando una vida humana en su fase inicial de desarrollo, e introduciendo alteraciones genéticas con consecuencias imprevisibles para las generaciones futuras.
Marco Regulatorio Internacional y Nacional
El Convenio sobre Derechos Humanos y Biomedicina (Convenio de Oviedo), aprobado en 1997, subraya la necesidad de respetar al ser humano y garantizar su dignidad. Su artículo 18 prohíbe la creación de embriones in vitro con fines de experimentación.
La Declaración Universal sobre el Genoma Humano y los Derechos Humanos de la UNESCO (1997) afirma que el genoma humano es patrimonio de la humanidad y base del reconocimiento de su dignidad intrínseca.
Posición del Reino Unido y Otros Países
El Reino Unido, impulsor del concepto de "preembrión" para embriones in vitro de menos de 14 días, no se adhirió al Convenio de Oviedo y ha promovido innovaciones tecnológicas menos respetuosas con la vida humana en sus etapas iniciales, como embriones quimera humano-animal, "hermanos salvadores", embriones triparentales o edición genómica en embriones. Muchas de estas prácticas han sido adoptadas posteriormente por otros países, especialmente Estados Unidos y China.
Situación en España
En España, el referente debería ser el Convenio de Oviedo y el Código de Deontología Médica, que afirma que el ser humano es un fin en sí mismo desde la concepción hasta la muerte. Sin embargo, la Ley de Técnicas de Reproducción Asistida de 1988 y sus reformas introducen el término "preembrión", reduciendo el estatus moral de los embriones de menos de 14 días y exponiéndolos a la instrumentalización.
Conclusiones sobre el DGP y la Edición Genética
Las tecnologías del DGP y de la edición genómica en embriones humanos no solo resultan éticamente inaceptables por implicar la eliminación de miles de vidas humanas, sino que además están sobrevaloradas en cuanto a su eficacia y seguridad reales.
No se conocen los genes que determinan muchos de los caracteres que se prometen mejorar, y estas prácticas suponen una grave amenaza para la vida humana en su etapa más vulnerable. A pesar de ello, se observa un auge de nuevas empresas biotecnológicas dispuestas a desafiar los límites éticos y ampliar el campo de la manipulación genética humana.