La hemorragia obstétrica, y de manera particular la hemorragia posparto (HPP), se erige como una de las principales causas de morbilidad y mortalidad materna a nivel mundial. Actualmente, continúa siendo la causa directa más frecuente de muerte materna, representando aproximadamente una cuarta parte de las muertes y de los resultados adversos graves para la salud de la madre. La incidencia de la HPP presenta una notable variabilidad entre regiones, observándose la prevalencia más alta en África y la más baja en Asia. A nivel global, la hemorragia es responsable de aproximadamente el 27.1% de las muertes maternas, consolidándose como la principal causa de mortalidad materna.
En México, las zonas rurales y marginadas experimentan tasas más elevadas de complicaciones obstétricas, lo cual se atribuye a la falta de acceso a atención médica adecuada y oportuna. Un obstáculo significativo para dimensionar la problemática y los factores de riesgo de la HPP es la ausencia de una definición universalmente aceptada.
Definiciones Clave
Existen diversas definiciones para la hemorragia obstétrica y la HPP:
- Hemorragia obstétrica: Se define como la pérdida de sangre que ocurre durante el embarazo, el parto o el puerperio, la cual puede manifestarse a través de los genitales externos o de forma interna hacia la cavidad peritoneal.
- Hemorragia posparto (HPP): Se refiere a la pérdida de sangre que ocurre después del parto. Tradicionalmente, se define como una pérdida superior a 500 ml tras un parto vaginal y más de 1,000 ml después de una cesárea.
Es fundamental considerar que los cambios fisiológicos inherentes al embarazo pueden enmascarar los signos de hipovolemia, lo que a su vez puede retrasar el diagnóstico y tratamiento de la pérdida de sangre. La estimación visual de la pérdida de sangre a menudo resulta inexacta, ya sea por la contaminación con líquido amniótico o por la posibilidad de que la sangre esté oculta internamente o en los paños.
Mecanismos Fisiológicos y Cambios en la Gestación
El embarazo cursa con cambios fisiológicos significativos que impactan el sistema hemostático:
Cambios Fisiológicos del Embarazo
- Aumento de la masa eritrocitaria y volumen plasmático: Se produce un incremento del 20-30% en la masa eritrocitaria y del 50% en el volumen plasmático, lo que resulta en una anemia fisiológica dilucional.
- Estado hipercoagulable: Existe un estado de hipercoagulación propio del embarazo, caracterizado por un aumento en la concentración plasmática de la mayoría de los factores de la coagulación (fibrinógeno, factores VII, VIII y IX). Paralelamente, el sistema fibrinolítico ve disminuida su actividad, aunque el plasminógeno está aumentado, su actividad se reduce debido al incremento del inhibidor del plasminógeno tipo II. Se observa una hiperfibrinogenemia fisiológica.
- Descenso de anticoagulantes naturales: Anticoagulantes naturales como la proteína S disminuyen, contribuyendo a un estado protrombótico y a un aumento de la fibrinólisis, especialmente en el útero al momento de la separación placentaria.
- Trombocitopenia gestacional: Puede presentarse una trombocitopenia gestacional fisiológica sin que esto se traduzca clínicamente en un aumento de la tendencia hemorrágica.
Estos cambios fisiológicos conducen a un acortamiento del tiempo de protrombina (TP) y del tiempo parcial de tromboplastina activado (aPTT), así como a un incremento de parámetros tromboelastográficos como la máxima firmeza del coágulo y la máxima amplitud. Algunas comorbilidades asociadas al embarazo pueden exacerbar la aparición de una hemorragia catastrófica con coagulopatía de consumo.
Monitorización de la Hemostasia y Fisiopatología de la Coagulopatía
La monitorización de la hemostasia en una hemorragia obstétrica masiva (HMO) suele realizarse mediante test de coagulación rutinarios. Sin embargo, estas pruebas pueden ser lentas en una situación tan dinámica y su sensibilidad puede no ser la más adecuada. El método de Clauss es una opción para valorar el nivel de fibrinógeno plasmático.
El uso de sistemas de point of care como la tromboelastografía (TEG) o la tromboelastometría (ROTEM) ofrece ventajas significativas. Estos métodos evalúan las propiedades viscoelásticas de la coagulación de forma global, permitiendo valorar la formación y lisis del coágulo en pocos minutos. Su aplicación a pie de cama facilita la toma de decisiones clínicas precoces y una valoración global de la coagulación, promoviendo una reposición agresiva y decidida de hemoderivados.
Las pacientes obstétricas con HMO presentan con frecuencia y de manera precoz alteraciones graves de la coagulación que requieren tratamiento individualizado. Los test viscoelásticos permiten la administración de hemocomponentes (plasma fresco y plaquetas) y de concentrados de factores de coagulación de manera ajustada a las necesidades específicas.
La tipología, gravedad e incidencia de la coagulopatía varían según la etiología de la hemorragia. En casos de atonía uterina y desgarros del canal del parto, la coagulopatía predominante es la dilucional. Por el contrario, en el desprendimiento de placenta, se inicia rápidamente una coagulopatía de consumo, caracterizada por hipofibrinogenemia y trombocitopenia, incluso con pérdidas iniciales de sangre relativamente escasas.
La coagulopatía de consumo auténtica se observa en la embolia de líquido amniótico, ciertos casos de preeclampsia grave o síndrome HELLP, y el desprendimiento placentario grave. En estas situaciones, los niveles de fibrinógeno plasmático pueden alcanzar rápidamente niveles críticos. La activación local de la coagulación y del sistema fibrinolítico en el lecho placentario también contribuye a la rápida instauración de la coagulopatía por consumo.
Los cambios en la coagulación observados en el embarazo, evaluados con ROTEM, objetivan un estado de hipercoagulabilidad, con tiempos de coagulación más cortos y firmezas del coágulo más amplias. Los dinteles para instaurar tratamiento pueden diferir de los de otros pacientes críticos. Existe una buena correlación entre los parámetros estándar de coagulación y los valores de ROTEM en el posparto inmediato. Asimismo, se ha encontrado correlación entre el ROTEM FIBTEM y la concentración de fibrinógeno, pudiendo el ROTEM FIBTEM A5 (disponible en 10 minutos) usarse de forma equivalente a la medición de fibrinógeno por el método de Clauss.
Tratamiento Médico de la Hemorragia Obstétrica
El correcto reconocimiento de una HMO es vital, ya que el retraso en el manejo se asocia a acidosis metabólica, hipotermia, coagulopatía y anemia, una combinación potencialmente letal. Se recomienda la corrección temprana de estos factores.
Medidas Generales y Reanimación con Líquidos Intravenosos
La corrección de la hipovolemia mediante la administración intravenosa de cristaloides y/o coloides es prioritaria ante cualquier tipo de hemorragia aguda. Una vez que la pérdida estimada supera los 1,000 ml y la hemorragia persiste, se recomienda canalizar dos vías venosas periféricas de grueso calibre, iniciar la administración de cristaloides calentados y enviar una muestra al banco de sangre para grupo y escrutinio de anticuerpos irregulares.
La reanimación con líquidos intravenosos debe ser rápida, sin confiarse únicamente en los resultados de hemoglobina. La discusión sobre la estrategia más adecuada para la reposición de la volemia puede ser extensa. El volumen máximo a infundir debería limitarse, no excediendo de 3.5 litros (hasta 2 litros de cristaloides calentados lo más rápido posible), ampliable a otros 1,500 ml mientras se espera la llegada de sangre compatible. Es importante recordar que la administración excesiva de líquidos puede conducir a una coagulopatía dilucional.
Los cristaloides más empleados incluyen la solución salina isotónica al 0.9%, la solución de Ringer y otras soluciones balanceadas como la de Hartmann (Ringer lactato). Estos son económicos, no alteran la hemostasia ni la función renal, y cuentan con una amplia experiencia de uso. Sin embargo, solo aproximadamente el 25% del volumen administrado permanece en el espacio intravascular.
Los coloides, aunque tienen un mayor efecto sobre el volumen intravascular, pueden inhibir la agregación plaquetaria e interferir con la medición precisa de los niveles de fibrinógeno. Los coloides disponibles son los hidroxietil-almidones, las gelatinas y la albúmina humana. La infusión de albúmina al 5% expande el plasma en un 75% del volumen infundido. Las gelatinas, debido a su bajo peso molecular, tienen una vida media intravascular corta (2-3 horas) y una capacidad expansora limitada (70-80%). Los hidroxietil-almidones al 6% presentan una vida media intravascular más larga (6-8 horas) y una mayor capacidad expansora (80-120%).

Agentes Uterotónicos
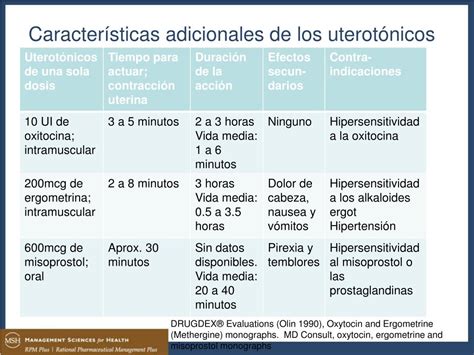
La evaluación de la eficacia y seguridad de los diferentes uterotónicos es crucial para optimizar los protocolos de manejo de la hemorragia obstétrica. Agentes como la oxitocina, el misoprostol y la carbetocina han demostrado efectividad, aunque presentan perfiles específicos de acción, costo y disponibilidad. Estos fármacos actúan aumentando la fuerza, frecuencia y/o efectividad de las contracciones uterinas, ya sea para la inducción o conducción del trabajo de parto (o aborto), o para disminuir el sangrado posparto.
Es común administrar un uterotónico de forma profiláctica durante la tercera etapa del trabajo de parto o posterior a la cesárea. Sin embargo, la práctica clínica y la investigación muestran una considerable heterogeneidad y variabilidad.
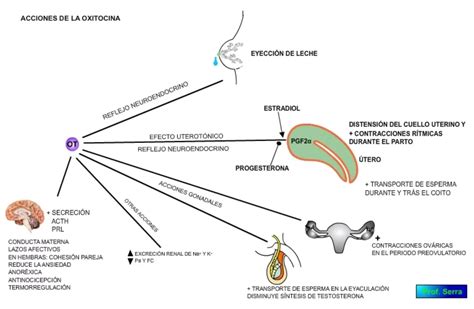
Oxitocina
La oxitocina es una hormona peptídica sintetizada en el hipotálamo y liberada desde la hipófisis posterior. Sus receptores se encuentran distribuidos en el miometrio, endometrio, sistema cardiovascular y sistema nervioso central. Al unirse a un receptor acoplado a proteína G, eleva el calcio intracelular, activando la cinasa de la cadena ligera de miosina y favoreciendo la formación de actomiosina, lo que desencadena contracciones uterinas.
Es el uterotónico más frecuentemente utilizado. En dosis bajas induce contracciones rítmicas similares a las del trabajo de parto espontáneo, mientras que dosis elevadas pueden provocar contracciones continuas, con riesgo de taquifilaxia y rotura uterina iatrogénica. Este mismo mecanismo es el que permite aumentar el tono uterino en la tercera fase del trabajo de parto y el puerperio para controlar la HPP.
Debido a su corta vida media, la oxitocina suele administrarse como bolo intravenoso seguido de una infusión continua para mantener el tono uterino adecuado. Estudios recientes sugieren que la dosis efectiva para lograr un tono uterino adecuado es menor que las dosis históricamente utilizadas. Investigaciones han indicado que dosis bajas, como 1 UI, pueden ser suficientes para obtener un tono uterino inicial adecuado en cesáreas electivas en mujeres sanas. Para la prevención activa de la tercera etapa del trabajo de parto, se puede considerar una dosis inicial en bolo IV de 0.35-1.0 UI, sin sobrepasar los 5 UI.
El manejo de infusiones IV de oxitocina posterior al bolo inicial requiere un control cuidadoso. En América del Norte, es común administrar oxitocina mediante infusiones rápidas no reguladas. Estudios han estimado velocidades de infusión óptimas para lograr un tono uterino adecuado, sugiriendo que una infusión de aproximadamente 17.4 UI/h podría ser suficiente. Las mujeres que reciben oxitocina para la conducción del trabajo de parto pueden requerir dosis más altas debido a una posible desensibilización de los receptores.
Carbetocina
La carbetocina es un análogo sintético de la oxitocina con un inicio de acción rápido y una vida media prolongada (40-60 minutos por vía intravenosa), lo que permite su administración en bolo sin necesidad de una infusión de mantenimiento. Presenta una mayor lipofilia que la oxitocina, lo que contribuye a su vida media extendida. Es estable a temperaturas elevadas, lo que la hace útil en contextos con recursos limitados.
Aunque su perfil de efectos secundarios es similar al de la oxitocina, estudios de determinación de dosis sugieren que dosis más bajas pueden ser apropiadas en cesáreas. La dosis efectiva para cesáreas electivas se ha estimado en torno a los 14.8 μg. En mujeres sometidas a cesáreas intraparto, especialmente si se requieren dosis superiores a 100 μg, la carbetocina debe administrarse con precaución. En mujeres con obesidad mórbida, la dosis efectiva estimada es mayor (aproximadamente 62.9 μg). Se puede considerar en situaciones donde no se puede asegurar la integridad de la oxitocina, con dosis clínicamente efectivas que varían de 15 a 63 μg por vía IV o 100 μg IM para profilaxis poscesárea programada o parto en embarazos no complicados.
Ergots y Prostaglandinas
Si la oxitocina o la carbetocina no logran un tono uterino adecuado, se debe considerar de manera temprana un fármaco de segunda línea, como los ergots o los análogos de prostaglandinas.
Alcaloides del Cornezuelo de Centeno (Ergots)
Estos fármacos, derivados del compuesto 6-metilergolina, se administran generalmente por vía intramuscular a una dosis de 0.2 mg, con inicio de acción en 2-3 minutos y efectos uterotónicos que duran varias horas. Pueden administrarse en bolo IV lento, aunque esta vía está desaconsejada en algunos países. Los efectos adversos comunes incluyen náuseas y vómitos. Las contraindicaciones relativas abarcan preeclampsia, otros trastornos hipertensivos, enfermedad vascular periférica y enfermedad cardíaca isquémica.
Prostaglandinas
Las prostaglandinas de las familias E y F se utilizan como agentes de tratamiento de segunda línea para la atonía uterina. El carboprost, un análogo sintético de la prostaglandina F2α, se administra a una dosis recomendada de 0.25 mg por vía IM, con un pico plasmático máximo en 20-30 minutos. La inyección intramiometrial es una vía alternativa, aunque "fuera de indicación". Los efectos secundarios comunes incluyen fiebre, escalofríos, diarrea, náuseas y vómitos. El broncoespasmo es un efecto adverso respiratorio raro pero potencialmente mortal.
El misoprostol, un análogo sintético de la prostaglandina E1, es económico y fácil de almacenar, siendo termoestable. Puede administrarse por vía oral, bucal, sublingual, vaginal y rectal (aunque estas últimas vías son off label o menos prácticas en el contexto de HPP). Las vías sublingual y oral ofrecen un inicio de acción más rápido. Para el tratamiento de la HPP, se ha recomendado misoprostol oral o sublingual de 600 μg. Las dosis repetidas no se recomiendan por al menos 2 horas. La incidencia y gravedad de los efectos adversos están relacionados con la dosis y la vía de administración, siendo más frecuentes con dosis ≥ 600 μg.
Calcio Intravenoso
El calcio intravenoso ha surgido como un agente uterotónico prometedor, gracias a su rol fundamental en la activación del complejo calmodulina-miosina cinasa, indispensable para las contracciones uterinas efectivas. La administración de 1 g de cloruro de calcio o 3 g de gluconato de calcio genera un incremento significativo en las concentraciones de calcio ionizado, alcanzando un pico máximo en los primeros 10 minutos tras su infusión.
Protocolo Médico-Quirúrgico de la Hemorragia Posparto Masiva
La hemorragia posparto masiva (HPM) es una causa principal de morbimortalidad materna. Se define, entre otras formas, como la pérdida de más de 2,500 ml de sangre, asociada a ingreso en unidades de cuidados intensivos y/o histerectomía. Los cambios fisiológicos del embarazo, como la hemodilución relativa y el alto gasto cardíaco, permiten una hemorragia cuantiosa antes de que se objetive una caída en la hemoglobina y/o el hematocrito.
La hipercoagulabilidad asociada a la gestación, junto con comorbilidades, puede contribuir a hemorragias catastróficas con coagulopatía de consumo. La optimización, preparación, uso racional de recursos y la protocolización de actuaciones son cruciales para mejorar los resultados. El uso de protocolos basados en point of care con test viscoelásticos está demostrando utilidad.
Si se identifica hipofibrinogenemia durante el episodio de hemorragia, la administración precoz de fibrinógeno puede ser muy beneficiosa. Para corregir eficazmente la coagulopatía, pueden ser necesarios otros factores de la coagulación además de fibrinógeno durante la reposición.
Se recomienda la realización de una histerectomía si las medidas médicas y quirúrgicas resultan ineficaces.
Etiología de la Hemorragia Posparto
La HPP se produce por la regla de las 4T:
- Tono: Atonía uterina.
- Tejido: Retención de restos placentarios.
- Trauma: Desgarros en el canal del parto.
- Trombina: Alteraciones de la coagulación.
Otras causas incluyen el acretismo placentario (no desprendimiento de la placenta) y la inversión uterina.
Tratamiento de la Inversión Uterina
Para la inversión uterina, se pueden emplear 50 mcg de nitroglicerina, 0.25 mg de terbutalina IV, o gases inhalados, junto con reposición manual (sin extraer la placenta).
Monitorización Bioquímica
Se recomienda la monitorización de glucosa, ionograma, equilibrio ácido-base, urea, creatinina y sodio.
Inversion Uterina
tags: #escalones #hemorragia #obstetrica