La investigación en el campo del desarrollo embrionario ha sido históricamente limitada por diversos aspectos, tanto técnicos como legales y éticos. Sin embargo, el avance de tecnologías como la edición del genoma, y específicamente el sistema CRISPR, está abriendo nuevas y prometedoras vías para comprender los intrincados procesos moleculares que dan forma a un nuevo organismo desde sus etapas más tempranas.
Investigación con Embriones Humanos Mediante Edición Genómica
Investigadores del IDIBELL y Dexeus Mujer están utilizando la técnica CRISPR de edición del genoma para modificar el material hereditario de embriones humanos. El objetivo principal es estudiar el desarrollo embrionario temprano, un proceso que involucra una serie de eventos moleculares perfectamente orquestados que determinan la futura formación de tejidos, órganos y sistemas del cuerpo.
Los embriones humanos que se utilizan en esta investigación proceden de ciclos de fecundación in vitro llevados a cabo en el centro Dexeus Mujer. Estos embriones han sido cedidos voluntariamente por sus progenitores con la finalidad de ser empleados en investigación. Una vez modificados, su desarrollo será monitorizado en tiempo real para estimar la función de genes específicos con precisión.
CRISPR: Una Herramienta Revolucionaria para la Investigación Genética
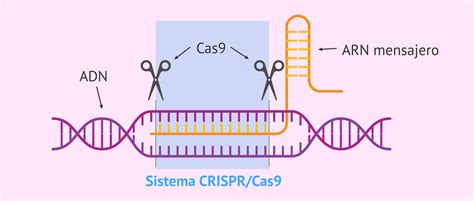
El sistema CRISPR de edición del genoma se considera una de las herramientas con mayor potencial para corregir enfermedades causadas por defectos en el ADN. Mediante CRISPR, es posible modificar el genoma de una célula de forma específica, ya sea eliminando, añadiendo un fragmento de ADN o corrigiendo directamente su secuencia.
La seguridad y eficacia de CRISPR en pacientes adultos con diversas enfermedades ya está siendo evaluada en múltiples ensayos clínicos. Sin embargo, más allá de su aplicación terapéutica, la tecnología CRISPR posee múltiples aplicaciones en el campo de la investigación. Una de sus utilidades más destacadas es el estudio de la función de los genes, ya que permite su inactivación de forma específica.
El Genoma Humano: ADN Codificante y No Codificante
Una parte fundamental de la investigación genómica se centra en comprender la compleja organización del genoma. Se estima que aproximadamente el 98% del genoma humano es ADN no codificante, es decir, secuencias que no contienen genes directamente. Sin embargo, una porción significativa de este ADN no codificante está ocupada por elementos reguladores.
Estos elementos reguladores funcionan como "interruptores" que controlan la expresión de los genes, encendiéndolos o apagándolos. Durante el desarrollo embrionario, el proceso mediante el cual una sola célula se transforma en un animal completo, la regulación de la expresión génica alcanza su máxima complejidad.
La Estructura Tridimensional del Genoma y su Regulación
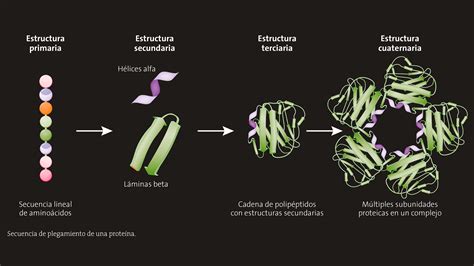
Aunque los elementos reguladores (interruptores) y los genes a los que controlan pueden encontrarse a largas distancias en la secuencia lineal del ADN, la investigación reciente ha demostrado que el genoma se pliega tridimensionalmente, similar a una madeja de lana. Este plegamiento facilita el contacto entre los interruptores y sus genes diana.
En mamíferos, la proteína CTCF ha sido identificada como clave para el plegamiento tridimensional del genoma. Estudios recientes han revelado que CTCF es esencial para la correcta regulación de los genes implicados en el desarrollo embrionario. CTCF se une al ADN y actúa como una barrera, delimitando zonas dentro de las cuales los interruptores pueden actuar. Esto crea una organización en "ovillos" consecutivos, separando regiones genómicas.
Cuando CTCF está ausente, estas barreras desaparecen, los "ovillos" se fusionan, debilitando el contacto de los interruptores con sus genes diana y permitiendo nuevos contactos con genes no deseados. La generación de mutantes de CTCF mediante CRISPR en modelos animales, como el pez cebra, ha proporcionado un modelo valioso para profundizar en la función de CTCF in vivo durante el desarrollo embrionario animal.
La Transición Materno-Cigótica: Un Hito en el Desarrollo Embrionario
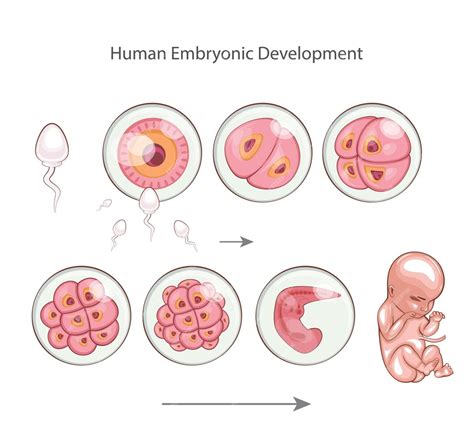
El desarrollo embrionario temprano se caracteriza por una transición fundamental conocida como la transición materno-cigótica (TMC). Este proceso marca el paso del control del desarrollo del embrión, que inicialmente depende de los recursos (ARN mensajeros y proteínas) acumulados por la madre en el ovocito, a la activación y expresión del propio genoma del embrión.
Eventos Clave de la Transición Materno-Cigótica
- Degradación de ARNm maternos: Durante las primeras divisiones embrionarias, los transcritos de origen materno se van degradando gradualmente. En ratones, esta degradación ocurre principalmente en el estadio de 2 células, mientras que en humanos ocurre en el estadio de 4 células y en ganado en el de 8 a 16 células.
- Activación del genoma cigótico (ZGA): Tras la degradación de la mayoría de los transcritos maternos, el genoma del embrión se activa, comenzando la transcripción de sus propios genes. Este evento es crucial para el desarrollo posterior.
- Cambios celulares y moleculares: La TMC implica cambios en la división celular (de asimétricas a simétricas), redistribución de orgánulos como las mitocondrias y el retículo endoplasmático, y procesos de metilación en los genomas materno y embrionario.
Genes y Complejos Implicados en la TMC
Varios genes y complejos proteicos desempeñan roles cruciales durante la TMC:
- Factor de transcripción Hinfp: Es el único factor de transcripción conocido para la expresión del gen de la histona H4, esencial para la estabilidad genómica y la viabilidad celular.
- Gen Brm: Su subunidad catalítica Brg1 es un factor de supervivencia celular esencial para la ZGA y está vinculado a la modificación de histonas.
- Complejo SCMC (Subcortical Maternal Complex): Este complejo, compuesto por múltiples proteínas maternas (Mater, Pillia, Floped, Tle6, Zbed3, Nlrp2, Padl6), actúa como modulador de procesos necesarios para la TMC, incluyendo el control de la posición del huso, la formación del retículo endoplasmático, la distribución de orgánulos, y el establecimiento del linaje celular. Se ha demostrado que sus componentes están conservados en mamíferos, incluyendo humanos.
El SCMC también parece jugar un papel importante en el establecimiento del destino celular, influyendo en la formación del trofoectodermo y la masa celular interna en embriones de ratón.
Desarrollo Embrionario Temprano y su Estudio
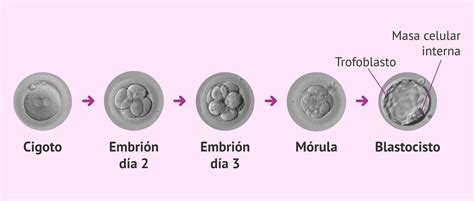
Desde el momento de la fecundación, las primeras divisiones embrionarias han sido responsabilidad del ovocito, ya que la síntesis de ADN y proteínas ocurre antes de la fecundación. La valoración del embrión en día 3 permite estimar su potencial para llegar a fase de blastocisto, evaluando parámetros morfocinéticos como el número de células (esperándose entre 6 y 8 células) y la presencia de fragmentos celulares.
La compactación temprana, que ocurre alrededor del tercer día, es un signo de activación embrionaria. Sin embargo, la calidad del ovocito es un factor crítico que limita la eficacia de las tecnologías de reproducción asistida (TRA) y el éxito del embarazo, debido a la influencia de los factores maternos acumulados en diversos procesos del desarrollo embrionario temprano.
Avances en el Diagnóstico Genético Preimplantacional (PGT)
En el campo de la medicina reproductiva, una de las preguntas más desafiantes es por qué algunos embriones genéticamente normales no logran implantarse o acaban en aborto espontáneo. A pesar del uso de tecnologías como el diagnóstico genético preimplantacional (PGT), el resultado reproductivo no siempre es el esperado.
El PGT tradicional se centra en detectar aneuploidías o mutaciones familiares conocidas. Sin embargo, la Secuenciación del Genoma Completo (WGS) permite analizar los ~20.000 genes del genoma humano. Se estima que el 50% de los embriones considerados genéticamente normales (euploides) no llegan a implantarse, y un 10% adicional acaba en aborto espontáneo. Esto indica una brecha significativa en la capacidad de predecir con precisión el éxito de la implantación y el desarrollo embrionario.
La WGS representa la próxima frontera del PGT, ofreciendo una alternativa más completa a enfoques invasivos como la biopsia de trofectodermo. Aunque la implementación de la WGS requiere profesionales capacitados en interpretación genética, asesoramiento genético reproductivo y bioética, tiene el potencial de convertirse en una prueba estándar para mejorar las probabilidades de éxito en la concepción.
El diagnóstico genético preimplantacional o DGP
Consideraciones Éticas en la Edición Genómica
La edición del genoma, especialmente cuando se aplica a embriones humanos, plantea importantes preocupaciones éticas. La mayoría de los cambios realizados con tecnologías como CRISPR-Cas9 se limitan a células somáticas, las cuales no se transmiten a las generaciones futuras.
Sin embargo, los cambios introducidos en las células germinales (óvulos y espermatozoides) o en las de un embrión podrían transmitirse a las generaciones venideras. Esto genera debates éticos sobre la posibilidad de utilizar esta tecnología para mejorar rasgos humanos normales, como la altura o la inteligencia, y sobre los límites y regulaciones que deben aplicarse.
tags: #desarrollo #embrionario #y #el #genoma