El cribado neonatal universal es una herramienta fundamental de salud pública con un gran impacto en la salud de los recién nacidos, orientada a la detección precoz de enfermedades, su diagnóstico y tratamiento temprano. Se ofrece a todos los recién nacidos, sean o no susceptibles de padecer alguna enfermedad, incluso si no presentan síntomas. Este programa de prevención busca identificar trastornos genéticos, hormonales y metabólicos poco frecuentes que, de no ser tratados a tiempo, pueden causar graves problemas de salud y discapacidades.
¿Qué es el Cribado Neonatal?
El cribado neonatal es un servicio público de salud que evalúa un grupo de trastornos que no se pueden detectar a simple vista en el momento del nacimiento. Su propósito es diagnosticar rápidamente a los bebés e iniciar el tratamiento lo antes posible, lo que previene discapacidades asociadas a la enfermedad y mejora significativamente el pronóstico y la calidad de vida de los afectados.
Orígenes y Evolución
Los inicios del cribado neonatal se remontan a la década de los años 60, con el desarrollo de una prueba bacteriológica capaz de detectar una elevación de los niveles de fenilalanina en una gota de sangre seca recogida en papel de filtro, conocida como el test de Guthrie. A lo largo del tiempo, el momento de realización y el tipo de análisis han ido variando. La incorporación de técnicas analíticas basadas en la espectrometría de masas en tándem (MS/MS) ha condicionado cambios significativos, permitiendo la detección simultánea de una gran cantidad de enfermedades metabólicas (más de 40) en una misma muestra, lo que se ha denominado cribado metabólico expandido.
Tipos de Pruebas de Cribado Neonatal
Las pruebas incluidas en el cribado neonatal varían entre diferentes regiones y países, evolucionando conforme avanzan la tecnología y mejoran los tratamientos. A pesar de las recomendaciones nacionales o internacionales, la decisión final sobre las pruebas que se incluyen en el cribado depende de cada jurisdicción.
Cribado por Prueba del Talón (Detección Metabólica y Hormonal)
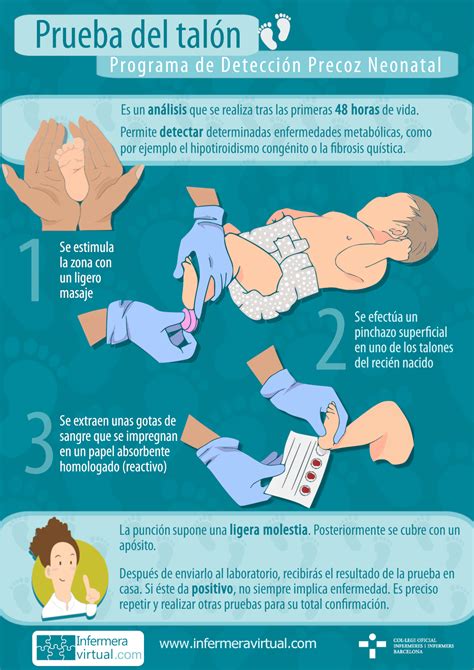
La prueba del talón es el procedimiento más conocido y consiste en tomar una pequeña muestra de sangre del talón del bebé. Se realiza una punción con una lanceta especial diseñada para minimizar el dolor, generalmente entre las 24 y 72 horas de vida del recién nacido, siempre antes del alta hospitalaria. Antes de la toma de muestra, los profesionales sanitarios informan a los padres o tutores sobre la prueba y recogen el consentimiento informado. En ocasiones, es necesario recoger una segunda muestra si la primera no fue suficiente, se recogió de forma incompleta o los resultados no fueron concluyentes, lo cual no implica necesariamente que el bebé esté enfermo.
Con esta simple prueba, los médicos pueden evaluar una serie de afecciones genéticas, hormonales y metabólicas poco frecuentes:
- Problemas metabólicos: Son trastornos que dificultan la transformación de los alimentos en energía. La mayoría ocurren cuando algunas enzimas están ausentes o no funcionan correctamente. Ejemplos incluyen:
- Fenilcetonuria (PKU): Enfermedad del metabolismo de la fenilalanina, con una prevalencia de 1/12.000-1/18.000 recién nacidos. El cribado se realiza midiendo fenilalanina (Phe) y tirosina (Tyr) en sangre.
- Deficiencia de acil-CoA deshidrogenasa de ácidos grasos de cadena media (MCADD) y deficiencia de 3-hidroxi acil-CoA deshidrogenasa de ácidos grasos de cadena larga (LCHADD): Trastornos de la beta oxidación mitocondrial con prevalencia variable entre 1/9.000 y 1/100.000 recién nacidos.
- Aciduria glutárica tipo I (AG-1): Enfermedad del metabolismo de los ácidos orgánicos por defecto de la enzima GCDH, que metaboliza la lisina (Lys) y el triptófano (Trp). Su prevalencia en España es de 1/85.000 recién nacidos.
- Deficiencia de biotinidasa (BTD): Error congénito del metabolismo con una prevalencia estimada de 1/61.000, que sin tratamiento puede causar convulsiones, problemas respiratorios, hipotonía, erupciones cutáneas, alopecia y retraso del desarrollo. El tratamiento primario consiste en suplementos de biotina oral de por vida.
- Tirosinemia tipo I: Enfermedad endocrino-metabólica grave que, de no diagnosticarse y tratarse precozmente, puede causar daños hepáticos, renales y neurológicos.
- Problemas hormonales: Ocurren cuando las glándulas fabrican una cantidad excesiva o insuficiente de hormonas. El principal ejemplo es el hipotiroidismo congénito (HC), cuya frecuencia de 1/3.500 recién nacidos vivos justifica su cribado. La detección precoz y el inicio del tratamiento dentro del primer mes de vida se asocian a un desarrollo intelectual normal. El cribado sistemático neonatal se basa en la determinación del nivel de TSH en sangre del talón.
- Problemas relacionados con la hemoglobina: La hemoglobina es la proteína de los glóbulos rojos encargada de transportar oxígeno. Un ejemplo es la anemia de células falciformes (AF).
En España, se recomienda el cribado neonatal en muestra de sangre impregnada en papel para al menos ocho entidades: hipotiroidismo congénito (HC), fenilcetonuria (PKU), deficiencia de acil-CoA deshidrogenasa de ácidos grasos de cadena media (MACDD), deficiencia de 3-hidroxi acil-CoA deshidrogenasa de ácidos grasos de cadena larga (LCHADD), aciduria glutárica tipo I (AG-1), deficiencia de biotinidasa (BTD), fibrosis quística (FQ) y anemia de células falciformes (AF). Recientemente, se ha ampliado para incluir la tirosinemia tipo I.
Cribado de Hipoacusia Congénita
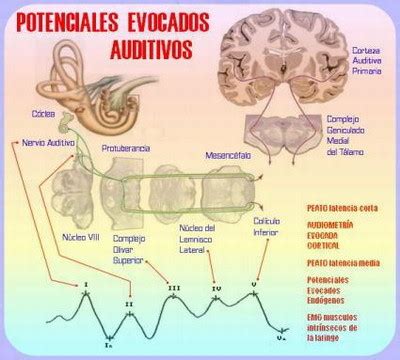
La pérdida de audición es uno de los defectos de nacimiento más frecuentes, afectando a aproximadamente 2-3 de cada 1.000 lactantes. El programa de cribado neonatal de hipoacusia busca detectar precozmente la pérdida auditiva, confirmar el diagnóstico, iniciar el tratamiento y realizar el seguimiento adecuado. La prueba de cribado se realiza mediante Potenciales Evocados Auditivos de Tronco Cerebral Automatizados (PEATC-A) en ambos oídos, preferiblemente antes del alta hospitalaria y siempre dentro del primer mes de vida.
Se presta especial atención a recién nacidos con factores de riesgo de hipoacusia, como antecedentes familiares, infecciones maternas durante el embarazo (toxoplasmosis, rubéola, citomegalovirus), hiperbilirrubinemia grave, encefalopatías hipóxico-isquémicas, o síndromes asociados con hipoacusia.
Cribado de Cardiopatías Congénitas Críticas (CCC)
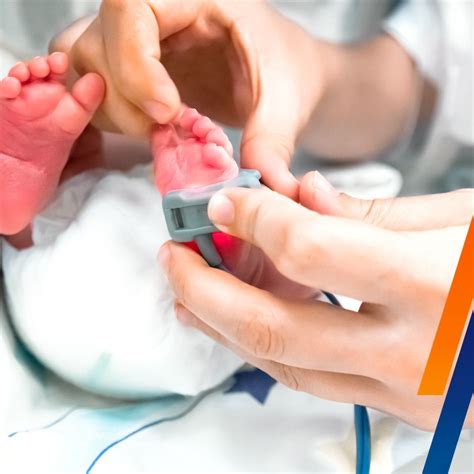
Las cardiopatías congénitas son el grupo más prevalente de anomalías congénitas en neonatos y la causa más frecuente de mortalidad entre todas las malformaciones congénitas. Las cardiopatías congénitas críticas son la forma más grave y asocian un aumento significativo de la mortalidad y morbilidad si no se identifican y tratan precozmente. La prueba de cribado utilizada es la pulsioximetría, que permite medir de forma no invasiva la saturación de oxígeno en la hemoglobina.
La detección se realiza cuando los lactantes tienen 24 horas o más de vida y se considera positiva si:
- Alguna medición de saturación de oxígeno es inferior al 90%.
- Las mediciones de saturación de oxígeno, tanto en la mano como en el pie derechos, son inferiores al 95% en tres mediciones separadas tomadas con una hora de diferencia.
- Existe una diferencia absoluta superior al 3% entre la saturación de oxígeno en la mano derecha (preductal) y el pie derecho (posductal) en tres mediciones separadas tomadas con una hora de diferencia.
Cualquier niño con un examen de detección positivo debe someterse a pruebas adicionales, como radiografía de tórax, electrocardiograma y ecocardiograma.
Otras Pruebas de Cribado
Además de las pruebas mencionadas, se pueden incluir otras, dependiendo de las normativas regionales y las necesidades clínicas:
- Cribado de ictericia: Debe buscarse durante toda la hospitalización y antes del alta, evaluando el riesgo de hiperbilirrubinemia mediante criterios de riesgo o determinación de bilirrubina.
- Cribado de VIH: Indicado para hijos de madres seropositivas o con comportamientos de alto riesgo.
- Estudios toxicológicos: Indicados ante antecedentes maternos de consumo de drogas, desprendimiento prematuro de placenta de causa desconocida, trabajo de parto prematuro inexplicable, atención prenatal deficiente o evidencia de abstinencia de drogas en el recién nacido.
- Cribado a partir de muestras de orina: Es posible realizar estudios de cribado a partir de muestras de orina en papel de filtro, utilizando técnicas analíticas basadas en MS/MS o cromatografía de gases y espectrometría de masas (GC/MS) para confirmación diagnóstica, complementar la información de la muestra de sangre o ampliar a nuevos diagnósticos.
El Proceso del Cribado Neonatal: Etapas y Seguimiento
El cribado neonatal es una estrategia coordinada que implica a maternidades, centros de salud, laboratorios de cribado neonatal y equipos clínicos especializados. Un programa robusto cuenta con protocolos normalizados de trabajo, control interno y auditorías externas para garantizar la fiabilidad de los resultados. El programa se desarrolla típicamente en las siguientes etapas:
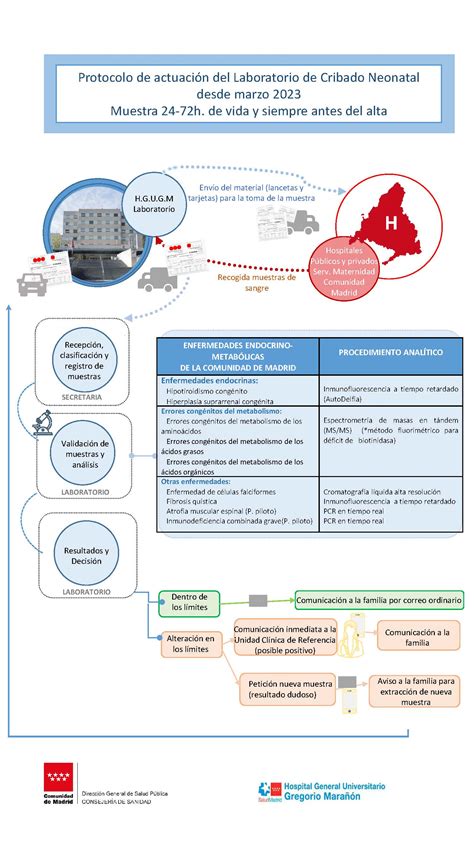
- Información a las familias y toma de muestra: Los profesionales sanitarios informan a los padres o tutores sobre el programa de cribado y se realiza la toma de muestra de sangre capilar del talón en la tarjeta de cribado, preferiblemente entre las 24 y 72 horas de vida y siempre antes del alta hospitalaria.
- Transporte de las muestras: Las tarjetas de toma de muestra se trasladan diariamente desde las maternidades y los centros de salud al Laboratorio de Cribado Neonatal, siguiendo un protocolo que garantiza su trazabilidad y conservación adecuada.
- Recepción, análisis y emisión de resultados: El Laboratorio de Cribado Neonatal recibe las muestras, realiza el análisis y emite el resultado. Los análisis de sangre suelen estar listos cuando el bebé tiene entre 5 y 7 días de vida. Los resultados de las pruebas de audición y cardiopatías congénitas se obtienen al concluir las pruebas.
- Derivación urgente a Unidad Clínica de Referencia: Si el resultado está fuera de los límites normales, se activa un circuito de derivación. La Unidad Clínica de Referencia establece comunicación directa por vía telefónica con la familia para concertar una cita.
- Confirmación diagnóstica, tratamiento y seguimiento: Las Unidades Clínicas de Referencia realizan el diagnóstico confirmatorio, inician el tratamiento y llevan a cabo el seguimiento de los casos. Cuando se requiere tratamiento, es importante iniciarlo lo antes posible.
- Planificación, coordinación y evaluación: Esta etapa transversal implica funciones de planificación del programa, coordinación de los circuitos y profesionales implicados, y evaluación del funcionamiento y los resultados por parte de Salud Pública.
¿ Como se realiza el Tamiz metabólico Neonatal ? TOMA DE MUESTRA
Resultados y su Interpretación
Generalmente, a los padres no se les informa sobre los resultados si todas las pruebas salen bien. Solo se contacta con ellos si alguna prueba ha dado un resultado alterado o "positivo". Es crucial entender que un resultado alterado o positivo en una prueba de cribado neonatal no implica necesariamente una enfermedad. Los médicos solicitarán análisis complementarios para confirmar o descartar el diagnóstico. Hay dos tipos principales de resultados alterados:
- Resultados altamente sugestivos de una alteración metabólica grave: En estos casos, se contacta a la familia lo antes posible mediante llamada telefónica por un profesional con experiencia en enfermedades metabólicas, quien explicará el significado del resultado y los pasos a seguir.
- Resultados fuera del rango normal, pero no tan alterados como para indicar una enfermedad: Estos casos sospechosos requieren una repetición del test para distinguir entre un verdadero positivo y una anomalía transitoria. Se solicita una nueva muestra, y se aconseja a los padres que acudan a su pediatra para una explicación adicional.
La parte de la muestra que no se utiliza para el análisis se guarda durante cinco años en el Laboratorio de Cribado Neonatal en condiciones seguras. Su conservación garantiza la calidad del proceso y permite repetir la prueba si fuera necesario.
Criterios para la Inclusión de Enfermedades en el Cribado
Clásicamente, se definieron criterios para que un trastorno se incluya en el cribado masivo:
- Que la gravedad de la enfermedad curse con morbilidad (como retraso mental) o mortalidad si no se diagnostica en el período neonatal.
- Que exista un tratamiento eficaz.
- Que la frecuencia de la enfermedad sea relativamente elevada (al menos, 1 de cada 10.000-15.000 recién nacidos).
- Que exista un método analítico de cribado rápido, fiable y de bajo coste.
Aunque estos criterios permanecen vigentes, la incorporación de la tecnología de MS/MS ha modificado la perspectiva, permitiendo considerar eficiente la inclusión de enfermedades con muy baja prevalencia (inferior a 1:50.000 recién nacidos) si pueden ser detectadas con la misma prueba. En 2005, la Academia Americana de Pediatría (AAP) y la Asociación Americana de Genética Médica (ACMG) emitieron recomendaciones para Estados Unidos sobre los trastornos que deberían cribarse.
Consideraciones Especiales en la Toma de Muestras
La estrategia de obtención de las muestras biológicas puede diferir, pero como norma general, se recomienda una extracción única de sangre capilar a partir de las 48 horas de vida del recién nacido, tras una ingesta de 24 horas de alimento. La extracción debe ser realizada exclusivamente por personal sanitario, siendo la punción del talón el procedimiento habitual.
Para minimizar el dolor durante la punción, se recomienda administrar una toma de lactancia materna, soluciones de glucosa o chupetes impregnados en sacarosa. La punción debe realizarse con una lanceta estéril en la porción medial o lateral de la superficie plantar del talón, evitando daños osteo-articulares. Es fundamental masajear el pie previamente para aumentar el flujo sanguíneo y desinfectar con alcohol de 70º, evitando derivados yodados. Después de la punción, se debe limpiar la primera gota de sangre y permitir que una nueva gota grande caiga sobre el papel absorbente, llenando el círculo por completo con una sola aplicación.
Para una muestra óptima, las manchas de sangre deben contener al menos 75 μl (aproximadamente 13 mm de diámetro) y dejarse secar en una superficie horizontal no absorbente, seca y limpia, durante al menos una hora a temperatura ambiente, evitando la luz solar directa. Las muestras deben enviarse al laboratorio lo antes posible, idealmente dentro de las 24-48 horas siguientes a la extracción, evitando el contacto entre muestras y cualquier tipo de contaminación.
Situaciones Clínicas Específicas:
- Recién nacidos con patología grave al nacimiento: Se recomienda tomar una muestra en el momento del ingreso (si es posible antes de recibir tratamiento antibiótico o alimentación parenteral) y repetirla a las 48-72 horas de vida.
- Transfusiones previas: Se debe tomar una muestra a las 48-72 horas de la transfusión y repetirla a los 120 días.
- Alimentación parenteral: Se debe realizar una toma de muestra a las 48-72 horas después de haber iniciado la alimentación enteral, sin importar la edad del niño en ese momento.
El Cribado Neonatal en España: Avances y Desafíos
Los programas de cribado neonatal en España están reconocidos como programas esenciales de prevención en Salud Pública. Recientemente, el país ha ampliado el cribado neonatal con la incorporación de la tirosinemia tipo I y las cardiopatías congénitas críticas, reforzando la equidad en el acceso al diagnóstico precoz de enfermedades raras en todo el territorio nacional. Esta ampliación, fruto del trabajo conjunto entre organismos de salud y asociaciones de pacientes, representa un paso clave para reducir la "odisea diagnóstica" y mejorar la calidad de vida de las personas afectadas por enfermedades raras.
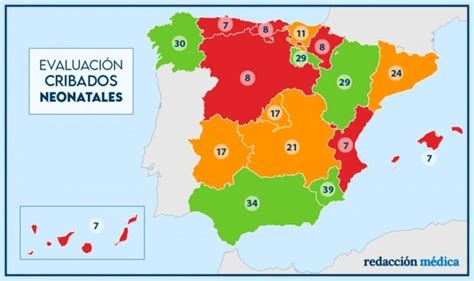
Sin embargo, la inequidad en el acceso al cribado neonatal sigue siendo un problema grave en España. El número de patologías cribadas varía entre comunidades autónomas, lo que significa que el lugar de nacimiento puede condicionar las oportunidades de diagnóstico precoz. Para abordar esta situación, se han impulsado iniciativas legislativas que buscan garantizar una equidad total, homogeneizar los paneles de cribado, agilizar la incorporación de nuevas patologías basadas en la evidencia científica y asegurar la dotación de recursos necesarios. El objetivo es que el cribado neonatal sea un derecho universal y un pilar fundamental de la salud pública, previniendo la mortalidad prematura y la discapacidad.