En la actualidad, un número creciente de mujeres se enfrenta a la necesidad de recurrir a tratamientos de fertilidad, experimentando a menudo desesperación ante la persistencia de intentos fallidos. Diversos estudios han puesto de manifiesto la significativa influencia que el estrés puede ejercer sobre la fertilidad femenina.
Es ampliamente conocido que las situaciones de estrés crónico generan una multitud de problemas de salud. Investigaciones recientes, llevadas a cabo por la Escuela de Salud Pública y Ciencias de la Información de la Universidad de Louisville en Kentucky y la Universidad de Emory en Atlanta, subrayan que las mujeres que experimentan mayores niveles de estrés durante la ovulación podrían tener hasta un 45% menos de probabilidades de concebir.
Estrés y Fertilidad: El Impacto del Cortisol
Una investigación que analizó a 400 mujeres de aproximadamente 40 años de edad registró sus niveles diarios de estrés en una escala del 1 al 4. También se monitorizaron sus ciclos menstruales, el uso previo de métodos anticonceptivos, la frecuencia de relaciones sexuales con su pareja, y el consumo de alcohol, cafeína y tabaco. Los resultados revelaron que las mujeres con altos niveles de cortisol, la denominada "hormona del estrés", presentaban una interrupción de la ovulación o ciclos menstruales muy irregulares, lo que dificultaba la concepción. Este perfil corresponde a mujeres con estilos de vida acelerados y trabajos altamente estresantes. Adicionalmente, el elevado estrés puede disminuir el deseo de mantener relaciones sexuales.
Las conclusiones del estudio indican que el estrés durante la ventana ovulatoria reduce la probabilidad de embarazo en un 40%, y el estrés en general hasta en un 45%. La forma en que el estrés afecta a cada persona y las reacciones que provoca dependen de factores individuales.
El estrés puede afectar el funcionamiento del hipotálamo, una glándula cerebral que regula el apetito, las emociones y las hormonas que envían la señal a los ovarios para liberar óvulos. Si una mujer está muy estresada, podría ovular más tarde en su ciclo reproductivo o no ovular en absoluto. El aumento de cortisol también puede disminuir la libido, reduciendo así el interés por las relaciones sexuales y, consecuentemente, la probabilidad de embarazo.
Por otro lado, para que la implantación del embrión sea exitosa, se requieren niveles adecuados de estrógenos y progesterona. Un déficit de estas hormonas puede impedir que el embarazo continúe, incluso si el óvulo ha sido fecundado. Si una mujer intenta concebir y está estresada, su flujo cervical puede enviar una señal de advertencia. En lugar de un aumento gradual del flujo a medida que se acerca la ovulación, pueden alternarse días de flujo abundante con días secos, como si el cuerpo intentara ovular pero el estrés lo retrasara continuamente.
Es importante destacar que el estrés no solo afecta a las mujeres. El estrés en el hombre también puede reducir la cantidad y calidad de los espermatozoides.
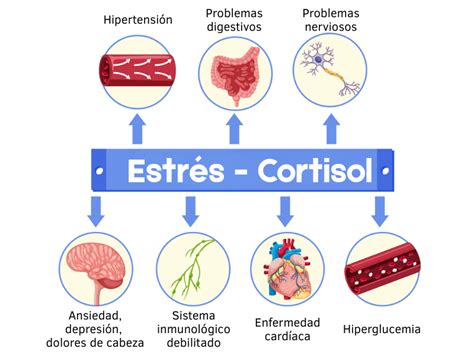
El Papel del Cortisol en la Fertilidad
El cortisol, conocido comúnmente como la "hormona del estrés", es una hormona esteroidea producida por las glándulas suprarrenales. Su liberación se regula a través del eje hipotálamo-pituitaria-suprarrenal (HPA) y está diseñada para preparar al cuerpo ante situaciones de estrés extremo. Sin embargo, el problema surge cuando el cuerpo y la mente no logran distinguir entre una amenaza real y una imaginaria, lo que puede hacer que el cortisol se vuelva perjudicial si sus niveles se mantienen elevados de forma crónica.
Cuando los niveles de cortisol permanecen altos durante periodos prolongados, el cuerpo puede entrar en un estado de "intoxicación por cortisol". Este estado crónico puede ser desencadenado por factores como el estrés constante, la falta de sueño, una dieta inadecuada o un entrenamiento excesivo.
Unos niveles excesivamente elevados de cortisol pueden tener un impacto directo en el ciclo menstrual al interferir con la producción de gonadotropinas, hormonas cruciales para la función ovárica. Además, el cortisol elevado puede disminuir los niveles de estrógenos y progesterona, hormonas esenciales para mantener un embarazo saludable y preparar el revestimiento uterino para la implantación embrionaria.
El cortisol y la progesterona comparten una vía metabólica común, derivada de la pregnenolona. Cuando el estrés demanda una alta producción de cortisol, el cuerpo desvía la pregnenolona disponible para su síntesis, dejando escasos recursos para la producción de progesterona. El estrés oxidativo, generado por un estilo de vida frenético, puede dañar las mitocondrias de los ovocitos. Asimismo, el útero no es inmune al estrés; una elevada carga alostática puede alterar el sistema inmune, incrementando las citoquinas proinflamatorias en el endometrio. En los hombres, el estrés laboral y vital eleva los radicales libres (ROS), causando daños en el ADN de los espermatozoides. El cortisol actúa como antagonista de la testosterona.
La fertilidad femenina depende de un delicado equilibrio hormonal. Demasiado cortisol puede interferir con la hormona liberadora de gonadotropina (GnRH), que desencadena la ovulación. El estrés crónico no solo afecta la ovulación, sino también la implantación embrionaria, un proceso vital para lograr un embarazo.
El cortisol no se sintetiza de novo en el ovario, sino que se transporta desde las glándulas suprarrenales. La mayor parte circula unida a proteínas plasmáticas, y solo una pequeña porción es libre y biológicamente activa. Los niveles de cortisol libre en el fluido folicular son más elevados que en plasma.
Existe la posibilidad de que el metabolismo del cortisol en el fluido folicular esté relacionado con la probabilidad de concebir en ciclos de fecundación asistida. Una tasa elevada de cortisol/cortisona intrafolicular (indicativa de baja actividad ovárica de 11b-HSD) se ha asociado con una mayor probabilidad de éxito en tratamientos de reproducción asistida en algunos estudios. Sin embargo, otros no han encontrado una relación clara.
En la especie porcina, las enzimas 11b-HSD actúan en el oocito y en las células del cúmulo inactivando los glucocorticoides, un mecanismo que podría ser importante para limitar efectos negativos durante la maduración del oocito. Estudios recientes sugieren que la inactivación del cortisol por parte de las 11b-HSDs en las células de la granulosa en el cerdo se incrementa con el desarrollo folicular y que esta inactivación está reducida en quistes foliculares ováricos, implicando al cortisol en el crecimiento folicular y el desarrollo de quistes.
Estrategias para Reducir el Estrés y Mejorar la Fertilidad
Afortunadamente, si bien el estrés no se puede eliminar por completo de la vida diaria, sí es posible tomar medidas para mitigar sus efectos negativos sobre la fertilidad. Las mujeres que optan por tratamientos para reducir su nivel de estrés han demostrado poder neutralizar el impacto negativo y aumentar sus posibilidades de embarazo.
Las técnicas de relajación son fundamentales. La meditación, el yoga y la respiración profunda son prácticas eficaces para disminuir los niveles de cortisol y promover un estado de relajación. El ejercicio regular, realizado de forma moderada (como caminar, yoga o natación), ayuda a reducir el estrés y mejora la circulación sanguínea, lo cual beneficia la salud reproductiva. El ejercicio físico de alta intensidad, sin embargo, puede aumentar los niveles de cortisol al ser percibido por el cuerpo como una amenaza.
Una dieta equilibrada, rica en antioxidantes, vitaminas y minerales, contribuye a reducir el estrés oxidativo y favorece la salud hormonal. Se recomienda priorizar ácidos grasos omega-3 (DHA/EPA), proteínas magras, carbohidratos complejos, frutas, verduras y granos enteros.
El sueño tiene un impacto directo en los niveles hormonales y, por ende, en la fertilidad. Asegurar un descanso adecuado es crucial. La melatonina, además de regular el sueño, es un potente antioxidante que protege al ovocito del daño oxidativo.
El apoyo social y profesional es igualmente importante. Hablar con un terapeuta, la pareja o amigos cercanos puede ser de gran ayuda para gestionar el estrés emocional. No se debe dudar en pedir ayuda si uno se siente abrumado.
Incrementar los niveles de oxitocina, conocida como la "hormona de la felicidad", puede ayudar a reducir el cortisol. Disfrutar de la sexualidad es clave para reducir el estrés, ya que durante las relaciones sexuales se liberan altos niveles de oxitocina, especialmente durante el orgasmo. Aunque el estrés crónico puede disminuir la libido, existen soluciones para revitalizar el deseo sexual femenino.
La práctica de Mindfulness (atención plena) aplicada a la "betaespera" (el periodo entre la transferencia embrionaria y la prueba de embarazo) ha mostrado mejores tasas de embarazo en estudios realizados en clínicas de fertilidad.
Es importante recordar que el estrés no solo reside en la mente, sino que tiene manifestaciones físicas y celulares, afectando a la tiroides y al útero. Abordar el factor emocional es una parte esencial del tratamiento de fertilidad.
Meditación 5 MINUTOS para Reducir ESTRES y Calmar la Mente. Aumenta tu BIENESTAR y tu CREATIVIDAD.
Impacto del Estrés en Tratamientos de Reproducción Asistida
El éxito de los tratamientos de reproducción asistida (TRA), como la fecundación in vitro (FIV) o la inyección intracitoplasmática de espermatozoides (ICSI), puede verse afectado por el estrés asociado a estos procedimientos. La ansiedad generada por estos métodos puede influir en los resultados.
Se ha observado que los niveles de adrenalina en el momento de la recuperación de ovocitos, así como las concentraciones de adrenalina y noradrenalina durante la transferencia de embriones, fueron menores en mujeres que lograron un ciclo de FIV/ICSI exitoso en comparación con aquellas que no lo consiguieron.
La vulnerabilidad al estrés se ha asociado con la FIV y la transferencia de embriones. Las mujeres que experimentan una mayor frecuencia cardíaca y presión arterial en respuesta al estrés durante estos tratamientos pueden tener un menor número de ovocitos fecundables.
Incluso en ciclos naturales, el "distrés" psicológico puede considerarse un factor de riesgo para la concepción en mujeres con ciclos menstruales prolongados.
La esteroidogénesis ovárica puede verse afectada por los glucocorticoides, cuyo efecto podría ser mediado por la alteración de las enzimas involucradas en su biosíntesis. Estudios in vitro han demostrado que la dexametasona puede afectar la esteroidogénesis inhibiendo la secreción de LH, y que el cortisol inhibe la síntesis de pregnenolona estimulada por la LH.
El papel del cortisol en el fluido folicular aún no está completamente definido. Se ha observado un incremento de los niveles de cortisol total y libre en el folículo durante el pico de LH. Algunos estudios sugieren que el cortisol podría tener funciones en el desarrollo folicular y la maduración del ovocito, o estar implicado en la respuesta antiinflamatoria post-ovulación.
En mujeres sometidas a estimulación ovárica con hormonas, se encontraron niveles de cortisol más bajos en el fluido folicular de folículos con ovocitos inmaduros en comparación con aquellos que contenían ovocitos maduros. Asimismo, la concentración de cortisol fue significativamente superior en fluidos foliculares de folículos con ovocitos maduros que no se fecundaron, en comparación con ovocitos maduros que sí fueron fecundados y se dividieron.
Existen diferencias entre especies en cuanto al efecto directo de los glucocorticoides en la maduración del ovocito. Mientras que en peces el cortisol parece estimular la maduración del ovocito, en mamíferos los estudios son contradictorios. Investigaciones in vitro en ovocitos de cerdo han mostrado que la maduración se ve inhibida por la exposición a dexametasona o cortisol. Sin embargo, la capacidad de los ovocitos madurados in vitro para ser fecundados no se vio afectada por la exposición previa a dexametasona.
El posible mecanismo de acción de los glucocorticoides sobre el ovocito aún se desconoce. El efecto inhibitorio observado se ha atribuido parcialmente a la reducida cantidad del complejo p34cdc2-ciclina B1 (MPF), un factor clave en la regulación del ciclo celular del ovocito.
Un estudio reciente en ratones evaluó el efecto de la dexametasona a nivel folicular. La dexametasona a concentraciones de hasta 40 μg/ml no afectó la foliculogénesis ni la oogénesis. Sin embargo, a 80 μg/ml, impidió la diferenciación folicular y la maduración del ovocito. La esteroidogénesis se vio afectada a partir de 5 μg/ml, y el desarrollo embrionario temprano a partir de 10 μg/ml.
Estos estudios sugieren que el efecto negativo potencial de los glucocorticoides sobre la oogénesis se observa a dosis relativamente elevadas y fuera del rango fisiológico in vitro, siendo probable que sea un efecto más farmacológico que fisiológico. No obstante, es necesario evaluar el efecto directo in vivo. En casos de perturbación del eje hipotálamo-hipófisis-adrenal con producción elevada de glucocorticoides, pueden producirse disrupciones en el ciclo reproductivo y la función ovárica, alterando el ambiente folicular.
En los últimos años, ha aumentado la preocupación por el bienestar animal y los efectos del manejo en animales domésticos y silvestres en cautividad. El estrés de manejo y la miopatía de captura son consecuencias frecuentes en animales salvajes. Dado que las situaciones estresantes pueden alterar el funcionamiento del eje hipotálamo-hipófisis-ovario, la reproducción puede verse afectada.
La reproducción natural de animales salvajes en cautividad es limitada, y el estrés se considera uno de los factores que contribuyen a esta reducida reproducción. Las tecnologías reproductivas tienen un gran potencial en especies amenazadas, pero su éxito es limitado por diversas causas, incluyendo el desconocimiento de la fisiología reproductiva y la deficiente calidad del material obtenido.
El estrés inducido durante el manejo asociado a los TRA en muflones podría contribuir a la reducida respuesta ovárica tras la superovulación. Asimismo, la alta incidencia de regresión lútea temprana en hembras de muflón podría estar parcialmente asociada al estrés repetitivo por inmovilización.
El estrés de manejo se ha descrito como un factor limitante en la aplicación de biotecnologías reproductivas en bisonte americano. En estudios con gacelas Mohor, una hembra tuvo que ser retirada del experimento debido al estrés de manejo durante las capturas repetidas para la administración de FSH, y la respuesta general al tratamiento de superovulación fue reducida.
El hecho de que el estrés pueda tener efectos perjudiciales en la reproducción subraya la importancia de evitarlo o minimizarlo, tanto para facilitar la reproducción natural como para aumentar las posibilidades de éxito en las biotecnologías reproductivas. La administración de tranquilizantes durante los procedimientos podría ser útil para reducir el estrés de manejo, captura y contención en estas especies.
Se ha descrito que el estrés de manejo durante los protocolos de superovulación en cabra montés puede llevar a un fallo completo en la tasa de fecundación. El tratamiento con tranquilizantes de acción prolongada permitió la superovulación y la obtención de embriones en estos animales.
En resumen: Si sientes que el estrés está bloqueando tu camino hacia la concepción, considera comenzar por lo básico: regula tu sueño, nutre tu tiroides y busca apoyo profesional. Abordar el factor emocional es una parte clínica esencial de tu tratamiento de fertilidad.
tags: #cortisol #metodos #de #fertilidad