La clonación por transferencia nuclear es una técnica avanzada que implica la transferencia de una célula diploide donante a un ovocito previamente enucleado. Posteriormente, este complejo ovocito-célula se activa artificialmente para iniciar el desarrollo embrionario, resultando en un embrión cuyo genoma nuclear es genéticamente idéntico al del animal donante. Este método, conocido como transferencia nuclear de células somáticas (SCNT), permite la producción de clones genéticamente idénticos.
Generalmente, el embrión clonado se cultiva en el laboratorio hasta la etapa de blastocisto. Una vez alcanzada esta fase, puede ser criopreservado para su uso futuro o transferido a una hembra sustituta para su gestación, lo que culmina en el nacimiento de una descendencia genéticamente idéntica al donante original. Es importante destacar que, si bien el genoma nuclear del clon es idéntico al del donante, otros factores como el ADN mitocondrial y las modificaciones epigenéticas pueden influir significativamente en el fenotipo final del individuo clonado.
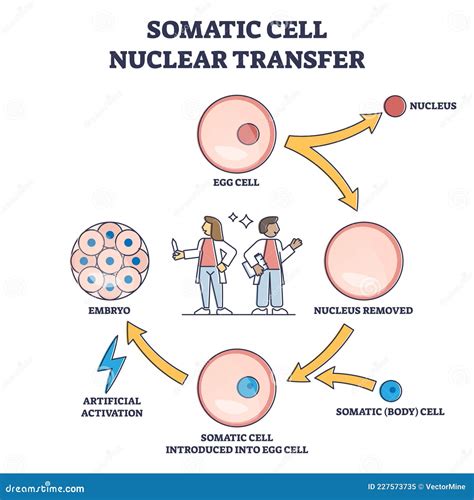
Aplicaciones de la Clonación en Animales Domésticos
La clonación de animales domésticos encuentra su aplicación más frecuente en especies como caballos, vacas, perros y camellos. En el ámbito de la práctica veterinaria, esta tecnología se emplea principalmente para:
- Reproducir animales reproductores de élite.
- Realizar edición genética en animales.
- Preservar la genética de individuos de alto rendimiento, valiosos o de compañía.
- Contribuir a la conservación de razas raras o en peligro de extinción.
Técnicas de Clonación y Selección de Células Donantes
La selección de la célula donante ha sido un área de investigación fundamental en el campo de la clonación. Las células derivadas de embriones en etapas tempranas, hasta la fase de mórula, han demostrado ser muy eficientes como células donantes. La clonación utilizando células embrionarias se llevó a cabo con éxito durante más de una década antes del hito histórico del primer mamífero producido mediante transferencia nuclear de células somáticas adultas: la oveja Dolly, clonada por el Instituto Roslin en Escocia en 1996.
A diferencia de la clonación a partir de células madre embrionarias, la SCNT, que emplea células somáticas diferenciadas como donantes nucleares, ofrece la ventaja de duplicar genéticamente animales adultos cuya calidad ya ha sido probada. Entre las células somáticas, el tejido conectivo subcutáneo es la fuente más comúnmente utilizada para la clonación de animales adultos. Este tejido se disgrega mecánicamente y se cultiva in vitro. Durante este proceso, los fibroblastos proliferan y se cosechan para su paso a nuevas placas de cultivo, promoviendo su crecimiento. Este procedimiento se repite hasta obtener millones de células, que luego se criopreservan para futuras aplicaciones de clonación.
Estudios sugieren que el uso de células madre podría mejorar la eficiencia de la clonación animal, aunque este punto sigue siendo objeto de debate. No obstante, empresas de clonación comercial están adoptando cada vez más células madre derivadas de la médula ósea para la clonación de caballos.
Requisitos y Proceso de Transferencia Nuclear
Para que la transferencia nuclear sea exitosa, se requieren ovocitos maduros de la misma especie o de subespecies estrechamente relacionadas. Aunque el valor genético de los ovocitos no es crítico, su composición mitocondrial puede influir en el resultado, dado que el clon resultante hereda las mitocondrias del ovocito receptor. Típicamente, los ovocitos se obtienen de material de matadero o, en algunas especies, se recolectan de animales vivos mediante la técnica de ovum pickup (OPU) y se maduran posteriormente in vitro. En ciertas especies, como los perros, los ovocitos maduros deben obtenerse de folículos preovulatorios o directamente del oviducto después de la ovulación.
La transferencia nuclear se realiza bajo microscopio utilizando herramientas de micromanipulación, siguiendo estos pasos:
- Enucleación del ovocito: Se eliminan los cromosomas (ADN genómico) del ovocito, generando un ovocito enucleado o ooplasto.
- Sincronización de la célula somática: La célula somática seleccionada para la clonación debe estar sincronizada con una fase temprana del ciclo celular, preferiblemente antes de la síntesis de ADN (fase G0-G1).
- Fusión celular: La célula somática se fusiona con el ooplasto mediante un pulso eléctrico que induce la fusión de membranas, o por inyección directa.
- Activación del ovocito: El ovocito recombinado, que ahora contiene el núcleo de la célula donante, se activa artificialmente para simular la señal de fertilización, iniciando así el desarrollo embrionario.
Estos pasos también pueden realizarse con ovocitos a los que se les ha retirado la zona pelúcida tras la maduración in vitro. Esta técnica, conocida como clonación «sin zonas», simplifica algunos de los procedimientos, pero requiere un sistema de cultivo especial para mantener las células embrionarias agrupadas durante la división celular.
La tecnología de transferencia nuclear se ha aplicado con éxito en gatos, perros y la mayoría de las especies de mamíferos domésticos de gran tamaño. Tras la activación de los ovocitos, el embrión en desarrollo puede ser transferido quirúrgicamente al oviducto de una hembra receptora (práctica común en especies como los perros), o cultivarse in vitro hasta alcanzar una etapa adecuada para su criopreservación o transferencia transcervical (no quirúrgica) al útero (práctica estándar en grandes mamíferos domésticos).
Salud y Fenotipo en Individuos Clonados
La salud y el fenotipo de los individuos clonados se ven influenciados por diversos factores, incluyendo los efectos epigenéticos, el ADN mitocondrial, el entorno uterino y posnatal, las mutaciones y la variación individual.
Efectos Epigenéticos
Tras la transferencia nuclear, el ooplasto debe reprogramar el ADN de la célula somática para que funcione de manera similar al de un cigoto. Esta reprogramación está predominantemente regulada por mecanismos epigenéticos, como la metilación del ADN y la modificación de histonas. Estos procesos controlan la transcripción génica sin alterar la secuencia de ADN, un fenómeno conocido como regulación epigenética. La capacidad del ovocito para reprogramar con precisión el ADN de la célula donante durante la clonación es crucial. El establecimiento y mantenimiento adecuados de la marca epigenética en las distintas etapas del desarrollo embrionario son esenciales para un desarrollo fetal exitoso. Se cree que los errores en la reprogramación epigenética son determinantes en el éxito o fracaso de la clonación.
Pequeñas imprecisiones en la reprogramación pueden no afectar gravemente la salud del clon, pero pueden resultar en diferencias fenotípicas respecto al donante. Un ejemplo de variación epigenética es el primer gato clonado, CC. Aunque su donante genético era un gato calicó, CC solo presentaba color marrón en su pelaje. En los gatos calicó, el color del pelaje está determinado por la inactivación del cromosoma X, un proceso en el que uno de los dos cromosomas X de las células femeninas se inactiva aleatoriamente. En CC, la inactivación del cromosoma X no fue aleatoria, probablemente debido a una reprogramación epigenética incompleta, lo que llevó a la activación exclusiva del gen del color marrón.
La placenta es uno de los tejidos más susceptibles a la reprogramación epigenética anormal después de la SCNT. Muchas muertes de embriones clonados se han atribuido a una función placentaria anormal, relacionada con una regulación epigenética inadecuada durante el desarrollo temprano. Por lo tanto, las estrategias dirigidas a mejorar la regulación epigenética durante la clonación podrían aumentar significativamente la eficiencia general del procedimiento. Sin embargo, muchos aspectos del proceso de reprogramación epigenética siguen siendo complejos y no se comprenden completamente.
Las diferencias epigenéticas también pueden influir en el fenotipo del animal clonado después del nacimiento. Por ejemplo, cambios en la expresión de genes relacionados con el crecimiento pueden hacer que algunos animales clonados crezcan más que otros, a pesar de compartir el mismo ADN. No obstante, la investigación en múltiples especies ha demostrado que la mayoría de las anomalías epigenéticas observadas en animales clonados no se transmiten a su descendencia. Esto se debe a que, durante la formación de espermatozoides y óvulos, la mayoría de las marcas epigenéticas se borran y restablecen, asegurando que la próxima generación comience con un "borrón y cuenta nueva". Si bien algunas marcas epigenéticas pueden escapar a esta reprogramación y transmitirse, la mayoría se restablece, lo que hace de la clonación una herramienta atractiva para la cría, ya que el riesgo de transmitir defectos epigenéticos a la descendencia es generalmente bajo.
ADN Mitocondrial
El embrión clonado hereda el ADN nuclear de la célula donante, pero el ADN mitocondrial proviene del ooplasto. Aunque puede persistir una pequeña cantidad de mitocondrias de la célula donante, generalmente son escasas en comparación con las mitocondrias del ovocito receptor. El papel del ADN mitocondrial en la determinación de rasgos como la resistencia y la eficiencia metabólica aún no está claro; sin embargo, es un área de potencial interés, particularmente en animales de producción. En algunos casos, desajustes entre el ADN mitocondrial y el ADN nuclear pueden interrumpir procesos como el desarrollo de la placenta, contribuyendo a embarazos anormales.
Las clones hembras transmiten sus mitocondrias a su descendencia, lo que podría resultar en una mezcla de mitocondrias donantes y hospedadoras. Sin embargo, el cuello de botella mitocondrial durante el desarrollo de los ovocitos significa que la proporción de cada tipo de mitocondria heredada por la descendencia puede variar. En los clones machos, el ADN mitocondrial no se transmite a la descendencia, ya que las mitocondrias paternas generalmente se eliminan después de la fertilización.
La producción de animales clonados con ADN mitocondrial genéticamente idéntico al del animal donante es posible si los ovocitos utilizados en el proceso provienen de la línea materna genéticamente relacionada con el animal donante. Esto se puede lograr recolectando óvulos a través de OPU.
Ambiente
Los factores ambientales, como la salud uterina, la nutrición, el ejercicio y la manipulación durante el desarrollo, pueden influir en el fenotipo de los animales clonados. Esta influencia es especialmente evidente cuando se espera que el fenotipo del animal clonado coincida con el del donante, pero exhibe variabilidad debido a diferencias en el entorno. Por ejemplo, CC, la gata clonada, mostró rasgos de comportamiento distintos a los de su donante genético, probablemente porque fue criada en un entorno más estimulante. Estas observaciones enfatizan que, si bien la identidad genética se conserva en los animales clonados, los factores ambientales pueden dar lugar a diferencias fenotípicas. Este fenómeno también se observa en caballos, cuyas marcas blancas en el pelaje pueden variar en cantidad y ubicación entre individuos clonados, a pesar de compartir la misma composición genética. Estas variaciones en las marcas blancas en diferentes caballos clonados resaltan la influencia de los factores ambientales uterinos en el fenotipo.
La diferenciación celular ocurre en cascadas, donde la diferenciación de un tipo celular afecta al estado de las células circundantes. Durante el desarrollo, la multiplicación celular y la apoptosis ocurren en respuesta a numerosos estímulos ambientales e internos. Por lo tanto, se producirán variaciones individuales aleatorias en la composición de los tejidos, incluso en individuos con el mismo origen genético.
Mutaciones Genéticas
Las células utilizadas para la clonación, particularmente aquellas cultivadas in vitro, pueden acumular anomalías cromosómicas durante el pasaje. A medida que las células crecen y se dividen en cultivo, aumenta el riesgo de mutaciones, lo que puede afectar la viabilidad del embrión clonado. Sin embargo, la mayoría de los embriones derivados de células con anomalías cromosómicas significativas no llegan a término, limitando el impacto de tales mutaciones en los clones nacidos vivos.
Se ha informado del nacimiento de una yegua clonada a partir de un donante macho. Estudios posteriores revelaron la pérdida del cromosoma Y durante el cultivo celular o el proceso de clonación, resultando en una hembra con un genotipo y fenotipo XO. Esta rara ocurrencia pone de relieve la posible inestabilidad cromosómica que puede surgir durante la clonación, particularmente en relación con los cromosomas sexuales.
Estado Actual de la Clonación en Diversas Especies
Se han producido crías vivas con éxito por transferencia nuclear en todas las principales especies de mamíferos domésticos, incluyendo gatos, perros, caballos, vacas, búfalos, cabras, ovejas, cerdos y camellos.
Clonación de Gatos
La clonación en gatos ha sido relativamente exitosa, con ovocitos a menudo obtenidos de tejido recuperado durante ovariohisterectomías. La clonación de gatos domésticos se utiliza principalmente para replicar mascotas, y su aplicación se ha expandido para incluir esfuerzos de conservación de felinos salvajes en peligro de extinción mediante la clonación interespecies. Aunque la tasa de éxito en la producción de gatitos vivos clonados sigue siendo modesta, está en constante mejora gracias a los avances tecnológicos.
Clonación de Perros
Desde el nacimiento del primer perro clonado del mundo, Snuppy, en 2005, la SCNT se ha empleado ampliamente para clonar diversos tipos de perros con fines variados. Sin embargo, la clonación de perros enfrenta importantes obstáculos biológicos. La biología reproductiva canina es única, ya que es necesario extraer ovocitos maduros del oviducto después de la ovulación, dado que los métodos de maduración in vitro aún no son fiables. Además, los ciclos estrales en las perras ocurren solo aproximadamente dos veces al año, lo que limita la disponibilidad de ovocitos y complica la sincronización con los receptores.
A pesar de estos obstáculos, la clonación comercial de perros ha tenido éxito, con varias empresas produciendo perros clonados para propósitos específicos, como la preservación de perros de trabajo de élite o mascotas queridas, y el apoyo a la investigación en modelos animales. El proceso también se ha aplicado a esfuerzos de conservación de especies en peligro de extinción, utilizando la tecnología SCNT para preservar material genético.
Aunque la sincronización de ovocitos sigue siendo un desafío, los continuos avances en las tecnologías reproductivas están haciendo que la SCNT en perros sea más accesible en diversos campos.
Reflexiones Históricas y Éticas sobre la Clonación
La publicación en la revista Nature del éxito en la clonación de una oveja a partir de una célula de un ejemplar adulto generó un gran debate científico y ético. El intento de obtener seres vivos viables a partir de células somáticas ha sido un objetivo científico durante mucho tiempo, pero los experimentos previos no habían arrojado resultados satisfactorios. La interpretación habitual de estos fracasos se atribuía a la pérdida de la totipotencia de las células embrionarias en etapas tempranas del desarrollo.
Una línea de trabajo sencilla consistía en la fisión embrionaria: la división de un embrión de pocas células para que cada una de ellas produjera un ser adulto completo. Este enfoque, utilizando células en estado embrionario, fue el empleado en el experimento de Hall y Stillman en 1993, que también generó controversia, principalmente por haberse realizado con embriones humanos. Dicho experimento no presentaba complicaciones técnicas especiales. Los autores tomaron 17 embriones triploides (resultado de la fecundación de un óvulo por más de un espermatozoide), que son inviables, como material de desecho. Los resultados indicaron que los embriones resultantes del estadio de dos blastómeros podían alcanzar hasta 32 células con buen aspecto, pero no se determinó si hubieran continuado desarrollándose. El experimento de Hall y Stillman buscaba determinar si las células embrionarias humanas en estadio de mórula poseían totipotencia. Aunque pareció confirmar esta suposición para el estadio de embrión de dos células, las conclusiones son discutibles, ya que se realizó con embriones triploides inviables. Por lo tanto, no se sabe con certeza qué ocurriría con embriones normales.
El segundo objetivo del experimento de Hall y Stillman era práctico: aumentar el rendimiento de la fecundación in vitro en mujeres que respondían pobremente a la estimulación hormonal. La clonación, mediante la división de los pocos embriones obtenidos, podría ofrecer a estas parejas las mismas posibilidades de tener un hijo que aquellas que producen muchos embriones. Sin embargo, la fiabilidad de esta técnica es baja, dado el alto número de embriones que mueren, incluso sin manipulación. La clonación de embriones humanos es especialmente delicada en comparación con la de terneros, donde la división de embriones de razas selectas se ha practicado con éxito, aunque con un rendimiento pobre.
El éxito de la técnica de clonación de la oveja Dolly, publicado por el equipo del Instituto Roslin, se basó en la transferencia nuclear de células somáticas adultas. El procedimiento implicó cultivar células de la ubre de una oveja adulta en un medio con concentración decreciente de proteínas para detener su división. Posteriormente, se extrajo el núcleo de óvulos y se fusionaron las células cultivadas con los ovocitos enucleados mediante un pulso eléctrico. Este pulso provocaba la fusión celular y activaba el metabolismo del ovocito, similar a la fertilización. El rendimiento de la técnica fue muy bajo: de 277 fusiones, solo se obtuvieron 29 embriones, y de ellos, nació solo un cordero, Dolly. La revista Nature publicó un comentario sobre las repercusiones científicas de este experimento, sugiriendo que los prejuicios sobre el papel del genoma en el desarrollo habían impedido un análisis más profundo de las consecuencias teóricas. La hipótesis genética del desarrollo, que asume la activación y represión programadas de genes, es cuestionada por fenómenos de interacción celular y especialización autónoma de funciones celulares, bien conocidos por la embriología experimental.
La clonación terapéutica, que busca obtener células madre embrionarias/pluripotentes para investigación o terapia, difiere de la clonación reproductiva. En la clonación terapéutica, el embrión precoz resultante de la TNCS no se implanta, sino que se induce la diferenciación de sus células para obtener células madre pluripotentes. Las células madre pluripotentes inducidas (iPSCs), descubiertas por Shinya Yamanaka, representan una alternativa clave, ya que permiten obtener células pluripotentes sin necesidad de crear embriones, reduciendo así el debate ético.
La clonación reproductiva, aunque ha sido aplicada en algunas especies animales, está prohibida en humanos en la mayoría de los países debido a implicaciones éticas y médicas. Su baja eficiencia, complejidad y riesgos la convierten en una práctica no habitual. La clonación terapéutica, aunque no es una técnica clínica rutinaria, es una línea de investigación con gran potencial biomédico.
La clonación de células madre humanas ha sido un área de gran interés para la medicina regenerativa. El escándalo del científico surcoreano Dr. Hwang, quien afirmó haber logrado la clonación de embriones humanos en 2004 pero luego se descubrió que había falsificado datos, resaltó los desafíos y controversias en este campo. La cafeína se ha introducido como un factor clave en la clonación de monos y humanos para mejorar la eficiencia del desarrollo de blastocistos y la obtención de células madre embrionarias.
La técnica de transferencia nuclear celular, que implica la introducción del material genético de una célula donante en un ovocito enucleado, es fundamental en la clonación. Los avances en este campo, como la adición de cafeína, han mejorado las tasas de éxito. Sin embargo, persisten problemas bioéticos y técnicos, como la necesidad de un número considerable de óvulos sanos y el borrado incompleto de las marcas epigenéticas del ADN de la célula donante.
Las aplicaciones terapéuticas potenciales de las células madre embrionarias son amplias, pero aún se requiere mucha investigación básica para asegurar su inocuidad y prevenir la posible aparición de cáncer, un efecto secundario asociado a su alta capacidad de multiplicación y diferenciación.
El futuro de la clonación animal: Desafíos, oportunidades y ética 🧬🔬
Consideraciones Éticas y Legales
La clonación reproductiva, especialmente en humanos, plantea profundas cuestiones éticas y legales. La opinión generalizada, incluso entre los propios investigadores como Ian Wilmut, es que la clonación humana no debería intentarse debido a su naturaleza aberrante y falta de utilidad clínica. Intentar recuperar a una persona fallecida mediante clonación resultaría en un individuo distinto, influenciado por su propio contexto vital, más similar a un gemelo tardío que a una reencarnación. Desde el punto de vista deontológico, el respeto al ser humano en estado embrionario y la alta tasa de fracasos en la clonación hacen que su aplicación sea inaceptable hasta que estos fallos se reduzcan drásticamente.
Las declaraciones europeas a menudo se basan en los derechos humanos básicos para prohibir la clonación humana. En contraste, el entorno legal estadounidense, que prioriza la libertad individual, presenta un desafío mayor para la prohibición. La Comisión creada por el presidente Clinton para estudiar la cuestión y la prohibición de la financiación federal a la investigación de clonación humana reflejan la complejidad del debate. La distinción entre tener un hijo y "fabricar" uno, y el derecho humano a nacer como fruto del amor en una familia, son aspectos cruciales que se difuminan con la manipulación genética y la clonación, abriendo la puerta a propuestas consideradas aberrantes, como la fabricación de órganos de repuesto.
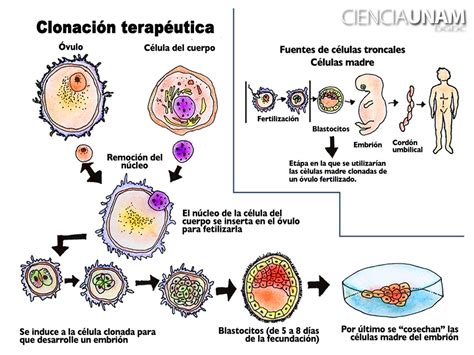
La clonación, aunque ofrece un potencial biomédico considerable, sigue siendo un tema polémico. La clonación reproductiva tiene un uso muy limitado y está restringida en la mayoría de los países, mientras que la clonación terapéutica, a pesar de no ser una técnica clínica rutinaria, representa una línea de investigación prometedora. La posibilidad de obtener células madre pluripotentes sin necesidad de crear embriones, como con las iPSCs, ha reducido parte del debate ético asociado.
tags: #clonar #nucleo #diferenciado #en #ovulo