Las células madre embrionarias (CME), también conocidas como ESC por sus siglas en inglés (Embryonic Stem Cells), han capturado la imaginación de científicos y del público en general debido a su asombroso potencial. Son un tipo especial de células que poseen dos propiedades fundamentales: la capacidad de auto-renovarse, produciendo más células idénticas a sí mismas, y la capacidad de diferenciarse, es decir, convertirse en cualquier otro tipo celular del cuerpo. Esta característica las convierte en las células maestras del organismo, siendo la base de todas las demás células, incluidas las sanguíneas, nerviosas y de órganos. Dada esta versatilidad, las CME son las células madre más potentes y valiosas para la investigación y su aplicación potencial en terapias regenerativas.
Origen y Características de las Células Madre Embrionarias
¿Qué son las Células Madre Embrionarias (CME)?
Las células madre embrionarias son células pluripotentes, lo que significa que tienen la capacidad de generar cualquier tipo celular. Provienen de embriones en sus primeras fases de desarrollo, específicamente entre los tres y cinco días de vida, una etapa conocida como blastocisto. Estos blastocistos contienen alrededor de 100 a 150 células y las CME son consideradas las más versátiles, capaces de convertirse en todas las células del feto en desarrollo.
Origen: El Blastocisto
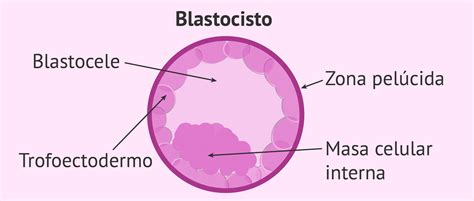
Las células madre embrionarias se cultivan a partir de células encontradas en el embrión de tan solo unos pocos días de edad. En humanos, ratones y otros mamíferos, el embrión en esta etapa es una esfera celular llamada blastocisto. El blastocisto está constituido por dos partes principales:
- La capa externa de células, o trofectodermo, que formará la placenta que contiene al embrión conforme va creciendo en el útero.
- Un grupo interno de células, conocido como masa celular interna, que es un agregado de 10 a 20 células. Estas células no están diferenciadas o especializadas y se multiplicarán y diferenciarán extensamente para formar los muchos tipos de células que se necesitan para formar un animal entero. Las células de la masa celular interna son pluripotentes, capaces de diferenciarse en cualquier tipo de célula en el cuerpo.
Además de estas, en el blastocisto también se distinguen la zona pelúcida (una membrana externa de glicoproteína) y el blastocele (una cavidad interna rellena de líquido).
Pluripotencia: Estados Naïve y Primed
La pluripotencia de las CME puede manifestarse en dos estados distintos:
- Pluripotencia primed (‘preparada’): Este estado ya contiene el germen de una diferenciación concreta.
- Pluripotencia naïve (‘no preparada’): Representa un estado primordial y anterior en el desarrollo embrionario. Posee una mayor capacidad para diferenciarse en cualquier tipo celular, lo que le confiere una mayor relevancia en investigación. El estado naïve es el más óptimo para la búsqueda de tratamientos para afecciones cardiacas o enfermedades neurodegenerativas, entre otras.
Sin embargo, el estado naïve es inherentemente inestable, ya que estas células reciben continuamente señales que promueven tanto su diferenciación al estado primed como su auto-renovación. Entender los mecanismos que regulan estos estados de pluripotencia es importante, ya que podrían mejorar el mantenimiento de los cultivos de CME con pluripotencia naïve equilibrada y duradera.
Mantenimiento y Cultivo de Células Madre Embrionarias
Métodos para el Mantenimiento del Estado Naïve
El método clásico para mantener las CME en el estado naïve se basa en inhibir dos de las vías de señalización que promueven precisamente la diferenciación de estas células, un método conocido como 2i. Más recientemente, se ha logrado generar CME en este estado utilizando una aproximación completamente distinta: inhibiendo la actividad de Cdk8/19, una proteína que controla la expresión de numerosos genes, incluyendo aquellos que ayudan a mantener el estado naïve. Aunque ambas aproximaciones permiten cultivar células naïve, los mecanismos moleculares exactos implicados son todavía poco conocidos.
Técnicas de Cultivo en Laboratorio
Una vez que la masa celular interna se obtiene de un blastocisto y se le proporcionan los nutrientes adecuados, es posible cultivarla en el laboratorio. En este entorno, el proceso de maduración y especialización celular que normalmente ocurriría en el embrión se detiene. En cambio, las células se multiplican para producir más células desdiferenciadas similares a la masa celular interna, que son las CME.
Para su crecimiento en buenas condiciones y su multiplicación sin problemas, las células madre embrionarias a menudo requieren la ayuda de otras células. Es común el uso de cultivos con sistema de feeder layer, una capa de células alimentadoras inactivadas. Estas células alimentadoras, que suelen ser fibroblastos de ratón, se siembran en soportes de cultivo y han sido radiadas para inactivar su división. Aunque radiadas, son células vivas con metabolismo activo que aportan importantes beneficios al cultivo, como una mezcla indefinida y compleja de componentes de la matriz extracelular y factores de crecimiento, sin invadir el cultivo debido a su incapacidad de proliferar.
Es crucial que las CME cultivadas in vitro sean diploides estables y tengan un cariotipo normal, ya que la mayoría de las líneas celulares usadas en laboratorios pueden presentar problemas de ploidía y cariotipos extraños. Las CME pueden vivir y crecer en soluciones especiales en probetas o placas de Petri en los laboratorios.
Investigación y Avances Científicos
La Proteómica en el Estudio de las CME
Investigadores de la Unidad de Proteómica del Centro Nacional de Investigaciones Oncológicas (CNIO), liderados por Javier Muñoz, han descrito mecanismos moleculares hasta ahora desconocidos que contribuyen al mantenimiento de las células madre embrionarias en su estado ‘naïve’. Sus hallazgos, publicados en Nature Communications, son cruciales para mejorar el uso de estas células en la búsqueda de tratamientos para infartos cerebrales, afecciones cardiacas o enfermedades neurodegenerativas como el alzhéimer o el párkinson.
Utilizando la proteómica, una técnica que estudia el conjunto de proteínas expresadas por el genoma de un organismo, el equipo del CNIO ha descrito una gran parte de los eventos moleculares que estabilizan estas valiosas células. Es la primera vez que se utiliza una aproximación proteómica en este contexto. Los mecanismos se analizaron a diferentes niveles:
- A nivel de fosfoproteoma: estudiando las proteínas que han experimentado fosforilación, un proceso químico que regula (activa o inhibe) sus funciones.
- Analizando la expresión de esas proteínas.
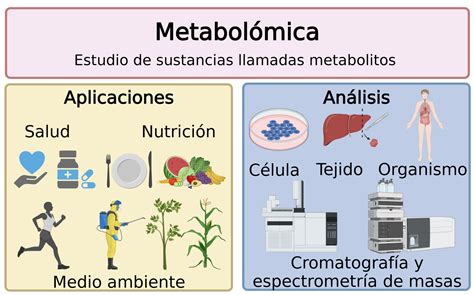
- Estudiando los cambios en los metabolitos, sustancias que producen las proteínas al llevar a cabo sus funciones.
Esta aproximación integrativa permite obtener una imagen precisa de las causas de la plasticidad celular que presentan las CME.
Implicaciones para la Investigación del Cáncer
Los resultados de esta investigación también podrían tener implicaciones para el estudio de algunos tipos de cáncer. Se sabe que la inhibición de Cdk8 reduce la proliferación celular en leucemia mieloide aguda a través de la activación de supresores tumorales, y que en cáncer colorrectal Cdk8 actúa como un oncogén. La actividad de Cdk8 es enigmática, ya que posee funciones completamente distintas dependiendo del contexto celular. Los datos revelados por el CNIO, que muestran numerosas dianas de Cdk8 hasta ahora desconocidas, pueden ayudar a entender mejor las funciones que controla esta proteína en otros contextos biológicos.
La Importancia de la Proteómica
El trabajo del equipo del CNIO evidencia la necesidad de integrar plenamente la proteómica en las estrategias de investigación básica y biomédica. Mientras la genómica (estudio del ADN) y la transcriptómica (estudio del ARN mensajero) han impulsado grandes avances, la proteómica es fundamental para completar el círculo. Estas últimas no pueden estudiar procesos que tienen lugar después de que las proteínas han sido creadas, como la fosforilación. Con la proteómica, se pueden estudiar propiedades de las proteínas que no están codificadas en la información genética y, por tanto, son inexplorables solo al estudiar ADN y ARN. Esto es crucial, ya que las proteínas son las responsables últimas de cumplir las funciones vitales de la célula.
Avances en la Generación de CME Humanas a partir de Células Adultas: La Transferencia Nuclear de Células Somáticas (SCNT)
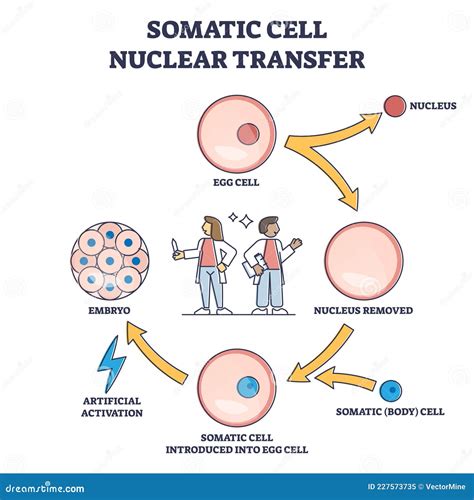
Por primera vez, un equipo de científicos ha conseguido producir células madre embrionarias humanas a partir de células adultas de la piel, un avance publicado en la revista Cell. Este descubrimiento abre un nuevo camino para entender las causas específicas de la enfermedad de un paciente y para desarrollar terapias personalizadas, permitiendo generar células madre para pacientes con órganos o tejidos dañados y regenerar tejidos u órganos completos. Este logro fue posible gracias a la técnica de transferencia nuclear de células somáticas (SCNT por sus siglas en inglés), la misma que dio lugar a la oveja Dolly, aunque en este caso no se trata de clonar un ser vivo. La técnica consiste en transferir el núcleo de una célula donante a un óvulo, generando así un embrión casi idéntico al donante original, lo que permite generar cualquier tipo celular necesario.
En el pasado, la SCNT se había utilizado para producir CME en ratones y monos, pero los intentos en humanos habían fracasado por desconocimiento de los factores que promueven el desarrollo embrionario por SCNT. El equipo de Shoukhrat Mitalipov, de la Health & Science University de Oregón, optimizó los protocolos en monos y los aplicó con éxito para transferir el núcleo de una célula epitelial a un óvulo. Sorprendentemente, se logró con solo dos óvulos, a pesar de que se pensaba que se necesitarían miles para la SCNT en humanos.
Modelos de Ratón Quimera en Investigación
Los primeros cultivos de células embrionarias de ratón derivadas de blastocistos se realizaron en 1981, sentando las bases para el desarrollo de metodologías similares en células embrionarias humanas. Estas células aisladas se denominaron células madre o troncales embrionarias. Muchas áreas de la ciencia utilizan CME de ratones para estudiar cómo los blastocistos crecen hasta convertirse en células adultas y qué señales dirigen a las células madre a diferenciarse en células especializadas.
Es habitual en investigación biomédica utilizar ratones quimera, es decir, ratones adultos generados a partir de blastocistos a los que se les han introducido células madre embrionarias portadoras de determinada enfermedad o alteración genética. Se ha aprendido mucho sobre el desarrollo embrionario y la enfermedad analizando estos ratones quimera con CME genéticamente modificadas. Estos modelos permiten a los investigadores analizar cómo genes específicos contribuyen a las funciones y enfermedades celulares.
Las células madre de ratón pueden ser reintroducidas en un blastocisto de ratón, y este blastocisto, a su vez, puede regresarse al útero de una ratona para su crecimiento. Las células inyectadas participan en el desarrollo del embrión, resultando en un cachorro con una mezcla de células: tanto del blastocisto huésped como de las células derivadas de las CME inyectadas, a este nuevo ratón con células de dos orígenes diferentes se le llama una quimera.
Las quimeras pueden heredar los genes de las células madre embrionarias a su descendencia, permitiendo a los investigadores alterar los genes de las CME en el laboratorio, regresarlas a los blastocistos y producir nuevos ratones con genes alterados o “mutaciones”. Los científicos utilizan ratones genéticamente modificados para estudiar genes involucrados en muchas enfermedades humanas, como las mutaciones encontradas en cánceres. El gran valor de esta técnica fue reconocido en 2007 con el Premio Nobel de Medicina, otorgado a tres científicos pioneros en el uso de CME para crear ratones genéticamente modificados.

Aplicaciones Terapéuticas de las Células Madre Embrionarias
La versatilidad de las células embrionarias las convierte en un material perfecto para ser investigado y utilizado en diversos procesos biomédicos. Los principales usos de las células madre embrionarias son:
Desarrollo de Nuevos Fármacos
Una de las grandes aportaciones de las CME a la ciencia es su enorme valor para el screening de nuevos fármacos. Antes de su lanzamiento al mercado, un fármaco debe superar pruebas exhaustivas para determinar su idoneidad para el consumo humano, tradicionalmente realizadas en animales antes de ensayos en humanos. La práctica actual busca aplicar estas pruebas sobre células madre pluripotentes para evaluar con mayor exactitud la efectividad de un medicamento o, por el contrario, revelar su toxicidad. El tejido más comúnmente objetivo para obtener a través de células embrionarias para estos fines es el del hígado, corazón o riñón, órganos frecuentemente afectados por los efectos secundarios de tratamientos experimentales. Los investigadores también pueden usar tipos de células madre programadas para convertirse en células de tejidos específicos para probar la seguridad y eficacia de nuevos medicamentos, ayudando a evaluar si causan toxicidad en el corazón, por ejemplo.
Reemplazo Celular y Medicina Regenerativa
La medicina regenerativa, o terapia de reemplazo celular, consiste en reemplazar células dañadas por células funcionales para restituir la función normal de tejidos u órganos de manera eficaz, evitando así otras terapias como trasplantes o tratamientos farmacológicos. Esta terapia con células madre embrionarias se aplica a pacientes con lesiones en la médula espinal, enfermedad de Parkinson, diabetes tipo 1, esclerosis lateral amiotrófica, Alzheimer, problemas cardíacos, quemaduras, cáncer o incluso osteoartritis. Las CME pueden ser orientadas para convertirse en células específicas que se pueden usar en personas para regenerar y reparar tejidos que la enfermedad dañó o afectó. Los tratamientos con células madre también podrían beneficiar a personas con leucemia, enfermedad de Hodgkin, linfoma no hodgkiniano, algunos tipos de cáncer de tumor sólido, anemia aplásica e inmunodeficiencias.
Células madre: ¿Cómo funcionan y por qué se les llama madre? - #EspecialMSP
Clonación Terapéutica (Transferencia Nuclear de Células Somáticas - SCNT)
La clonación terapéutica es una práctica que consiste en generar un embrión clonado para producir células embrionarias que tengan la misma carga genética que la célula donante. El objetivo es utilizar estas células en experimentos para analizar en profundidad cómo se producen las enfermedades y desarrollar nuevos tratamientos. Esta técnica, que es una forma de crear células madre versátiles e independientes de óvulos fecundados, implica extraer el núcleo de un óvulo no fecundado y reemplazarlo con el núcleo de una célula donante. El óvulo resultante se divide, formando un blastocisto y, a partir de él, una línea de células madre genéticamente idéntica a las células del donante, en esencia, un clon. Se cree que las células madre derivadas de la clonación terapéutica podrían ofrecer mayores beneficios al ser menos propensas al rechazo inmunológico una vez trasplantadas al donante, además de permitir a los investigadores comprender cómo se desarrolla una enfermedad específica.
Consideraciones Éticas y Desafíos
El Debate Ético sobre el Uso de Embriones Humanos
La obtención y uso de células madre embrionarias humanas genera un intenso debate ético que debe abordarse con respeto y rigor. El dilema ético surge porque las CME se obtienen de embriones en etapa temprana, un grupo de células que se desarrollan cuando un óvulo es fecundado. Para algunos, usar estas células equivale a sacrificar una vida humana (la del embrión), mientras que para otros, un blastocisto que no se implanta en el útero no tendría la posibilidad de prosperar y, por tanto, no es equivalente a un feto.
Los embriones utilizados en la investigación provienen de óvulos fertilizados en clínicas de fertilización in vitro que nunca fueron implantados en el útero de una mujer y son donados con el consentimiento informado de los donantes. Las pautas para la investigación con células madre humanas, como las establecidas por los Institutos Nacionales de Salud en 2009, definen cómo pueden usarse las CME e incluyen recomendaciones para su donación, especificando que solo se pueden utilizar embriones creados mediante fertilización in vitro cuando ya no sean necesarios para fines reproductivos.
Perspectivas Religiosas y el Argumento de los 14 Días
Las diferentes religiones abordan el estatus de un embrión humano temprano de distintas maneras. Los católicos romanos, ortodoxos e iglesias protestantes conservadoras creen que el embrión tiene el estatus de un humano desde la concepción y que la investigación con embriones no debería permitirse. Por otro lado, el judaísmo y el islam, destacando la importancia de ayudar a otros, argumentan que el embrión no tiene el estatus completo de un humano antes de los 40 días y permiten alguna investigación con embriones. Otras religiones mantienen posiciones diversas.
Existe también el argumento de los 14 días, una corriente de opinión que establece un límite temporal para la investigación embrionaria. Este es un punto de consenso en muchas legislaciones.
Regulación Legal en España
En España, la investigación con células madre embrionarias está regulada por la Ley sobre Técnicas de Reproducción Humana Asistida y la Ley de Investigación Biomédica. Estas normativas exigen la firma de un consentimiento informado por parte de los progenitores, donde explican el destino que desean para sus embriones congelados sobrantes de un ciclo de fecundación in vitro, entre los que se encuentra la investigación con células madre.
Diferencias y Retos entre CME de Ratón y Humanas
Existen diferencias entre el funcionamiento de las CME en ratones y en humanos. Por razones éticas y morales, los investigadores no pueden utilizar las CME humanas con la misma libertad que en experimentos con ratones, lo que exige enfoques más complejos e indirectos para entender su funcionamiento. Aunque los científicos han logrado hacer CME a partir de la masa celular interna de embriones humanos usando técnicas similares a las de ratones, no está permitido inyectar CME humanas de nuevo en blastocistos.
A pesar de ello, se siguen haciendo esfuerzos para aprender a crear diferentes tipos de células especializadas exponiendo las CME a distintas moléculas de señalización y condiciones de crecimiento. Se están utilizando CME de ratones para comprender el desarrollo del cuerpo desde las primeras fases embrionarias hasta la formación de órganos complejos, e incluso se intenta crear órganos primitivos en el laboratorio. Sin embargo, controlar exactamente cómo las CME se diferencian en numerosos tipos de células especializadas sigue siendo un desafío muy importante. Un objetivo principal es generar grandes cantidades de células especializadas de manera uniforme y fiable, lo cual no es tarea fácil.
Desafíos en la Aplicación Clínica en Humanos
Para que las CME sean útiles en terapias humanas, los investigadores deben garantizar que se diferenciarán en los tipos específicos de células deseados. Aunque se han descubierto formas de orientar su diferenciación (por ejemplo, hacia células cardíacas), la investigación en esta área continúa. Además, las CME pueden multiplicarse de forma irregular o especializarse espontáneamente en diferentes tipos de células, lo que exige un control preciso de su proliferación y desarrollo. Otro problema es que las CME pueden desencadenar una respuesta inmunitaria en el receptor, quien las atacaría como invasores extraños. También existe la posibilidad de que las células madre no funcionen como se esperaba, con consecuencias desconocidas. Los investigadores continúan estudiando cómo evitar estas posibles complicaciones.
Tipos de Células Madre y su Comparación
Además de las células madre embrionarias, existen otros tipos de células madre con distintos potenciales:
Células Madre Adultas
Estas células se encuentran en pequeñas cantidades en la mayoría de los tejidos adultos, como la médula ósea o la grasa. En comparación con las células madre embrionarias, las adultas tienen una capacidad más limitada para generar diferentes células del cuerpo, lo que restringe su uso para tratar ciertas enfermedades. Aunque prometedoras, no son tan versátiles ni duraderas como las embrionarias y son más propensas a irregularidades debido a peligros ambientales o errores durante la duplicación. Sin embargo, se ha descubierto que son más adaptables de lo que se pensaba inicialmente.
Células Madre Pluripotentes Inducidas (iPSC)
Los científicos han logrado transformar células adultas normales en células madre mediante reprogramación genética. Al modificar los genes de células adultas, los investigadores pueden hacer que actúen de manera similar a las CME, creando las llamadas células madre pluripotentes inducidas (iPSC). Esta técnica permite usar células reprogramadas en lugar de CME, evitando los problemas éticos asociados con el uso de embriones y previniendo el rechazo inmunitario a las nuevas células. Se ha demostrado que es posible reprogramar células comunes del tejido conectivo para que se conviertan en células cardíacas funcionales, lo que en estudios con animales mejoró la función cardíaca y el tiempo de supervivencia. Sin embargo, aún no se sabe si el uso de iPSC causará efectos adversos en humanos, y el proceso de reprogramación es todavía insuficiente.
Células Madre Perinatales
Los investigadores han descubierto células madre en el líquido amniótico y en la sangre del cordón umbilical. Estas células madre pueden convertirse en células especializadas. El líquido amniótico llena la bolsa que rodea y protege al feto en desarrollo en el útero, y las CME se han identificado en muestras obtenidas mediante amniocentesis.
Terapias con Células Madre Existentes
La aplicación de células madre en medicina ya es una realidad en algunos ámbitos. Los médicos han realizado trasplantes de células madre, también conocidos como trasplantes de médula ósea, durante muchas décadas. En estos trasplantes de células madre hematopoyéticas, las células madre reemplazan a las células dañadas por la quimioterapia o la enfermedad, o permiten que el sistema inmunitario del donante combata ciertos tipos de cáncer y enfermedades relacionadas con la sangre. La leucemia, el linfoma, el neuroblastoma y el mieloma múltiple suelen tratarse de esta forma. Estos trasplantes utilizan células madre adultas o de sangre del cordón umbilical. Los investigadores están probando células madre adultas para tratar otras afecciones, incluidas algunas enfermedades degenerativas, como la insuficiencia cardíaca.
tags: #creacion #de #celulas #madre #embrionarias