El sistema cardiovascular es el primero en alcanzar madurez funcional durante el desarrollo embrionario. Comienza a aparecer hacia la mitad de la tercera semana del desarrollo intrauterino, cuando el embrión ya no es capaz de satisfacer sus necesidades nutritivas por mecanismos primitivos, como la difusión desde la sangre materna. Nuestro sistema circulatorio no funciona del mismo modo cuando estamos dentro del útero materno que cuando llegamos al mundo. Durante el embarazo, la sangre fluye a través del feto de manera diferente que cuando nacemos. El corazón y el aparato circulatorio del feto comienzan a formarse poco después de la concepción. Al final de la quinta semana, el corazón puede bombear sangre a todo el cuerpo. Al igual que en un corazón ‘adulto’, el corazón prenatal desarrolla cuatro cavidades y cuatro válvulas.
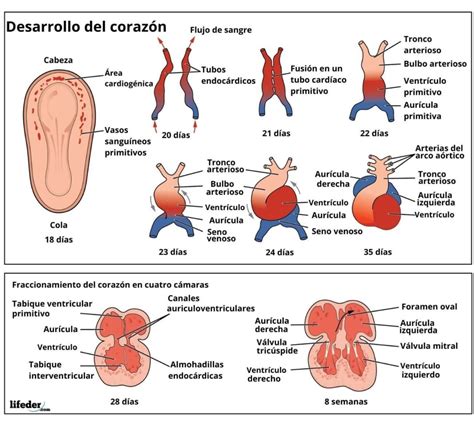
La Circulación Fetal
En la circulación fetal, la sangre rica en oxígeno se envía desde el cuerpo de la madre hasta la vena cava inferior del feto a través de la placenta y el cordón umbilical. El corazón del feto consta de dos aurículas, dos ventrículos y dos grandes arterias. Antes de continuar con la explicación de la circulación fetal, es importante destacar que el sistema cardiovascular del feto está diseñado de tal manera que la sangre rica en oxígeno se distribuye preferentemente al miocardio y al cerebro. La sangre proveniente de la placenta, rica en oxígeno, llega al feto a través de la vena umbilical. El conducto venoso de Arancio permite que la mayor parte de esta sangre oxigenada evite el hígado y pase directamente a la vena cava inferior. La vena cava también recibe sangre pobre en oxígeno procedente del cuerpo del feto.
La aurícula derecha está comunicada a través del foramen oval con la aurícula izquierda, por tanto, cuando la sangre oxigenada llega a la aurícula derecha, la mayor parte de esta sangre va a fluir de forma preferente a través del foramen oval hacia la aurícula izquierda, para ser conducida, pasando por el ventrículo izquierdo, hacia la arteria aorta ascendente. La mayor parte de la sangre mezclada en la aurícula derecha es empujada hacia la aurícula izquierda a través del foramen oval. A partir de ahí, se desplaza hacia el ventrículo izquierdo, que bombea la sangre hacia la aorta.
Desde el ventrículo derecho, este volumen de sangre circula a través de la arteria pulmonar en dirección a los pulmones. Sin embargo, como los pulmones aún no funcionan como órganos de intercambio gaseoso, la sangre se dirige desde la arteria pulmonar hasta la aorta a través del conducto arterial (ductus arterioso). El 8-15% de la sangre que llega a la circulación pulmonar es para el propio tejido pulmonar, mientras que el resto se desvía de derecha a izquierda a través del ductus arterioso sin problemas.
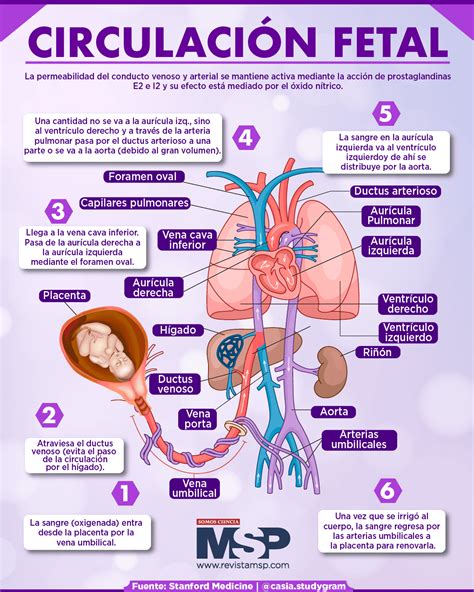
Transición de la Circulación Fetal a la Neonatal
Al nacer, el cordón umbilical se corta y el bebé ya no recibe oxígeno de la madre. Este evento marca el inicio de una transición fundamental en el sistema cardiovascular. El cierre del cordón umbilical y el inicio de la respiración desencadenan cambios drásticos en la hemodinámica fetal.
Cambios Fisiológicos Clave al Nacimiento:
- Cierre del Foramen Oval: Tras el nacimiento, con el aumento de la presión en la aurícula izquierda y la disminución de la presión en la aurícula derecha, el foramen oval tiende a cerrarse. Si este cierre se retrasa, el flujo sanguíneo pulmonar (FSP) disminuye y se compromete la mezcla interauricular. En algunos neonatos, esto puede requerir una septostomía auricular de emergencia (maniobra de Rashkind).
- Cierre del Conducto Arterial: Al incrementar de manera brusca la tensión arterial de oxígeno tras el nacimiento, se produce una constricción del ductus arterioso. El tejido ductal y el aumento del contenido de óxido nítrico contribuyen a este cierre. Los vasos umbilicales se contraen tras la ligadura del cordón, causando su trombosis. Tras el nacimiento, el conducto arterial se cierra espontáneamente en la mayoría de los recién nacidos a término, generalmente en las próximas 4-6 semanas.
- Cierre del Conducto Venoso de Arancio: Se cierra el conducto venoso de Arancio, vaso sanguíneo del feto que une la vena cava con la vena umbilical, pasando a ser el ligamento venoso y provocando la obstrucción de los vasos umbilicales.
- Expansión Pulmonar: Los pulmones comienzan a expandirse con las primeras respiraciones. A medida que se expanden los pulmones, el fluido de los alvéolos desaparece, permitiendo la entrada de aire y el inicio del intercambio gaseoso. La sangre pobre en oxígeno del lado derecho del corazón se bombea ahora a través de la arteria pulmonar hacia los pulmones.
- Cambio de la Circulación en Serie a Paralelo: La circulación en paralelo, característica del feto, pasa a estar en serie, de modo que cada ventrículo debe bombear sangre de forma independiente al sistema pulmonar o sistémico.
Circulación fetal y cambios al nacimiento
La transición de la circulación fetal a la neonatal es un proceso complejo y uno de los eventos más significativos y drásticos en la vida humana. Comprender la relevancia clínica y el manejo de la adaptación adversa es crucial para los médicos que atienden a recién nacidos.
Retraso del Cierre Ductal y su Impacto
El retraso del cierre del ductus arterioso (DAP) está inversamente relacionado con la edad gestacional. Podemos encontrar una incidencia de un 20% en prematuros mayores de 32 semanas hasta el 60% en menores de 28 semanas. Este hecho puede relacionarse con el déficit de surfactante pulmonar, ya que, en prematuros que no presentan síndrome de distrés respiratorio, el cierre ductal se produce en un período similar al de los recién nacidos a término.
Fisiopatología del Ductus Arterioso Persistente (DAP):
El ductus arterioso, desde la 6ª semana de gestación, soporta la mayor parte del débito del ventrículo derecho, que constituye el 60% del gasto cardíaco total. La persistencia del ductus durante la vida fetal y su cierre tras el nacimiento es el resultado de una compleja y coordinada interacción entre la presión parcial de oxígeno, factores neuro-humorales locales y circulantes, y las características específicas de la estructura del músculo liso de la pared ductal.
Tras el nacimiento, al incrementar de manera brusca la tensión arterial de oxígeno, se produce una constricción del ductus arterioso. En pacientes con un tamaño similar de ductus arterioso, el cierre puede ser más lento. La evaluación del ductus arterioso persistente (DAP) mediante Doppler muestra un patrón de flujo pulsátil.
Presión Arterial y Factores Neonatales
La presión arterial está determinada por el gasto cardíaco y las resistencias vasculares. La presión arterial en los prematuros está condicionada por la prematuridad, el bajo peso, la administración de corticoides a la madre y la puntuación en el test de Apgar al nacimiento. Antes de cualquier tratamiento, es importante valorar el grado de perfusión, la frecuencia cardíaca, la presencia de acidosis y la diuresis.
Diagnóstico y Cardiopatías Congénitas
Actualmente, y gracias a los avances en el campo del diagnóstico fetal, los nuevos ecocardiógrafos permiten valorar con alta resolución la estructura cardiaca, su concordancia con los grandes vasos y, mediante Doppler, estudiar alteraciones del ritmo cardíaco. La ecocardiografía funcional y la evaluación hemodinámica en niños son herramientas invaluables.
Las cardiopatías congénitas son las malformaciones congénitas más frecuentes y son la causa más frecuente de insuficiencia cardiaca en neonatos y lactantes. Se estima que en España 8-9/1000 nacidos vivos serán diagnosticados de cardiopatía congénita y que el 90% de ellos presentan problemas cardiovasculares frecuentes como comunicación interventricular, comunicación interauricular, persistencia del ductus, etc.
Manifestaciones y Tipos de Cardiopatías Congénitas:
- En este tipo de patologías, la manifestación clínica más evidente es la cianosis sin dificultad respiratoria. El debut en este tipo de cardiopatías suele ser brusco, debido al cierre del ductus arterioso.
- En estas cardiopatías, el ductus aporta gran parte del flujo sistémico al existir una obstrucción al paso de volemia en el tracto de entrada o salida del ventrículo izquierdo. Ante la sospecha de una cardiopatía congénita neonatal, se debe identificar la dependencia o no del flujo a través del ductus arterioso para mantener su gasto cardíaco. En algunas cardiopatías, la dependencia del ductus es vital, ya que su cierre puede llevar a una disminución intensa del flujo pulmonar o sistémico que puede desencadenar la muerte.
- La Tetralogía de Fallot (TF) es la cardiopatía compleja más común, representando el 5-10% de todas las cardiopatías congénitas y afectando a 1 de cada 8,500 recién nacidos vivos, con una mayor incidencia en varones.
- La atresia pulmonar con comunicación interventricular (AP+CIV) se caracteriza por la falta de conexión funcional entre el ventrículo derecho y las arterias pulmonares, acompañada de un defecto en el tabique interventricular, generalmente perimembranoso.
- La transposición de las grandes arterias (TGA) afecta a alrededor de 1 de cada 2,000-4,000 recién nacidos vivos, constituyendo aproximadamente el 5-7% de todas las cardiopatías congénitas, con una mayor incidencia en varones según un ratio de 1.5:1 a 3:1.
- La coartación de aorta (CoA) es un estrechamiento de la aorta descendente que provoca hipoperfusión de órganos y congestión retrógrada, afectando al 6-8% de las cardiopatías congénitas, con mayor prevalencia en varones. Suele ser una estenosis localizada, pero puede implicar un segmento hipoplásico o tortuoso, y frecuentemente se asocia con otras malformaciones cardíacas como la válvula aórtica bicúspide y la hipoplasia del arco aórtico.
- La comunicación interventricular (CIV) se define como un defecto en el tabique interventricular que permite la comunicación entre ambos ventrículos. Es la cardiopatía congénita más frecuente, excluyendo la válvula aórtica bicúspide, con una prevalencia aproximada de 4 de cada 1000 recién nacidos vivos.
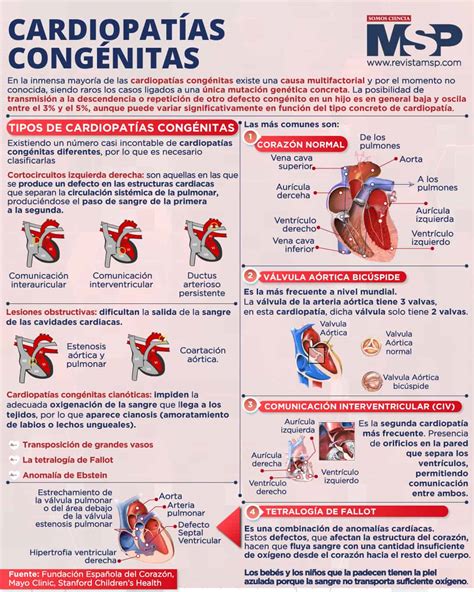
Coartación de Aorta (CoA) y su Dinámica Fetal y Postnatal:
Intraútero, la coartación de aorta (CoA) no compromete la hemodinámica fetal debido a que la mayoría del flujo sanguíneo pasa por el ductus arterioso (DA) desde la arteria pulmonar hacia la aorta descendente. Sin embargo, la CoA aumenta ligeramente la postcarga del ventrículo izquierdo (VI), elevando la presión en la aurícula izquierda (AI) y reduciendo el flujo a través del foramen oval. Esto aumenta el volumen del ventrículo derecho (VD) y el flujo por el DA, disminuyendo el flujo hacia el VI y la aorta ascendente, lo que agrava la discrepancia de calibre aórtico.
Al nacer, el cierre del ductus puede causar fibrosis y estenosis de la zona yuxtaductal, llevando a hipoperfusión distal y congestión retrógrada. Los mecanismos de compensación incluyen hipertrofia ventricular izquierda para manejar la mayor postcarga y el desarrollo de colaterales arteriales para mejorar el flujo anterógrado y aliviar la congestión.
Comunicación Interventricular (CIV) y su Comportamiento Hemodinámico:
En los recién nacidos, las resistencias vasculares pulmonares (RVP) están elevadas y disminuyen progresivamente en las primeras semanas de vida, lo que reduce la presión en el ventrículo derecho (VD) y aumenta el cortocircuito entre ambos ventrículos (de izquierda a derecha). En las CIV pequeñas (restrictivas), el cortocircuito de izquierda a derecha es escaso, manteniendo la presión en el VD y las RVP normales. En los defectos medianos, el cortocircuito es mayor y puede elevar la presión en el VD, aunque esta sigue siendo inferior a la sistémica y las RVP generalmente no están elevadas. En las CIV grandes, la relación entre las resistencias sistémicas y pulmonares determina la situación hemodinámica.
Insuficiencia Cardíaca en Neonatos
La insuficiencia cardíaca (IC) es un síndrome clínico que se produce cuando el corazón no puede satisfacer las demandas de oxígeno del organismo. El gasto cardíaco, que es la cantidad de sangre bombeada por el corazón en un período de tiempo determinado, es un factor clave en la función cardíaca. En muchas cardiopatías congénitas, la contractilidad del miocardio está conservada, pero pueden existir alteraciones en los otros factores que afectan el volumen latido y, por lo tanto, el gasto cardíaco. Por ejemplo, la sobrecarga de volumen puede aumentar la precarga, mientras que la sobrecarga de presión puede aumentar la postcarga.
Adaptación Adversa y Patologías Asociadas:
La adaptación adversa de la circulación transicional puede ser causada por múltiples factores, incluyendo la disfunción del miocardio, la hipertensión pulmonar persistente (HPPN) y la sepsis. La HPPN se evalúa mejor midiendo la presión de la arteria pulmonar. La disfunción biventricular puede ocurrir debido a la interdependencia ventricular. El bajo peso al nacer (< 28 semanas de gestación) puede afectar la transición cardiovascular.
El escenario de asfixia perinatal, la acidosis e hipoxia, que son los vasoconstrictores pulmonares más potentes, pueden deteriorar aún más la función cardíaca debido a postcarga aumentada. La administración de oxígeno inducirá constricción adicional del ductus arterioso. El shock neonatal, ya sea frío (sepsis temprana) o caliente (inducida por las citoquinas), es una respuesta compleja al shock.
Cianosis y Shunts Cardiovasculares:
La cianosis puede ser un signo clínico evidente en cardiopatías congénitas. Dependiendo del tipo de cardiopatía, puede haber un shunt de derecha a izquierda a través del ductus arterioso, el foramen oval, o una comunicación interventricular. Algunas cardiopatías, como la estenosis pulmonar severa, pueden causar cianosis dependiente del grado de estenosis.
Comprender el impacto de estas alteraciones hemodinámicas en la vida postnatal temprana es fundamental para el manejo de neonatos con cardiopatías congénitas. Las condiciones graves que conllevan una alta mortalidad temprana requieren una intervención rápida y precisa.
tags: #circulacion #sistemica #pulmonar #y #fetal