ZOVIRAX es el nombre comercial del aciclovir, un análogo sintético de nucleósido con actividad contra los virus del herpes. La Suspensión Oral de ZOVIRAX es una formulación destinada a la administración oral.
Composición y Propiedades del Aciclovir
El aciclovir, USP, es un polvo cristalino blanco con la fórmula molecular C8H11N5O3 y un peso molecular de 225. Su solubilidad máxima en agua a 37°C es de 2.5 mg/mL. La actividad inhibitoria del aciclovir es altamente selectiva debido a su afinidad por la enzima timidina quinasa (TK) codificada por el HSV y VZV. Esta enzima viral convierte el aciclovir en aciclovir monofosfato, un análogo de nucleótido. El monofosfato es posteriormente convertido en difosfato por la guanilato quinasa celular y en trifosfato por una serie de enzimas celulares. In vitro, el aciclovir trifosfato detiene la replicación del ADN viral del herpes.
Mecanismo de Acción Antiviral
El aciclovir trifosfato actúa contra la replicación del ADN viral del herpes de tres maneras:
- Inhibición competitiva de la ADN polimerasa viral.
- Incorporación y terminación de la cadena de ADN viral en crecimiento.
- Inactivación de la ADN polimerasa viral.
Sensibilidad Viral y Resistencia
La relación cuantitativa entre la susceptibilidad in vitro de los virus del herpes a los antivirales y la respuesta clínica a la terapia no ha sido establecida en humanos, y las pruebas de sensibilidad viral no están estandarizadas. Los resultados de las pruebas de sensibilidad, expresados como la concentración del fármaco requerida para inhibir el crecimiento del virus en cultivo celular en un 50% (IC50), varían considerablemente según diversos factores.
Utilizando ensayos de reducción de placas, la IC50 contra aislados del virus del herpes simple (HSV) varía de 0.02 a 13.5 mcg/mL para HSV-1 y de 0.01 a 9.9 mcg/mL para HSV-2. La IC50 para el aciclovir contra la mayoría de las cepas de laboratorio y aislados clínicos de VZV varía de 0.12 a 10.8 mcg/mL.
La resistencia del HSV y VZV al aciclovir puede resultar de cambios cualitativos y cuantitativos en la TK viral y/o la ADN polimerasa. Se han recuperado aislados clínicos de HSV y VZV con susceptibilidad reducida al aciclovir de pacientes inmunocomprometidos, especialmente con infección avanzada por VIH. Si bien la mayoría de los mutantes resistentes al aciclovir aislados hasta la fecha de pacientes inmunocomprometidos han resultado ser mutantes deficientes en TK, se han aislado otros mutantes que involucran el gen TK viral (TK parcial y TK alterado) y la ADN polimerasa. Los mutantes TK-negativos pueden causar enfermedades graves en lactantes y adultos inmunocomprometidos.
Farmacocinética del Aciclovir
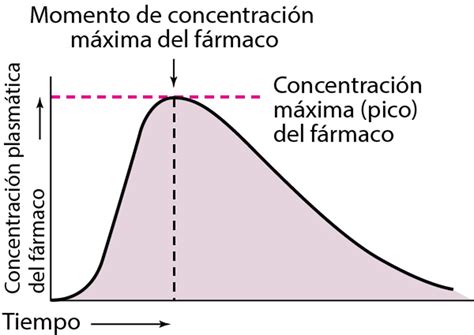
La farmacocinética del aciclovir tras la administración oral ha sido evaluada en voluntarios sanos y en pacientes inmunocomprometidos con infección por virus del herpes simple o varicela-zóster. En un estudio cruzado de dosis múltiples en sujetos sanos (n = 23), se demostró que los aumentos en las concentraciones plasmáticas de aciclovir eran menos que proporcionales a la dosis con el aumento de la dosis. La vida media y el aclaramiento corporal total del aciclovir dependen de la función renal. Las concentraciones plasmáticas de aciclovir son más altas en pacientes geriátricos en comparación con adultos más jóvenes, en parte debido a cambios relacionados con la edad en la función renal. En general, la farmacocinética del aciclovir en pacientes pediátricos es similar a la de los adultos. La coadministración de probenecid con aciclovir intravenoso ha demostrado aumentar la vida media promedio de aciclovir y el área bajo la curva tiempo-concentración.
Eficacia Clínica
Estudios controlados con placebo y doble ciego han demostrado que el ZOVIRAX administrado por vía oral reduce significativamente la duración de la infección aguda y la duración de la curación de las lesiones. En un estudio de pacientes que recibieron ZOVIRAX 400 mg dos veces al día durante 3 años, el 45%, 52% y 63% de los pacientes permanecieron libres de recurrencias en el primer, segundo y tercer año, respectivamente. Los análisis seriales de las tasas de recurrencia trimestrales para los pacientes mostraron que entre el 71% y el 87% estaban libres de recurrencias en cada trimestre.
Se llevaron a cabo tres ensayos aleatorizados, doble ciego y controlados con placebo en 993 pacientes pediátricos de 2 a 18 años con varicela. Todos los pacientes fueron tratados dentro de las 24 horas posteriores al inicio de la erupción. En 2 ensayos, ZOVIRAX se administró a 20 mg/kg 4 veces al día (hasta 3200 mg por día) durante 5 días. En el tercer ensayo, se administraron dosis de 10, 15 o 20 mg/kg 4 veces al día durante 5 a 7 días. El tratamiento con ZOVIRAX acortó el tiempo hasta la curación del 50%; redujo el número máximo de lesiones; redujo el número mediano de vesículas; disminuyó el número mediano de lesiones residuales al día 28; y disminuyó la proporción de pacientes con fiebre, anorexia y letargo al día 2. El tratamiento con ZOVIRAX no afectó las respuestas inmunitarias humorales o celulares específicas del virus varicela-zóster al mes o al año después del tratamiento.
Indicaciones de Zovirax Suspensión Pediátrica
ZOVIRAX está indicado para el tratamiento de la varicela. La Suspensión Oral de ZOVIRAX está destinada únicamente a la ingestión oral.
Advertencias y Precauciones
Se ha observado insuficiencia renal, en algunos casos resultando en muerte, con la terapia de aciclovir. Se recomienda el ajuste de la dosis al administrar ZOVIRAX a pacientes con deterioro renal. Se debe tener precaución al administrar ZOVIRAX a pacientes que reciben agentes potencialmente nefrotóxicos, ya que esto puede aumentar el riesgo de disfunción renal y/o el riesgo de síntomas reversibles del sistema nervioso central, como los reportados en pacientes tratados con aciclovir intravenoso.
No hay datos sobre el tratamiento iniciado más de 72 horas después del inicio de la erupción del herpes zóster. Se debe informar a los pacientes que ZOVIRAX no es una cura para el herpes genital y que no hay datos que evalúen si ZOVIRAX prevendrá la transmisión de la infección a otras personas. Dado que el herpes genital es una enfermedad de transmisión sexual, los pacientes deben evitar el contacto con las lesiones o las relaciones sexuales cuando haya lesiones y/o síntomas presentes para evitar infectar a sus parejas. El herpes genital también puede transmitirse en ausencia de síntomas a través de la eliminación viral asintomática.
La varicela en niños por lo demás sanos es generalmente una enfermedad autolimitada de gravedad leve a moderada. Los adolescentes y adultos tienden a tener una enfermedad más grave.
Estudios de Toxicidad y Seguridad
El aciclovir fue probado en bioensayos de por vida en ratas y ratones a dosis diarias únicas de hasta 450 mg/kg administrados por sonda nasogástrica. No hubo diferencias estadísticamente significativas en la incidencia de tumores entre los animales tratados y los controles, ni el aciclovir acortó la latencia de los tumores. El aciclovir fue probado en 16 ensayos genéticos in vitro e in vivo. El aciclovir no afectó la fertilidad o la reproducción en ratones (450 mg/kg/día, p.o.) o en ratas (25 mg/kg/día, s.c.). En el estudio en ratones, los niveles plasmáticos fueron de 9 a 18 veces los niveles humanos, mientras que en el estudio en ratas, fueron de 8 a 15 veces los niveles humanos. A dosis más altas (50 mg/kg/día, s.c.) en ratas y conejos (11 a 22 y 16 a 31 veces los niveles humanos, respectivamente), la eficacia de implantación, pero no el tamaño de la camada, se redujo. No se observaron anomalías testiculares en perros tratados con 50 mg/kg/día, IV durante 1 mes (21 a 41 veces los niveles humanos) o en perros tratados con 60 mg/kg/día por vía oral durante 1 año (6 a 12 veces los niveles humanos).
El aciclovir administrado durante la organogénesis no fue teratogénico en ratones (450 mg/kg/día, p.o.), conejos (50 mg/kg/día, s.c. e IV), o ratas (50 mg/kg/día, s.c.). No existen estudios adecuados y bien controlados en mujeres embarazadas. Se estableció un registro epidemiológico prospectivo del uso de aciclovir durante el embarazo en 1984 y se completó en abril de 1999. Se siguieron 749 embarazos en mujeres expuestas a aciclovir sistémico durante el primer trimestre del embarazo, resultando en 756 resultados. La tasa de ocurrencia de defectos de nacimiento se aproxima a la encontrada en la población general. Sin embargo, el pequeño tamaño del registro es insuficiente para evaluar el riesgo de defectos menos comunes o para permitir conclusiones fiables o definitivas sobre la seguridad del aciclovir en mujeres embarazadas y sus fetos en desarrollo.
Se han documentado concentraciones de aciclovir en la leche materna en 2 mujeres después de la administración oral de ZOVIRAX, oscilando entre 0.6 y 4.1 veces los niveles plasmáticos correspondientes. Estas concentraciones podrían exponer potencialmente al lactante a una dosis de aciclovir de hasta 0.3 mg/kg/día.
Uso en Pacientes Geriátricos
De los 376 sujetos que recibieron ZOVIRAX en un estudio clínico de tratamiento del herpes zóster en sujetos inmunocompetentes ≥50 años, 244 tenían 65 años o más, mientras que 111 tenían 75 años o más. No se informaron diferencias generales en la eficacia en cuanto al tiempo hasta la cesación de la formación de nuevas lesiones o el tiempo hasta la curación entre los sujetos geriátricos y los sujetos adultos más jóvenes. La duración del dolor después de la curación fue mayor en pacientes de 65 años o más. Las náuseas, los vómitos y los mareos se informaron con mayor frecuencia en sujetos de edad avanzada. Los pacientes de edad avanzada son más propensos a tener una función renal reducida y a requerir ajuste de dosis. Los pacientes de edad avanzada también son más propensos a tener eventos adversos renales o del SNC. Con respecto a los eventos adversos del SNC observados durante la práctica clínica, se informaron somnolencia, alucinaciones, confusión y coma con mayor frecuencia en pacientes de edad avanzada.
Eventos Adversos
Los eventos adversos más frecuentes reportados durante los ensayos clínicos de tratamiento del herpes genital con ZOVIRAX 200 mg administrado por vía oral 5 veces al día cada 4 horas durante 10 días fueron náuseas y/o vómitos en 8 de 298 tratamientos de pacientes (2.7%). Los eventos adversos más frecuentes reportados en un ensayo clínico para la prevención de recurrencias con administración continua de 400 mg (dos cápsulas de 200 mg) dos veces al día durante 1 año en 586 pacientes tratados con ZOVIRAX fueron náuseas (4.8%) y diarrea (2.4%).
Además de los eventos adversos reportados en ensayos clínicos, los siguientes eventos se han identificado durante el uso post-comercialización de ZOVIRAX. Debido a que se reportan voluntariamente de una población de tamaño desconocido, las estimaciones de frecuencia no se pueden hacer.
Eventos Adversos Neurológicos (Post-Comercialización)
- Agitación
- Ataxia
- Coma
- Confusión
- Disminución de la conciencia
- Delirio
- Mareos
- Disartria
- Encefalopatía
- Alucinaciones
- Parestesia
- Psicosis
- Convulsiones
- Somnolencia
- Temblores
Eventos Adversos Urogenitales (Post-Comercialización)
- Insuficiencia renal
- Dolor renal (puede estar asociado con insuficiencia renal)
- Nitrógeno ureico elevado en sangre
- Creatinina elevada
- Hematuria
Sobredosis
Se han reportado sobredosis que involucran la ingestión de hasta 100 cápsulas (20 g). Los eventos adversos reportados en asociación con la sobredosis incluyen agitación, coma, convulsiones y letargo. La precipitación de aciclovir en los túbulos renales puede ocurrir cuando se excede la solubilidad (2.5 mg/mL) en el líquido intratubular. Se han reportado sobredosis después de inyecciones en bolo o dosis inapropiadamente altas y en pacientes cuyo equilibrio de líquidos y electrolitos no fue monitoreado adecuadamente. Esto ha resultado en elevación del BUN y la creatinina sérica y posterior insuficiencia renal.
Dosificación y Administración
La dosificación de Zovirax Suspensión Pediátrica debe ajustarse según la indicación específica y la función renal del paciente.
Dosis Recomendadas (Ejemplos)
- Tratamiento de infecciones por VHS (herpes simple): 200 mg de aciclovir cinco veces al día, aproximadamente cada 4 horas, omitiendo la dosis nocturna. El tratamiento se debe iniciar tan pronto como sea posible tras el comienzo de la infección.
- Tratamiento de varicela e infecciones por herpes zóster: 800 mg de aciclovir 5 veces al día, aproximadamente cada 4 horas, omitiendo la dosis nocturna. El tratamiento se debe iniciar tan pronto como sea posible tras el comienzo de la infección.
- Profilaxis de infecciones por VHS en pacientes inmunocomprometidos: Las dosis orales recomendadas no conducirán a la acumulación de aciclovir por encima de los niveles establecidos como seguros por infusión intravenosa.
- Pacientes pediátricos (2 años o más): Dosis para adultos.
- Lactantes y niños menores de 2 años: La mitad de la dosis para adultos.
- Pacientes con insuficiencia renal: Se debe considerar la posibilidad de insuficiencia renal y, en consecuencia, se deberá ajustar la dosis.
- Pacientes de edad avanzada: Se debe considerar la posibilidad de insuficiencia renal y, en consecuencia, se deberá ajustar la dosis.
No diluya la formulación de la suspensión oral.
Información Adicional
Almacenamiento: Almacenar a temperatura ambiente y lejos del calor excesivo y la humedad (no en el baño). Mantenga todos los medicamentos fuera de la vista y del alcance de los niños.
Interacciones Medicamentosas: Informe a su médico y farmacéutico qué medicamentos con y sin receta médica, vitaminas, suplementos nutricionales y productos a base de hierbas toma o tiene planeado tomar. Muchos otros medicamentos también podrían interactuar con el aciclovir.
Embarazo y Lactancia: Si queda embarazada mientras toma aciclovir, llame a su médico. Las concentraciones de aciclovir se han documentado en la leche materna.
Conducción y Uso de Maquinaria: No se han realizado estudios para investigar el efecto de aciclovir en la capacidad para conducir o utilizar máquinas. No se puede predecir un efecto perjudicial sobre estas actividades a partir de la farmacología del principio activo.
IMPORTANTE⚠️ PEDIATRAS EN E.E.U.U. RECOMIENDAN USO DE ANTIVIRALES EN MANEJO DE COVID-19 EN. NIÑOS
tags: #zovirax #suspension #pediatrica