La variabilidad genética se refiere a la diversidad en las frecuencias de los genes dentro de una población. Esta diversidad puede manifestarse como diferencias entre individuos o entre distintas poblaciones. En el genoma humano, la variabilidad puede presentarse en diversas formas, desde polimorfismos de nucleótido simple (SNPs) hasta variaciones a mayor escala, como la duplicación o deleción de segmentos de ADN de cientos o miles de pares de bases. Estas diferencias pueden implicar tener un número distinto de copias de un segmento genético o incluso la inversión de un orden de genes, como un orden ABC frente a ACB. Es importante destacar que no todas estas variaciones son necesariamente patológicas.
Un ejemplo clásico de adaptación a cambios ambientales es el de las mariposas del abedul (Biston betularia), cuya coloración ha variado desde el inicio de la Revolución Industrial. Su camuflaje original se volvió ineficaz cuando la contaminación oscureció las cortezas de los árboles, alterando el entorno donde solían posarse.
La evolución, desde la perspectiva de la genética de poblaciones, se debe a procesos que resultan en cambios en las características genéticas de las poblaciones a lo largo del tiempo. Las mutaciones, que son cambios en el ADN de los organismos, pueden afectar desde un solo nucleótido hasta cromosomas enteros. Estas mutaciones son consideradas la fuente principal de variabilidad genética en una población. Si bien el efecto inmediato de una mutación en una generación suele ser mínimo, con el tiempo, una cantidad considerable de variación puede acumularse. La mayoría de las mutaciones, al afectar la probabilidad de persistencia en la población, tienden a perderse. Sin embargo, algunas mutaciones pueden tener efectos insignificantes en la adaptación, mientras que otras pueden mejorarla, promoviendo su mantenimiento.
La variabilidad genética es, en esencia, la cantidad de genotipos diferentes presentes en una población determinada. La reproducción sexual juega un papel crucial en la generación de descendencia distinta de sus progenitores y entre sí. Durante la meiosis, se producen gametos (células sexuales) con la mitad de cromosomas que las células somáticas. El proceso de entrecruzamiento en la profase I de la meiosis permite el intercambio de información genética entre cromosomas homólogos, y el reparto aleatorio de estos cromosomas en la separación posterior asegura que cada gameto contenga una mezcla única de material genético paterno y materno.
Otros mecanismos que influyen en la variabilidad genética de las poblaciones incluyen la deriva genética, que ocurre cuando las proporciones alélicas cambian en una población, y el flujo génico, que implica la transferencia de alelos entre poblaciones. La deriva genética puede manifestarse a través del efecto fundador, cuando un pequeño grupo aislado da origen a una nueva población con variabilidad reducida, o el efecto cuello de botella, que ocurre cuando solo unos pocos individuos sobreviven a un evento de alta mortalidad, limitando la diversidad genética de la población resultante.
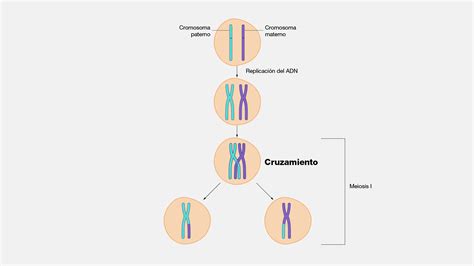
Variabilidad Genética y Fecundación Humana
Un estudio liderado por la Universidad Johns Hopkins ha aportado información clave sobre las razones por las cuales menos de la mitad de las concepciones humanas llegan a término. Este trabajo proporciona evidencia sobre las vías moleculares que generan un riesgo variable de errores cromosómicos en humanos, según Rajiv McCoy, biólogo computacional especializado en genética de la reproducción humana.
La pérdida del embarazo es un evento frecuente en humanos, estimándose que alrededor del 15% de los embarazos reconocidos terminan en aborto espontáneo, además de numerosas concepciones perdidas en etapas muy tempranas. La mayoría de estos errores cromosómicos se originan en el óvulo y su frecuencia aumenta con la edad materna. La comprensión de estos fenómenos requiere el análisis de datos genéticos de un gran número de embriones y sus progenitores.
Rajiv McCoy señala que, al ser un rasgo ligado a la supervivencia y al éxito reproductivo, la evolución tiende a limitar las diferencias genéticas con efectos pequeños. El equipo de investigación analizó datos de embriones de FIV (fertilización in vitro), encontrando asociaciones significativas en genes que regulan el apareamiento, la recombinación y la unión de cromosomas durante la formación del óvulo. Un gen destacado en este estudio es el SMC1B, crucial para mantener unidos los cromosomas. La meiosis femenina, que comienza durante el desarrollo fetal y se interrumpe hasta la ovulación y fecundación, es un proceso complejo donde pueden surgir estos errores.
A pesar de la identificación de genes asociados con la pérdida gestacional, predecir el riesgo individual sigue siendo un desafío. Las variantes genéticas comunes, según los investigadores, tienen un impacto menor en comparación con factores como la edad materna o el entorno.
Recomendaciones para el Estudio Genético en Disfunción Reproductiva
Expertos en reproducción han actualizado las recomendaciones para el estudio genético e inmunológico en parejas con disfunción reproductiva, con el objetivo de mejorar la asistencia sanitaria. Estas recomendaciones se clasifican según la relevancia para la toma de decisiones clínicas: alta, moderada y baja.
Introducción a la Genética y la Inmunología Reproductiva
Los avances en el conocimiento del genoma humano y la inmunopatología, junto con el desarrollo de técnicas de biología molecular, permiten un análisis exhaustivo de enfermedades y ofrecen información relevante para el diagnóstico, pronóstico y tratamiento de parejas con problemas reproductivos. La inmunología reproductiva estudia los cambios en la respuesta inmunológica durante la fertilización, implantación, desarrollo placentario y parto. Sin embargo, persisten interrogantes sobre cómo la unidad feto-placentaria evita el rechazo inmunitario materno.
La realización de estudios genéticos o inmunológicos se basa en la historia clínica, características y antecedentes familiares de la pareja. Es fundamental evitar exploraciones y tratamientos innecesarios. Antes de incorporar nuevas pruebas diagnósticas, se debe considerar su impacto sanitario, prevalencia, eficacia, coste-efectividad, calidad, magnitud de la asociación genotipo-enfermedad, interacción con otros factores de riesgo, intervenciones preventivas o terapéuticas, impacto económico y aspectos éticos, legales y sociales.
Las recomendaciones se dirigen a especialistas como ginecólogos, urólogos, genetistas clínicos, andrólogos y especialistas de medicina de laboratorio, para estandarizar los estudios de causas genéticas o inmunológicas. Se excluyen el estudio de enfermedades mitocondriales y sistémicas asociadas con alteraciones de la reproducción.
Consideraciones Éticas en Genética y Reproducción
Las nuevas tecnologías genéticas plantean diversos dilemas éticos que requieren una reflexión sobre los conceptos y valores implicados, así como la justificación de decisiones prudentes. Los beneficios potenciales, como la prevención de daños en la descendencia, generan esperanza. Sin embargo, también entran en juego los principios de justicia y autonomía, el riesgo de utilizar tecnologías no suficientemente seguras, la protección de la confidencialidad y el acceso desigual a estas tecnologías.
La transmisión de datos genéticos, especialmente en casos como la donación de gametos, plantea controversias sobre la prevalencia de la privacidad individual frente al interés común. La posibilidad de que una persona no desee conocer sus predisposiciones a enfermedades incurables es otro aspecto crucial. El consentimiento informado es primordial, buscando promover la autonomía individual y la toma de decisiones racionales, basadas en los valores y creencias propios.
La información escrita debe advertir sobre descubrimientos inesperados y su posible trascendencia, así como sobre el derecho del individuo a recibir o no dicha comunicación. También debe incluir la advertencia sobre la implicación para los familiares y la conveniencia de que el afectado transmita la información.
Recomendaciones Específicas
- Todas las Unidades de Reproducción deben contar con asesoría genética especializada.
- En caso de solicitar tests de secuenciación masiva, es necesario explicar detalladamente el estado actual de la ciencia, ofrecer información clara y veraz, y obtener el consentimiento informado.
- No se puede garantizar la ausencia de peligro de alteración genética en la descendencia, incluso con la realización de tests.
- Debe evitarse la publicidad engañosa sobre los tests de secuenciación masiva y sus beneficios.
Consulta Preconcepcional
La consulta preconcepcional tiene como objetivo identificar condiciones médicas y sociales maternas o paternas que puedan ser intervenidas antes de la gestación para minimizar su impacto. Se debe valorar a parejas consanguíneas, individuos con historial o sospecha de enfermedad hereditaria, y personas pertenecientes a grupos con alta proporción de portadores de mutaciones para enfermedades hereditarias.
Entre los antecedentes familiares relevantes para la evaluación preconcepcional se incluyen la existencia de varios miembros de la familia con la misma afectación, personas con malformaciones mayores, retraso del desarrollo, discapacidad intelectual o anomalías en el crecimiento. Es importante recopilar información sobre familiares afectos de esterilidad, retraso mental, enfermedades musculares progresivas, cataratas tempranas, alteraciones de la coagulación, minusvalías, malformaciones o parálisis al nacer. Se debe investigar la consanguinidad de la pareja y realizar un árbol genealógico de al menos 3 generaciones.
Si se cumplen criterios clínicos para estudios cromosómicos, moleculares o inmunológicos, estos se realizarán antes de plantear cualquier tratamiento de reproducción.
Uso de Pruebas Genéticas e Inmunológicas
El uso de pruebas genéticas e inmunológicas se clasifica en tres categorías: alta, moderada y baja, basándose en las ventajas y riesgos de la prueba, la coherencia y precisión de los resultados, la calidad de la evidencia, la relevancia directa de las pruebas, los valores y preferencias de los afectados, y los recursos a utilizar. Se considera altamente recomendable cuando la prueba es relevante para la toma de decisiones; moderada cuando los resultados son poco consistentes; y baja cuando el beneficio es incierto.
La estrategia de búsqueda de estudios genéticos incluyó términos como cariotipo, fibrosis quística, X frágil, trombofilias, microdeleciones del cromosoma Y, FISH en el cromosoma Y, estudio de meiosis testicular, fragmentación del ADN espermático, variación en el número de copias, enfermedades autosómicas recesivas, estudios genéticos en donación de gametos y epigenética. Para estudios inmunológicos, se consideraron síndrome antifosfolípido, hipotiroidismo, enfermedad celíaca, células NK uterinas y en sangre periférica, desregulación de respuestas Th1/Th2 y Th17/Treg, antígenos HLA y genotipo KIR materno, y lectina de unión a manosa.
El trabajo multidisciplinar para la elaboración de estas recomendaciones involucró a expertos de diversas sociedades científicas, quienes revisaron literatura científica y definieron un documento de consenso. La evaluación del documento mediante la herramienta AGREE-II resultó en una puntuación global aceptable, recomendándose su uso en la práctica clínica.
Recomendaciones de Estudios Genéticos en la Mujer
La indicación de pruebas genéticas en mujeres con disfunción reproductiva se clasifica en alta, moderada o baja, basándose en la historia clínica, y se presentan en tablas específicas.
Cariotipo en Sangre Periférica
La frecuencia de anomalías cromosómicas en recién nacidos es del 0,7% al 0,8%. Las parejas con disfunción reproductiva presentan una mayor prevalencia de anomalías cromosómicas, tanto estructurales como numéricas. La aneuploidia más común asociada a esterilidad femenina es la monosomía del cromosoma X (síndrome de Turner), resultado de una no disyunción cromosómica durante la meiosis. Las alteraciones cromosómicas constitucionales pueden contribuir al fracaso reproductivo (esterilidad o abortos recurrentes) sin presentar manifestaciones clínicas evidentes.
Cariotipo en Abortos
El aborto espontáneo es la complicación más frecuente del embarazo, siendo las alteraciones cromosómicas la causa principal en el primer trimestre (50-60% de los abortos involuntarios). La trisomía es la más frecuente, seguida por poliploidia y monosomía X. La detección de anomalías cromosómicas espontáneas en el aborto es crucial para determinar las causas de la pérdida gestacional y proporcionar asesoramiento genético adecuado a las familias.
Fibrosis Quística
La fibrosis quística (FQ) es una enfermedad autosómica recesiva causada por mutaciones en el gen cystic fib...
MITOSIS Y MEIOSIS 🧐 Explicación fácil sobre sus DIFERENCIAS
tags: #variabilidad #genetica #fecundacion