La retinopatía del prematuro (RDP) es una patología ocular que afecta a los recién nacidos prematuros, especialmente aquellos de bajo peso corporal. Esta condición representa un riesgo incrementado de defectos visuales futuros, incluida la ceguera, y se suma a otras comorbilidades propias de la prematuridad.
Históricamente, el uso del oxígeno se introdujo en la práctica neonatal sin estudios aleatorios rigurosos, y su dosificación no siempre fue controlada. A pesar de los avances en la monitorización de los niveles de oxígeno, como la pulsioximetría, la oxigenoterapia sigue siendo un tratamiento frecuente en las unidades de cuidados intensivos neonatales, a menudo sin límites o controles estrictos. La relación entre la prematuridad, el oxígeno y la RDP ha sido objeto de estudio durante décadas, y la comprensión de este proceso continúa evolucionando.
La RDP es una alteración proliferativa de los vasos sanguíneos de la retina inmadura, que afecta principalmente a los recién nacidos de muy bajo peso (RNMBP) y de menor edad gestacional. Su gravedad es variable y se clasifica mediante un examen detallado del fondo de ojo. La Clasificación Internacional de la Retinopatía del Prematuro (ICROP) establece la severidad en etapas y zonas, según la localización de las lesiones. El objetivo de la detección es identificar los RN con retinopatía que requieren tratamiento para evitar un déficit visual severo o ceguera.
Diagnóstico y Población de Riesgo
La detección de la RDP se enfoca principalmente en los RNMBP y aquellos con una edad gestacional inferior a 32 semanas. Sin embargo, también se ha propuesto un criterio basado en la edad postmenstrual. La detección se realiza a través de oftalmoscopía binocular indirecta, con una lente de 20 a 28 dioptrías, por un oftalmólogo con experiencia. El inicio de la detección suele basarse en la historia natural de la enfermedad, comenzando generalmente entre las 4 y 6 semanas postnatales.
Los criterios para iniciar la detección, según la edad gestacional, indican que el 99% de las retinopatías severas ocurren después de las 31 semanas de edad postmenstrual o 4 semanas postnatales. En pacientes con vascularización inmadura o en etapas tempranas en zonas II o III, el examen puede realizarse cada dos semanas. El examen ocular se suspende cuando la vascularización retiniana alcanza la ora serrata en 360 grados, o a una edad postmenstrual de 50 semanas en ausencia de enfermedad pre-umbral, y a las 45 semanas en retinopatía no tipo 1. En casos tratados con agentes anti-VEGF, la suspensión del examen se recomienda a las 65 semanas de edad postmenstrual debido a que esta terapia altera la historia natural de la enfermedad.
La población con riesgo de RDP incluye:
- Neonatos por debajo de las 27 semanas de gestación.
- Pacientes neonatos con peso inferior a 1000 gramos.
- Neonatos con complicaciones sistémicas, como hemorragias intraventriculares.
La Clasificación Internacional de la Retinopatía del Prematuro (ICROP), revisada en 2005, unifica criterios y describe seis grados de severidad basándose en cuatro parámetros: localización, estadio, extensión y presencia de Enfermedad Plus.
Parámetros de Clasificación de la RDP
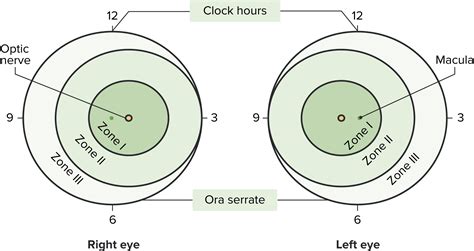
- Localización: Se determina según tres zonas centradas en el disco óptico (Zona I, Zona II, Zona III).
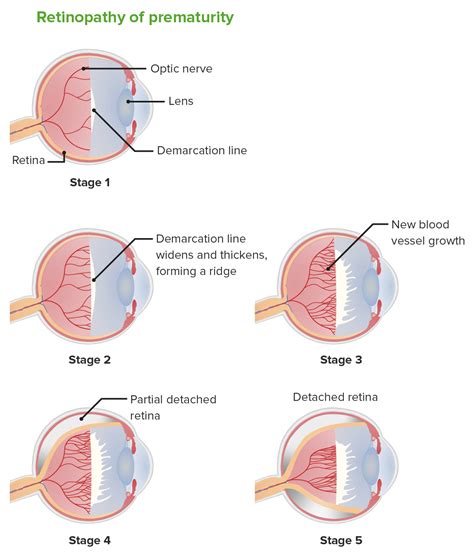
- Estadio: Describe la progresión de la enfermedad.
- Estadio 1: Una línea delgada, blanco-grisácea y tortuosa paralela a la hora serrata.
- Estadio 2: La línea de demarcación se convierte en una cresta de tejido que se extiende fuera del plano de la retina.
- Estadio 3: Cresta con proliferación fibrovascular extraretiniana.
- Estadio 4: Desprendimiento de retina subtotal traccional.
- Estadio 5: Desprendimiento de retina total.
- Extensión: Determinada por el número de horas de la esfera del reloj afectadas.
- Presencia de Enfermedad Plus: Se presenta en un 6% de los recién nacidos prematuros con pesos inferiores a 1.200 gramos, caracterizada por dilatación de venas y tortuosidad de las arteriolas en el polo posterior retiniano.
La Clasificación Internacional de la Retinopatía del Prematuro (ICROP) establece la severidad en 5 etapas y 3 zonas, según la localización de estas. El objetivo de la detección es identificar los RN con retinopatía que requieren tratamiento, con la finalidad de evitar un déficit visual severo o ceguera.
El diagnóstico se puede realizar mediante la cámara de campo amplio denominada RETCAM.
Tratamiento de la Retinopatía del Prematuro
Actualmente, la mayoría de las retinopatías del prematuro regresan espontáneamente. Solo menos del 10% de las retinopatías en Estadio 1 y 2 progresan hacia la enfermedad umbral. Los tratamientos se aplican en función de la afectación de las retinas.
Terapias Tradicionales y Actuales
Hace 30 años, la crioterapia fue el primer tratamiento efectivo para la retinopatía umbral o severa. Consiste en la quemadura por frío de la retina avascular inmadura. Posteriormente, la fotocoagulación con láser se convirtió en el método preferido, ofreciendo resultados iguales o mejores que la crioterapia, con menor dolor e inflamación. La terapia con láser continúa siendo el tratamiento estándar para la retinopatía umbral, evitando en más de un 80% la progresión de la enfermedad.
Sin embargo, el tratamiento con láser puede presentar complicaciones como hemorragia vítrea, hifema, cataratas, aumento de vicios de refracción y la destrucción de la retina periférica avascular, lo que resulta en un campo visual limitado. Además, el equipo láser tiene un costo considerable y requiere dominio y destreza del oftalmólogo.
Por estos motivos, se han explorado nuevas alternativas terapéuticas con menos complicaciones o secuelas. El estudio ETROP (Early Treatment for Retinopathy of Prematurity) estableció guías actuales de tratamiento más eficaces y oportunas para la RDP de tipo 1, determinando que la fotocoagulación con láser en esta RDP tiene una alta tasa de éxito visual y anatómico. Se definió como RDP tipo 1 aquella localizada en:
- Zona I: cualquier etapa con enfermedad plus.
- Zona I: etapa 3 ROP, con o sin enfermedad plus (raro).
- Zona II: estadios 2 o 3 ROP con enfermedad plus.
La RDP tipo 2 incluye RDP en Zona I, estadios 1 y 2 sin enfermedad plus, y RDP en Zona II, estadio 3 sin enfermedad plus. Para la RDP tipo 2 se recomienda observación continua y frecuente.
Agentes Anti-VEGF
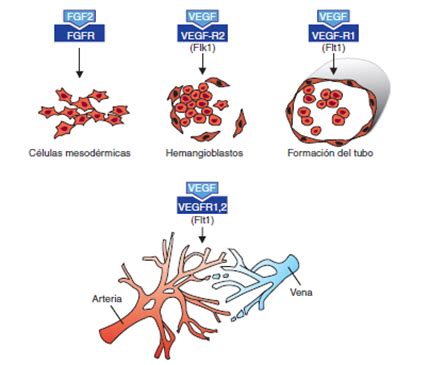
En la patogénesis de la RDP, la fase 2 se caracteriza por un aumento de los niveles circulantes de VEGF (Factor de Crecimiento Endotelial Vascular), que estimula la vasoproliferación de nuevos vasos sanguíneos. Existen varios inhibidores del VEGF, siendo el Bevacizumab (Avastin) uno de los más utilizados en niños prematuros.
El Bevacizumab es un anticuerpo monoclonal que neutraliza el VEGF, evitando su unión a los receptores endoteliales. Aunque aprobado por la FDA para tratar ciertos tipos de cáncer, aún no está aprobado específicamente para la RDP. Los reportes iniciales de su uso en neonatos datan de 2007, mostrando experiencias favorables, a veces en combinación con láser.
Estudios como el BEAT-ROP (Bevacizumab Eliminates the Progression of Threshold ROP) compararon la eficacia del Bevacizumab versus la fotocoagulación con láser en la RDP etapa 3 plus. Los resultados mostraron una menor recurrencia de la enfermedad con Bevacizumab como monoterapia en comparación con el láser, especialmente en la detención de la enfermedad en zona I.
Investigaciones posteriores han comparado la efectividad de diferentes agentes anti-VEGF (aflibercept, bevacizumab, conbercept, ranibizumab) y dosis versus el láser. Un metaanálisis en red demostró que los fármacos anti-VEGF no eran inferiores al láser en términos de tasa de retratamiento. El Bevacizumab intravítreo, incluso en dosis menores a la convencional, mostró un bajo riesgo de retratamiento y menores tiempos hasta el retratamiento.
Estudios realizados en Turquía han demostrado una eficacia similar entre los agentes anti-VEGF y el láser, pero con menores alteraciones refractivas a futuro en los niños tratados con agentes anti-VEGF. Sin embargo, el tratamiento con Bevacizumab no está exento de complicaciones, como hemorragia vítrea, hifema, endoftalmitis, desprendimiento de retina, cataratas y, de manera crítica, la disminución de los niveles séricos de VEGF, importante para el desarrollo de otros órganos.
Existen interrogantes sobre la dosis óptima y segura, el tipo de retinopatía en que debe utilizarse, el momento óptimo de administración, la necesidad de dosis adicionales, los riesgos oculares a largo plazo y los posibles efectos de la supresión del VEGF en otros órganos. Estudios sobre el neurodesarrollo de niños tratados con Bevacizumab han arrojado resultados contradictorios, lo que subraya la importancia de continuar el seguimiento ocular hasta la edad escolar y realizar más estudios multicéntricos aleatorizados sobre la seguridad a mediano y largo plazo.
Propranolol Oral
En los últimos años, el propranolol oral se ha utilizado en el tratamiento de la retinopatía del prematuro en etapas pre-umbrales, con resultados alentadores, e incluso en su prevención. El propranolol ha demostrado ser efectivo en inhibir el aumento de la expresión del VEGF y la respuesta neovascular posterior a la exposición a un ambiente hipóxico.
Se han publicado varios estudios sobre el propranolol oral como tratamiento o profilaxis de la RDP. Algunos estudios han mostrado una tendencia a la reducción en la progresión de la afectación a etapas más avanzadas y una disminución en la necesidad de tratamiento con láser y/o Bevacizumab. Un estudio piloto en neonatos con retinopatía en etapa pre-umbral demostró que el grupo tratado con propranolol no requirió tratamiento en un porcentaje significativamente mayor en comparación con el grupo control.
Otros estudios aleatorizados y controlados han evaluado el efecto del propranolol en diferentes etapas de la retinopatía. Se observó una diferencia significativamente menor en la necesidad de láser en el grupo tratado con propranolol respecto al grupo control. Sin embargo, en niños con retinopatía en etapa 1, no se encontraron diferencias en la necesidad de láser o de agentes anti-VEGF entre ambos grupos. Otro estudio observó una tendencia a menor incidencia de retinopatía y menor utilización de terapia con láser en el grupo tratado con propranolol, aunque no alcanzó significación estadística.
Nuevos Enfoques y el Futuro
El descubrimiento de marcadores como el IGF-1 (Factor de Crecimiento similar a la Insulina 1), VEGF y BFGF (Factor de Crecimiento de Fibroblastos Básico) ha representado un avance significativo en la comprensión de la patogenia de la RDP. El hallazgo de estos marcadores angiogénicos abre nuevas vías para el tratamiento.
Un estudio reciente, publicado en 2024, utilizó la metodología de metaanálisis en red (network meta-analysis) para determinar si dosis intraoculares más bajas de anticuerpos anti-VEGF son tan efectivas como dosis más altas en el tratamiento de la RDP. La investigación, que revisó 68 estudios, concluyó que el uso de dosis más bajas que las convencionales resulta eficaz con menor probabilidad de eventos adversos. Este análisis es considerado el más completo publicado hasta la fecha sobre el uso de fármacos anti-VEGF en el tratamiento de la RDP.
El futuro de la retinopatía del prematuro se enfoca actualmente más hacia la prevención de la enfermedad que hacia los tratamientos en sí. El descubrimiento de los marcadores antiangiogénicos determina un nuevo enfoque en el pronóstico y en los factores de riesgo. El conocimiento más profundo de estos factores permite un diagnóstico más certero del momento en que se produce la enfermedad, posibilitando una actuación más precoz con el tratamiento necesario antes de que las secuelas sean irreversibles.
El avance en los estudios de telemedicina, con imágenes fundoscópicas digitales de alta resolución, facilita la identificación de estos pacientes, delimita y localiza mejor las lesiones en retina, y por tanto, asegura una aplicación del tratamiento mucho más efectiva.
A pesar de los avances, sigue siendo necesario hallar un remedio y identificar el "momento ideal para tratar", de modo que no se pierdan oportunidades y que, al mismo tiempo, ningún niño sea tratado innecesariamente. Una vez efectuado el diagnóstico, no existe ningún tratamiento que detenga con eficacia el progreso hacia formas más graves, y no se dispone de ninguna medida definitiva y completamente preventiva, aparte de evitar los nacimientos prematuros.
La monitorización cuidadosa de la administración de oxígeno y la saturación de oxígeno, evitando fluctuaciones amplias y saturaciones elevadas poco después del nacimiento y durante las primeras semanas de vida, se asocia con una menor incidencia de retinopatía del prematuro grave, menor necesidad de tratamiento con láser, menos ceguera y menos displasia broncopulmonar.
El Reportero I Los riesgos a largo plazo de los bebés prematuros
tags: #retinopatia #prematuro #vegf #igf1