La detención del desarrollo embrionario, también conocida como arresto embrionario o bloqueo embrionario, es una de las experiencias más desafiantes y emocionalmente agotadoras en el camino hacia la concepción, especialmente para quienes recurren a tratamientos de reproducción asistida como la fecundación in vitro (FIV).
Este fenómeno ocurre cuando un embrión deja de dividirse antes de alcanzar la etapa de blastocisto, que es cuando está listo para ser transferido al útero. Aunque puede ser devastador, es importante comprender que se trata de un evento relativamente común y que existen diversas causas y estrategias para abordar esta problemática.
¿Qué es el Arresto Embrionario?
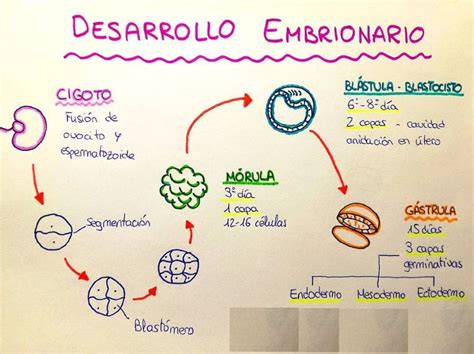
Tras la fecundación en el laboratorio, el embrión comienza un proceso de división celular: de una célula a dos, luego a cuatro, ocho y así sucesivamente. Alrededor del quinto día después de la fecundación, un embrión sano debería haber formado un blastocisto, una estructura de aproximadamente 100 a 200 células preparada para la implantación en el útero.
El arresto embrionario se define como la detención de este proceso de división celular antes de que se alcance la etapa de blastocisto. Comúnmente, los futuros padres reciben esta noticia cuando sus embriones dejan de crecer en el Día 3 o no logran desarrollarse hasta el Día 5. Este período entre el Día 3 y el Día 5 es crucial para el desarrollo embrionario, y desafortunadamente, es donde ocurren la mayoría de las detenciones. Una vez que un embrión se detiene, no reanuda su crecimiento y no puede ser utilizado para la transferencia.
Es fundamental entender que este fenómeno es mucho más común de lo que se piensa. Dependiendo de la edad y la calidad ovocitaria, es normal que solo entre el 30% y el 50% de los óvulos fecundados alcancen la etapa de blastocisto. Estudios indican que hasta dos tercios de los embriones de FIV pueden experimentar arresto del desarrollo, y casi la mitad de los embriones analizados se detienen debido a errores genéticos ocurridos durante las primeras divisiones celulares.
Lamentablemente, una vez que un embrión se detiene, no se recupera. Por ello, comprender las causas del desarrollo embrionario deficiente es esencial para poder reducir el riesgo.
Causas Principales del Arresto Embrionario
El arresto embrionario rara vez se debe a un único factor. Generalmente, es el resultado de una combinación de factores biológicos y ambientales que actúan conjuntamente. Las causas más significativas incluyen:
1. Errores Cromosómicos (Aneuploidía)
Cada vez que las células de un embrión se dividen, los 46 cromosomas deben copiarse perfectamente. Si la maquinaria de copiado comete un error, resultando en un número incorrecto de cromosomas (aneuploidía), el embrión a menudo deja de crecer como un mecanismo de protección natural. Las anomalías cromosómicas siguen siendo una de las principales causas del arresto embrionario, y este riesgo aumenta significativamente con la edad materna.
Investigaciones recientes sugieren que la mayoría de estos errores ocurren después de la fecundación, durante las divisiones celulares del propio embrión, lo que podría ser influenciado por las condiciones del cultivo en el laboratorio. Además, estudios recientes indican que incluso embriones cromosómicamente normales pueden detenerse, lo que apunta a la importancia de otros factores, como la producción de energía mitocondrial.
2. Fallo en la Activación del Propio ADN Embrionario
Durante los primeros dos o tres días después de la fecundación, el embrión depende de las instrucciones genéticas del óvulo. Alrededor del Día 3, debe ocurrir un proceso crítico: la activación del genoma embrionario (EGA, por sus siglas en inglés), donde el embrión debe activar su propio ADN y comenzar a leerlo. Si el embrión no logra esta transición, no tiene una hoja de ruta para continuar su desarrollo. En algunos casos, esta falla puede estar vinculada a mutaciones heredadas en genes maternos.
3. Deficiencia Energética del Embrión
Las mitocondrias, las "baterías" de las células, son responsables de suministrar la energía necesaria para la rápida división celular. Si las mitocondrias están debilitadas -debido al envejecimiento, daño oxidativo o factores genéticos- el embrión puede no tener suficiente energía para seguir creciendo. La calidad del óvulo está intrínsecamente ligada a la función mitocondrial; los óvulos de mayor edad tienden a tener una función mitocondrial más débil, lo que conduce a menores tasas de formación de blastocistos.
4. Daño en el ADN del Espermatozoide
La fragmentación del ADN espermático (SDF) se reconoce cada vez más como un factor significativo en el desarrollo embrionario deficiente. El espermatozoide también aporta el centrosoma, crucial para la correcta separación cromosómica durante la división celular. Si el centrosoma es defectuoso, las divisiones celulares del embrión pueden fallar desde el principio.
Las causas comunes del daño en el ADN espermático incluyen estrés oxidativo, edad paterna avanzada, tabaquismo, consumo excesivo de alcohol, obesidad y exposición a toxinas ambientales.
5. Estrés Oxidativo
El estrés oxidativo, causado por un desequilibrio entre los radicales libres y los antioxidantes, puede dañar el ADN, las proteínas y las mitocondrias. Este daño puede afectar tanto a óvulos como a espermatozoides, debilitando su capacidad para el desarrollo embrionario.
6. Condiciones del Laboratorio de FIV
El laboratorio de FIV intenta recrear el ambiente uterino, y las diferencias, por pequeñas que sean, pueden tener un impacto. Factores clave incluyen:
- Niveles de oxígeno: Cultivar embriones a niveles de oxígeno más bajos (aproximadamente 5%) ha demostrado producir mejores resultados.
- Calidad del aire: Compuestos orgánicos volátiles (COV) pueden ser perjudiciales para los embriones.
- Control de temperatura: Fluctuaciones mínimas en la temperatura de la incubadora pueden alterar el desarrollo.
- Medio de cultivo: La solución nutritiva debe estar cuidadosamente formulada y libre de contaminación.
La calidad del laboratorio varía significativamente entre clínicas, y elegir un centro con altos estándares es crucial.
Dr. Miguel Ruiz - ¿ Cómo Funciona un Laboratorio de FIV ?
Tipos de Embarazos No Evolutivos
Un embarazo no evolutivo es aquel que se ha detenido precozmente y no da lugar al nacimiento de un bebé, ocurriendo con mayor frecuencia en el primer trimestre. Aproximadamente el 70% de estos casos están relacionados con anomalías cromosómicas del embrión.
Existen varios tipos de pérdidas gestacionales tempranas:
- Aborto bioquímico: Una pérdida gestacional muy precoz, detectada por un test de embarazo positivo que posteriormente se vuelve negativo, sin llegar a visualizarse saco o embrión por ecografía.
- Aborto diferido: Diagnóstico ecográfico de detención del crecimiento embrionario o ausencia de latido cardíaco. Puede cursar con o sin sangrado, y en algunos casos requiere intervención médica.
- Gestación anembrionada (huevo huero): Diagnóstico ecográfico donde solo se visualiza el saco gestacional, sin evidencia de embrión.
- Gestación ectópica: Implanta el embrión fuera del útero, frecuentemente en las trompas de Falopio. Puede ser asintomática o presentar dolor pélvico. El diagnóstico se basa en ecografía y niveles de BHCG. El tratamiento puede ser médico o quirúrgico.
- Gestación molar: Desarrollo anormal del tejido trofoblástico (placentario) sin formación fetal. Causa un aumento exagerado de BHCG y crecimiento placentario anómalo. Requiere legrado y seguimiento de BHCG.
Soluciones y Estrategias para el Fallo de Implantación y Arresto Embrionario
Afortunadamente, existen diversas estrategias y tecnologías para abordar el fallo de implantación y el arresto embrionario, mejorando las posibilidades de éxito en los tratamientos de reproducción asistida.
1. Cultivo Largo hasta Blastocisto
Llevar el cultivo embrionario hasta la etapa de blastocisto (Día 5 o 6) permite una mejor selección embrionaria. Los embriones que alcanzan esta etapa tienen una mayor probabilidad de implantación y desarrollo. Además, la transferencia en Día 5 puede mejorar la sincronización embrión-endometrio.
2. Test Genético Preimplantacional (PGT-A)
El PGT-A (anteriormente DGP/PGS) es una técnica que permite analizar genéticamente los embriones antes de la transferencia. Mediante una biopsia embrionaria, se detectan anomalías cromosómicas, seleccionando los embriones genéticamente sanos. Esto reduce significativamente los fallos de implantación y los abortos prematuros, especialmente en mujeres de edad materna avanzada.
La tasa de éxito por transferencia de un embrión genéticamente sano se sitúa entre el 70-80%.
3. Evaluación y Mejora de la Fertilidad Masculina
En cuanto a la fertilidad masculina, es crucial analizar la fragmentación del ADN espermático. Técnicas como el test COMET y el uso de dispositivos de selección espermática (Fertile Chip/Zymöt-ICSI y Fertile Plus/ZyMōt Multi) pueden ayudar a seleccionar espermatozoides no fragmentados antes de la fecundación, reduciendo así los fallos de implantación y pérdidas gestacionales.
4. Tratamiento con Heparina
Para mujeres con trombofilias (alteraciones en la coagulación sanguínea) o trastornos que favorecen la coagulación, el tratamiento con heparina puede ser indicado para prevenir la formación de trombos a nivel endometrial y uterino, mejorando la implantación.
5. Test de Receptividad Endometrial (Test ERA)
El Test ERA es una prueba molecular que analiza la expresión de genes relacionados con la receptividad endometrial. Permite determinar si la ventana de implantación (el período óptimo para la implantación) está desplazada, y así definir el momento más adecuado para la transferencia embrionaria, ya sea un endometrio receptivo o no receptivo.
6. Eclosión Asistida (Assisted Hatching)
Esta técnica consiste en realizar un pequeño orificio en la zona pelúcida del embrión para facilitar su salida (eclosión) y posterior implantación. Puede ser útil en casos de embriones con zona pelúcida engrosada o elongada.
7. Ovodonación y Donación de Semen
La ovodonación es una excelente opción ante fallos de implantación repetidos, especialmente si el útero y el endometrio son normales. Los embriones generados con óvulos de donantes jóvenes y sanas suelen ser de alta calidad, aumentando las tasas de implantación. En casos de factor masculino severo, la donación de semen también puede ser recomendable.
8. Gestación Subrogada
Como última opción, en casos de fallos de implantación inexplicables y tras agotar otras alternativas, la gestación subrogada puede considerarse en países donde es legal.
9. Apoyo Psicológico
El impacto emocional de un embarazo no evolutivo o de fallos de implantación repetidos es inmenso. Contar con apoyo psicológico especializado es fundamental para superar estos momentos difíciles y desarrollar herramientas de afrontamiento.
Es importante recordar que la implantación es un proceso complejo que depende tanto del embrión como del endometrio. La investigación continúa avanzando para comprender mejor estos fenómenos y ofrecer soluciones cada vez más efectivas.