La Importancia de los Ovocitos Maduros en la FIV
Una de las etapas fundamentales en cualquier programa de fertilización in vitro (FIV) es la obtención de ovocitos maduros y de alta calidad, esenciales para un proceso de fertilización exitoso. Idealmente, el procedimiento de punción folicular debería resultar en la recuperación de entre el 75% y el 90% de ovocitos maduros. Estos ovocitos son los únicos capaces de ser fecundados de manera efectiva. Un porcentaje de ovocitos inmaduros que no supere el 10-25% es crucial para la eficacia del programa de FIV, ya que un mayor número de ovocitos inmaduros puede reducir significativamente las probabilidades de éxito (Human Reproduction, 2018; Comité de Práctica de ASRM, 2021; Frontiers in Endocrinology, 2023).
Los ovocitos inmaduros no pueden ser fertilizados porque carecen de una etapa genética vital: la reducción del número de cromosomas y la preparación para la fusión con el material genético del espermatozoide. Sin esta meiosis completa, no se forma un conjunto cromosómico adecuado, lo que los hace inviables para la concepción (Directrices de ESHRE, 2020; Fertility and Sterility, 2019; Journal of Assisted Reproduction and Genetics, 2025).

¿Qué Define la Madurez de un Ovocito?
El desarrollo y la maduración de los ovocitos son procesos intrincados y distintos a los de las células sexuales masculinas. La reserva ovárica se forma durante la vida intrauterina de la mujer y disminuye progresivamente desde el nacimiento. Antes de la ovulación, cada ovocito contiene 46 cromosomas y se encuentra en un estado inmaduro. La maduración del ovocito comienza con la formación del folículo dominante y culmina en el momento de la ovulación.
Al momento de la ovulación, el ovocito alcanza la metafase II de la meiosis, preparándose completamente para la fecundación y conteniendo 23 cromosomas. Esta dotación cromosómica es esencial para asegurar la correcta composición genética del futuro bebé. En los programas de FIV, la estimulación ovárica controlada tiene como objetivo principal inducir el crecimiento folicular para obtener ovocitos en esta fase madura, destinados a la crioconservación o fertilización directa.
De forma natural, la ovulación en la mujer suele ocurrir alrededor del día 14 o 15 del ciclo menstrual, momento en el cual los ovocitos alcanzan su madurez. Un ovocito maduro se encuentra típicamente dentro de un folículo con un diámetro de 18 a 22 mm. Por esta razón, la punción folicular se programa cuando la mayoría de los folículos han alcanzado este tamaño óptimo. Los embriólogos evalúan la madurez y calidad de los ovocitos entre 2 y 4 horas después de la punción. En casos donde se recuperan ovocitos inmaduros, el laboratorio puede intentar su maduración in vitro; sin embargo, la probabilidad de obtener embriones cromosómicamente sanos a partir de estos ovocitos es considerablemente menor que con ovocitos que ya se encuentran en etapa MII.
Causas de la Obtención de Ovocitos Inmaduros
Existen diversas razones por las cuales se pueden obtener ovocitos inmaduros durante la punción folicular:
- Insuficiencia en la estimulación de la hormona luteinizante (LH): Esta hormona es crucial para la maduración final del ovocito.
- Desincronización en el tamaño folicular: Incompatibilidad en el tamaño de los folículos en el momento de administrar el desencadenante de la ovulación.
- Factores genéticos: Mutaciones en los genes de los receptores de LH o FSH.
- Uso de ciertos medicamentos: Algunos fármacos pueden disminuir la sensibilidad a la LH.
Todos estos factores pueden contribuir a que, en el día de la punción, una parte de los ovocitos no haya completado su proceso de maduración.
Consecuencias de Fertilizar un Ovocito Inmaduro
La fertilización de un ovocito inmaduro es, en la práctica, imposible y potencialmente peligrosa. Para una concepción exitosa, tanto el ovocito como el espermatozoide deben aportar 23 cromosomas cada uno. Un ovocito inmaduro conserva el conjunto completo de 46 cromosomas, lo que impide la formación de un genoma diploide correcto en el embrión, resultando en la imposibilidad de desarrollo de un embrión viable.
Estrategias ante la Obtención de Ovocitos Inmaduros en Ciclos Previos de FIV
Si en un ciclo de FIV anterior se obtuvo una proporción elevada de ovocitos inmaduros, es fundamental realizar un examen exhaustivo y ajustar el protocolo de tratamiento. Las medidas a considerar incluyen:
- Análisis detallado del tamaño folicular y el momento de administración del desencadenante de la ovulación.
- Evaluación del diámetro de los folículos principales en el día del desencadenante.
- Realización de pruebas genéticas para detectar anomalías en los receptores hormonales.
- Selección del desencadenante de la ovulación más adecuado o el uso de un protocolo de doble desencadenante para mejorar la respuesta.
- Ajuste del intervalo de tiempo entre la administración del desencadenante y la punción folicular.
Estas modificaciones requieren una gran experiencia por parte del ginecólogo reproductólogo y tienen el potencial de aumentar significativamente la proporción de ovocitos maduros en ciclos subsecuentes, mejorando así las posibilidades de obtener embriones sanos y, en última instancia, lograr un embarazo.
FIV y la Particularidad de los Protocolos
FIV Estándar
En el protocolo estándar de FIV, el objetivo primordial es maximizar la obtención de ovocitos maduros, ya que su cantidad y calidad influyen directamente en los resultados del tratamiento.
FIV con Donación de Ovocitos
En programas de donación de ovocitos, estos son seleccionados rigurosamente bajo criterios de madurez y calidad, excluyendo los inmaduros para garantizar una alta tasa de fertilización.
FIV con Doble Donación
Cuando se emplean tanto ovocitos como espermatozoides de donantes, las probabilidades de éxito son elevadas, pero la verificación de la madurez de los ovocitos sigue siendo un paso crucial en la preparación del procedimiento.
En resumen, los ovocitos inmaduros representan una causa frecuente de disminución en la eficacia de los programas de FIV. Las mujeres nacen con un número determinado de ovocitos inmaduros en sus ovarios, y aunque la edad es un factor importante en la calidad ovárica, la respuesta a la medicación de estimulación ovárica, influenciada por la reserva ovárica, juega un papel determinante.
FOLICULOGÉNESIS ¿Qué son los FOLÍCULOS OVÁRICOS? | EMBRIOLOGÍA HUMANA 📚
Maduración In Vitro (MIV) de Ovocitos
La maduración in vitro (MIV) es una técnica de reproducción asistida que permite madurar ovocitos inmaduros en el laboratorio hasta alcanzar el estado de madurez necesario para la fecundación, conocido como metafase II (MII). Este proceso implica la incubación de los ovocitos inmaduros en un medio de cultivo con condiciones controladas durante un periodo de 24 a 48 horas.
Una diferencia clave de la MIV respecto a la FIV convencional es que, en la MIV, la paciente recibe poca o ninguna estimulación hormonal previa, o incluso ninguna estimulación ovárica. Esto minimiza el riesgo de síndrome de hiperestimulación ovárica (SHO), una complicación potencial de la estimulación ovárica.
Indicaciones de la MIV
La MIV se presenta como una alternativa valiosa en diversas situaciones:
- Mujeres con Síndrome de Ovario Poliquístico (SOP): Estas pacientes tienen un alto recuento folicular y un mayor riesgo de SHO con FIV convencional. La MIV, al no requerir estimulación, se ajusta bien a sus necesidades.
- Pacientes con alto riesgo de SHO o que desean evitar la estimulación ovárica: La MIV reduce las molestias, costes y el riesgo asociado a la medicación hormonal.
- Preservación de la fertilidad: Es una opción para pacientes con tumores hormonodependientes o que necesitan iniciar tratamientos oncológicos rápidamente. La MIV puede aumentar el número de ovocitos disponibles para preservar.
- Pacientes con baja respuesta a la estimulación ovárica: En casos de baja respuesta donde los ciclos de FIV convencionales pueden ser cancelados, la MIV de ovocitos inmaduros ("rescate") puede ser una alternativa para aumentar el número de embriones potenciales.
Ventajas de la MIV
- Reducción del riesgo de síndrome de hiperestimulación ovárica.
- Menores costes, molestias y tiempo de tratamiento.
- Alternativa para la preservación de la fertilidad cuando la estimulación ovárica está contraindicada.
Inconvenientes y Limitaciones de la MIV
A pesar de sus ventajas, la MIV aún presenta limitaciones y no se ha generalizado:
- Se considera una técnica experimental en muchos contextos.
- Los resultados en términos de tasas de embarazo y gestación evolutiva son, en general, inferiores a los de la FIV convencional.
- La evidencia científica que respalda su uso generalizado frente a la FIV convencional en pacientes con SOP aún es limitada.
- Los resultados obstétricos y perinatales, aunque generalmente buenos, se basan en un número limitado de estudios con seguimiento a corto plazo.
Por estas razones, la MIV no suele ser una alternativa a la FIV convencional cuando la estimulación ovárica está médicamente indicada y no presenta contraindicaciones.
Perspectivas Históricas y Evolución de la MIV
La primera maduración in vitro de ovocitos se logró en conejos en 1935, demostrando la capacidad de los ovocitos para continuar su maduración fuera del folículo y ser fecundados. En humanos, los primeros experimentos se iniciaron en 1965, publicándose el primer embarazo derivado de ovocitos madurados in vitro en 1991. Inicialmente, la aplicación de la MIV se centró en "rescatar" ovocitos inmaduros de ciclos de FIV, pero investigaciones posteriores revelaron que los ovocitos inmaduros de ciclos no estimulados también conservaban la competencia para madurar y dar lugar a embriones viables.
La MIV ha encontrado aplicaciones en pacientes con ovarios poliquísticos (PCO/PCOS), pacientes oncológicas para preservación de la fertilidad, y como estrategia para optimizar el rendimiento en pacientes con baja respuesta ovárica. La técnica ha evolucionado, incluyendo mejoras en los medios de cultivo y en las técnicas de criopreservación, como la vitrificación, que ha aumentado la eficiencia de los ovocitos MIV vitrificados.
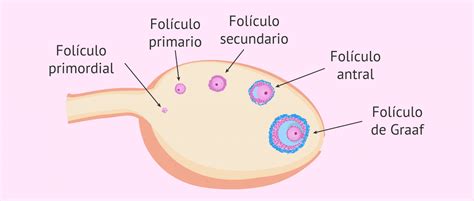
El Proceso de Ovogénesis y la Foliculogénesis
La ovogénesis es el complejo proceso de formación y maduración de los gametos femeninos en los ovarios. Este proceso, que comienza en la vida embrionaria, implica etapas de maduración nuclear y citoplasmática. En los tratamientos de reproducción asistida, se busca obtener ovocitos en estadio de metafase II (MII), aptos para la fecundación. La foliculogénesis es el desarrollo de los folículos ováricos, desde primordiales hasta preovulatorios, un proceso crucial para la adquisición de la competencia del ovocito.
La foliculogénesis está regulada por factores paracrinos y endocrinos. La interacción entre las células de la granulosa y el ovocito, mediada por señales intercelulares y uniones tipo gap junction, es fundamental. La acción de la LH desencadena la progresión del ovocito desde la vesícula germinal (VG) hasta metafase II (MII).
La Técnica de MIV en la Práctica Clínica
Los protocolos de MIV pueden variar, realizando el procedimiento sin estimulación ovárica exógena, con una estimulación mínima de FSH, o con la administración de hCG. La elección del protocolo depende de las características de la paciente, especialmente en casos de SOP, donde una estimulación suave puede mejorar los resultados.
La monitorización del ciclo de MIV considera el grosor endometrial, el tamaño folicular y los niveles de estradiol. Los criterios para la punción folicular se basan en alcanzar un tamaño folicular óptimo, generalmente entre 16 y 18 mm, indicativo de que el ovocito en su interior ha completado su maduración. La punción folicular se realiza mediante ultrasonido, aspirando el contenido de los folículos. La manipulación de los ovocitos inmaduros recuperados y su cultivo en medios específicos, a menudo suplementados con FSHr, hCG y suero autólogo, son pasos clave en el proceso de MIV.
La inseminación de los ovocitos maduros puede realizarse mediante fertilización in vitro convencional o microinyección intracitoplasmática de espermatozoides (ICSI). La elección entre ambas técnicas dependerá de la calidad del esperma y de las preferencias del laboratorio.
Criopreservación y MIV
La criopreservación de ovocitos inmaduros es un área de investigación activa. Inicialmente, se consideró la criopreservación de ovocitos en estadio de vesícula germinal (VG) debido a la aparente protección de la membrana nuclear. Sin embargo, estudios posteriores han indicado que la criopreservación de ovocitos en estadio MII, especialmente mediante vitrificación, ofrece mejores tasas de supervivencia, maduración post-descongelación y calidad embrionaria.
La vitrificación ha revolucionado la criopreservación de ovocitos, incluyendo aquellos que han pasado por un proceso de MIV. Los nacimientos reportados a partir de ovocitos vitrificados post-MIV sugieren la viabilidad de esta estrategia, aunque la eficiencia y los resultados a largo plazo continúan siendo objeto de estudio.
Consideraciones sobre la MIV y Pacientes con SOP
Las mujeres con síndrome de ovarios poliquísticos (SOP) son candidatas potenciales para la MIV debido a su elevado recuento folicular y el mayor riesgo de SHO con estimulación ovárica convencional. La MIV, al evitar o minimizar la estimulación hormonal, reduce este riesgo. Sin embargo, a pesar de la aparente idoneidad, la evidencia que respalda la MIV como opción preferente frente a la FIV convencional en pacientes con SOP aún no es concluyente, y las tasas de embarazo reportadas con MIV suelen ser inferiores.
Estadísticas y Resultados de la MIV
Los datos de registros de reproducción asistida, como los de la Sociedad Española de Fertilidad (SEF), muestran un número limitado de ciclos de MIV en comparación con la FIV/ICSI convencional. Las tasas de gestación y parto por transferencia de embriones en MIV son generalmente más bajas que en FIV/ICSI. Por ejemplo, en 2021, se reportaron 3 ciclos de transferencia de MIV con 1 gestación y 0 partos, frente a más de 18,000 transferencias en FIV/ICSI con más de 6,000 gestaciones y casi 5,000 partos.
Esta disparidad subraya la importancia de considerar la MIV como una técnica complementaria o alternativa en casos específicos, más que como un reemplazo generalizado de la FIV convencional, especialmente cuando la estimulación ovárica no está contraindicada.