La esquistosomiasis es una enfermedad parasitaria grave que afecta a millones de personas en todo el mundo, especialmente en países en vías de desarrollo. A pesar de los esfuerzos continuos, la erradicación completa de esta dolencia sigue siendo un desafío significativo. En este contexto, la investigación científica explora nuevas y prometedoras estrategias, incluyendo la manipulación genética para crear machos estériles, con el objetivo de interrumpir el ciclo de vida del parásito Schistosoma.
Comprendiendo la Esquistosomiasis
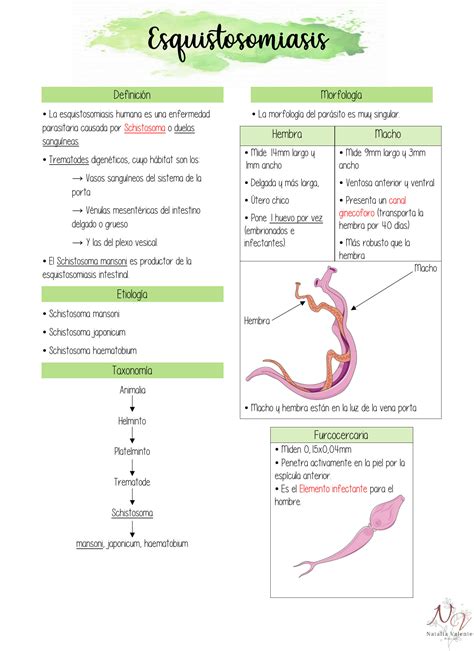
La esquistosomiasis, conocida comúnmente en Brasil como "barriga d’água", es una de las 17 enfermedades tropicales desatendidas (ETD) reconocidas por la Organización Mundial de la Salud (OMS). Afecta a aproximadamente 200 millones de personas en 74 países. La enfermedad es causada por duelas sanguíneas (trematodos) del género Schistosoma. La infección se adquiere cuando las personas entran en contacto con agua dulce infestada con las formas larvarias (cercarias) de estos parásitos sanguíneos. Los gusanos adultos microscópicos residen en las venas que drenan el tracto urinario y los intestinos, provocando deficiencias nutricionales, reacciones tisulares y, en ocasiones, daños que requieren intervención quirúrgica. Los efectos económicos y sanitarios de la esquistosomiasis son considerables, causando más discapacidad que muertes. En niños, puede manifestarse como anemia, retraso del crecimiento y problemas de aprendizaje, aunque estos efectos suelen ser reversibles con tratamiento. La esquistosomiasis crónica puede afectar la capacidad de trabajo y, en casos graves, ser mortal.
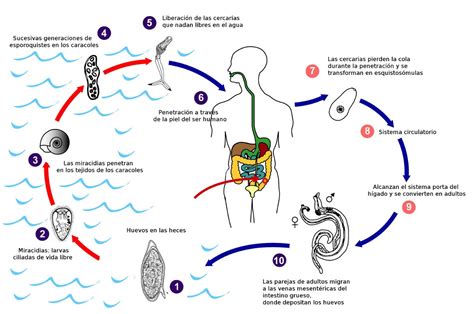
El ciclo de vida del parásito implica a un hospedador definitivo (humano) y un hospedador intermedio (caracoles de agua dulce). Una persona infectada elimina los huevos del gusano a través de sus excrementos. En contacto con el agua, los huevos eclosionan, liberando larvas que infectan a los caracoles. Después de un período de desarrollo, las larvas abandonan los caracoles como cercarias, que pueden penetrar la piel humana. Una vez en el torrente sanguíneo, las larvas pierden la cola, se convierten en esquistosómulos, maduran a gusanos adultos y migran a las venas del intestino o del tracto urinario, dependiendo de la especie. Los primeros síntomas suelen aparecer entre dos y seis semanas después de la infección. El diagnóstico se realiza mediante análisis de laboratorio de la materia fecal.
Avances en la Investigación de Control Parasitario
La investigación científica ha estado explorando diversas vías para combatir la esquistosomiasis. Un área de interés se centra en la comprensión de los mecanismos moleculares que sustentan la supervivencia del parásito. Investigadores del Instituto Butantan en São Paulo, Brasil, han descubierto que la supervivencia del gusano parásito depende de la expresión de un tipo específico de ARN: los ARN largos no codificantes (lncRNA). Estos ARN, que representan una gran proporción del ARN celular y que durante mucho tiempo pasaron desapercibidos, han demostrado ser esenciales para mantener la homeostasis en el parásito, lo que los convierte en posibles dianas terapéuticas.
Otro enfoque prometedor involucra la manipulación genética. En Burkina Faso, se ha llevado a cabo un experimento pionero para combatir la malaria, una enfermedad transmitida por mosquitos, mediante la liberación de mosquitos genéticamente modificados. Esta técnica, conocida como impulso genético, consiste en introducir un gen "defectuoso" que se transmite a la descendencia de los mosquitos, provocando esterilidad. El objetivo es reducir drásticamente las poblaciones de mosquitos vectores de enfermedades.
Ingeniería Genética en 5 minutos | ¿Qué es la ingeniería genética? | Genética
Si bien este experimento se centró en la malaria, el principio de la manipulación genética para inducir esterilidad en machos podría, en teoría, aplicarse a otros parásitos, incluyendo el Schistosoma. La idea sería interrumpir la reproducción del parásito en su fase de gusanos adultos, impidiendo así la producción de huevos y la propagación de la enfermedad. La investigación en este campo busca identificar los genes o mecanismos clave para el desarrollo y la reproducción de los gusanos, con el fin de diseñar estrategias de intervención genética.
El Papel de la Respuesta Inmunitaria y las Células Reguladoras
La interacción entre el parásito y el sistema inmunitario del huésped es compleja y juega un papel crucial en el desarrollo de la enfermedad y en la respuesta a posibles tratamientos o vacunas. Los parásitos, al ser entidades vivas que extraen nutrientes del hospedador, deben establecer una relación de equilibrio con las defensas del huésped para sobrevivir. La desregulación del sistema inmunitario, que puede llevar a respuestas anormales de tipo Th1 o Th2, está asociada con diversas enfermedades humanas.
Estudios recientes sugieren que la exposición a parásitos helmínticos puede modular la respuesta inmunitaria, a menudo atenuando la inflamación excesiva. Por ejemplo, se ha demostrado que la exposición a huevos de Schistosoma mansoni puede atenuar la colitis inducida en modelos animales, protegiendo contra la inflamación. Este efecto se relaciona con una disminución de la producción de citoquinas proinflamatorias como el IFN-gamma y un aumento de citoquinas antiinflamatorias como la IL-4 y la IL-10.
Las células T reguladoras (Tregs), incluyendo subconjuntos como las células Th3 y Tr1, juegan un papel fundamental en la supresión de respuestas inmunes exageradas. Estas células, que a menudo expresan marcadores como CD25 y secretan citoquinas inmunosupresoras como IL-10 y TGF-beta, son vitales para mantener la tolerancia y prevenir la autoinmunidad y las respuestas alérgicas. La investigación explora si las preparaciones de parásitos helmínticos pueden alterar la actividad de las células T reguladoras para tratar enfermedades relacionadas con desequilibrios Th1/Th2.
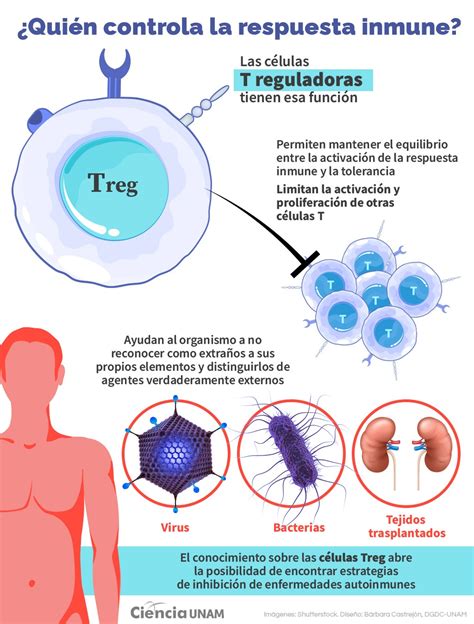
La comprensión de cómo los parásitos modulan la respuesta inmunitaria del huésped, y el rol de las células T reguladoras en este proceso, podría abrir nuevas vías para el desarrollo de terapias y vacunas. La identificación de biomarcadores internos o de superficie celular asociados a la actividad de las células T reguladoras, como Scurfina, Smad7, Gata 3, Tbet, CTLA-4, CD25, IL-10 o TGF-beta, es crucial para monitorizar la eficacia de tratamientos que buscan reequilibrar la respuesta inmune.
Desarrollo de Vacunas y Diagnóstico
El desarrollo de una vacuna eficaz contra la esquistosomiasis ha sido un objetivo a largo plazo. Investigadores utilizan técnicas como el phage display para identificar proteínas del parásito que son reconocidas por el sistema inmunitario del huésped. Este método permite analizar simultáneamente miles de proteínas del parásito y determinar cuáles son dianas de los anticuerpos generados tras la infección o reinfección.
Un estudio reciente utilizó el phage display para construir una "biblioteca" de péptidos que representan todas las proteínas conocidas del Schistosoma. Al analizar los anticuerpos de macacos rhesus infectados, se identificaron epítopos de proteínas extracelulares y, en etapas posteriores, proteínas intracelulares liberadas por la muerte del gusano. Estos péptidos se analizaron mediante bioinformática para identificar potenciales candidatos vacunales. Los resultados de estos estudios mejoran la comprensión de las respuestas inmunitarias y abren perspectivas prometedoras para el desarrollo de vacunas.
Paralelamente, se están desarrollando herramientas diagnósticas más precisas y accesibles. La proteína recombinante Sh-TSP-2 ha sido evaluada como método para diagnosticar la esquistosomiasis urogenital importada, especialmente en poblaciones migrantes. La esquistosomiasis genital masculina, causada por huevos del parásito Schistosoma haematobium en los órganos genitales, presenta desafíos diagnósticos debido a la baja sensibilidad y falta de estandarización de las técnicas convencionales. La investigación apunta hacia el desarrollo de pruebas moleculares isotérmicas, como el test Sh-RPA, que no requieren cadena de frío y son más accesibles en zonas endémicas.
Perspectivas Futuras
La erradicación de la esquistosomiasis requiere un enfoque multifacético que combine estrategias de control, tratamiento y prevención. La investigación en manipulación genética, el desarrollo de vacunas, la mejora de las herramientas diagnósticas y una mejor comprensión de la inmunología del parásito son pilares fundamentales. La OMS continúa reforzando los programas nacionales y los equipos de salud para abordar esta enfermedad desatendida. El futuro de la lucha contra la esquistosomiasis reside en la integración de estos avances científicos y tecnológicos para lograr una intervención más efectiva y, en última instancia, la erradicación de la enfermedad.
tags: #erradicar #esquistosomiasis #manipulacion #genetica #machos #infertiles