La preservación de embriones mediante congelación es un pilar fundamental en los tratamientos de reproducción asistida. A menudo, los pacientes tienen ideas preconcebidas sobre cómo se almacenan los embriones, imaginando desde armarios llenos hasta habitaciones similares a neveras. Sin embargo, la realidad es que los embriones congelados son microscópicos y ocupan muy poco espacio. Viven en tanques especiales con compartimentos donde se agrupan por "familias" de un color determinado, dentro de cubiletes de plástico. Cada cubilete contiene "pajuelas" de plástico blanco, donde se almacenan uno, dos o tres embriones. Estas pajuelas están etiquetadas con información relevante, incluyendo un código de color en una varilla interna que identifica a la familia de embriones.
Etapas de Congelación y Técnicas de Preservación
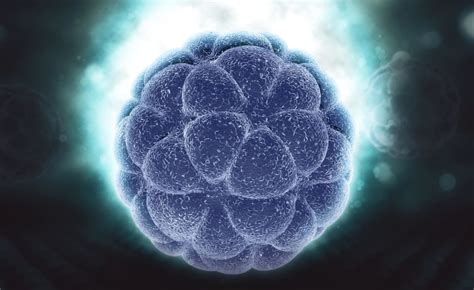
Los embriones pueden congelarse en diversas etapas de su desarrollo. Desde el día de la fecundación, cuando son una única célula, hasta cinco o seis días después, en el estadio de blastocisto, ya compuestos por numerosas células. Durante los primeros siete días de vida, los embriones se desarrollan dentro de la membrana externa del ovocito, de manera similar a como los pollitos crecen dentro de la cáscara de un huevo. Este proceso se denomina eclosión del blastocisto, tras lo cual el embrión está listo para implantarse en el útero.
El proceso tradicional de congelación de embriones dura varias horas. Implica sumergir los embriones en una solución crioprotectora para prevenir la formación de cristales de hielo y su posterior aspiración dentro de las pajuelas. Luego, estas pajuelas se someten a un descenso progresivo de temperatura en una máquina especial hasta alcanzar los -196 grados centígrados.
Actualmente, se prefiere la técnica de vitrificación, desarrollada inicialmente para superar las dificultades de la congelación tradicional con ovocitos. La vitrificación es más eficaz porque, a diferencia de la congelación lenta que puede dañar estructuras delicadas por la formación de cristales de hielo, la vitrificación solidifica el agua de forma casi instantánea, evitando dicho daño. Esta técnica es especialmente importante para ovocitos, que tienen un alto contenido de agua, pero también se aplica a embriones.
Longevidad de los Embriones Congelados
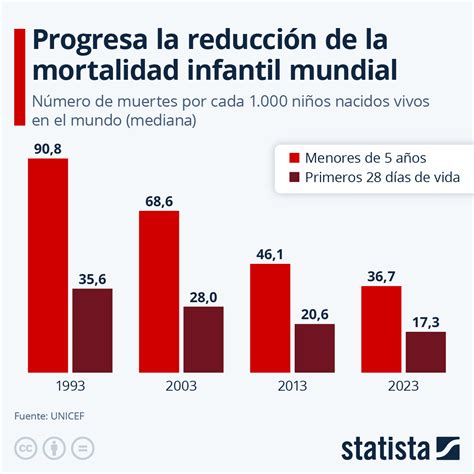
No se conoce un límite de tiempo definitivo para la viabilidad de los embriones en estado congelado. Un caso notable presentado en 2006 en el Congreso de la Sociedad Española de Fertilidad documentó el nacimiento de un niño que había permanecido congelado durante 13 años y medio, dentro de un programa de adopción de embriones. Este hito subraya la durabilidad de la criopreservación.
Cribado Genético Preimplantacional (PGS/PGT-A)
Durante un tratamiento de reproducción asistida, la selección del embrión más adecuado para la transferencia al útero es crucial. En este contexto, el cribado genético preimplantacional (PGS), también conocido como PGT-A (Test Genético Preimplantacional para Aneuploidias) o CCS (Comprehensive Chromosome Screening), juega un papel importante. Esta técnica permite determinar si un embrión posee el número correcto de cromosomas, es decir, si es cromosómicamente normal.
Para realizar el análisis genético, es necesario obtener una muestra de células del embrión mediante un proceso llamado biopsia embrionaria, sin que esto perjudique su desarrollo o implantación.
Evolución de la Técnica de Biopsia
Inicialmente, la biopsia se realizaba en el día 3 de cultivo embrionario, cuando los embriones tenían entre 6 y 8 células. El objetivo era minimizar cualquier efecto adverso en su desarrollo posterior. Sin embargo, la técnica actual de biopsia se realiza en la fase de blastocisto, que se alcanza a partir del día 5 de cultivo. La biopsia en fase de blastocisto se considera más segura y proporciona resultados más fiables que la realizada en día 3.
Biopsia de Blastómera en Día 3
En el tercer día de desarrollo embrionario, los embriones de buena calidad suelen presentar 8 células. Si la biopsia se realiza en este momento, se extrae una sola blastómera, o como máximo dos, para no comprometer la viabilidad del embrión. Para acceder a la blastómera, se realiza una pequeña abertura en la zona pelúcida del embrión, ya sea con pulsos de láser o con agentes químicos como el ácido Tyrodes. Tras la extracción de la blastómera, el embrión puede continuar su desarrollo hasta blastocisto mientras se esperan los resultados genéticos, o ser vitrificado para una transferencia posterior.
Biopsia de Trofoectodermo en Día 5 (Blastocisto)
Al quinto día de desarrollo, el embrión alcanza la fase de blastocisto, una estructura más compleja con tres partes diferenciadas: la masa celular interna (que dará lugar al feto), el blastocele (cavidad llena de líquido) y el trofoectodermo (capa externa que origina la placenta). La biopsia del trofoectodermo, la capa externa, permite extraer varias células, lo que resulta en un análisis genético más fiable y una mejor detección del mosaicismo (presencia de células con diferente dotación cromosómica). Además, la viabilidad del embrión se ve menos comprometida al extraer células de esta capa, que no forman parte del futuro feto.
Es crucial realizar la biopsia en el trofoectodermo, alejada de la masa celular interna, y preferiblemente con pulsos cortos de láser para evitar dañar el blastocisto, cuya zona pelúcida se ha adelgazado. Tras la biopsia de trofoectodermo, los embriones se vitrifican para ser transferidos en un ciclo posterior, ya que los resultados del análisis genético requieren varios días.
Técnicas de Análisis Genético
Existen diversas técnicas para el análisis genético de los embriones:
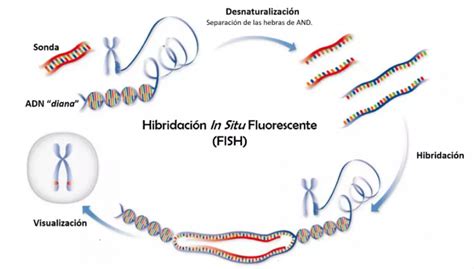
- Estudio FISH (Hibridación In Situ Fluorescente): Técnica tradicional que analiza regiones específicas de 9 cromosomas (13, 15, 16, 17, 18, 21, 22, X e Y). Al ser un análisis parcial, se considera incompleto y está siendo reemplazado por métodos más avanzados.
- Arrays de CGH (Hibridación Genómica Comparada): Permite un cribado cromosómico completo (CCS), analizando los 23 pares de cromosomas. Identifica pérdidas o ganancias de material genético, pero no detecta alteraciones en la ubicación de fragmentos cromosómicos (inversiones o traslocaciones).
- Reacción en Cadena de la Polimerasa (PCR): Técnica utilizada para el diagnóstico de enfermedades monogénicas. Permite amplificar secuencias de ADN específicas para identificar mutaciones concretas en un gen.
- Secuenciación Masiva (NGS - Next-Generation Sequencing): La técnica más avanzada y resolutiva. Permite analizar los 23 pares de cromosomas con alta resolución, estudiar simultáneamente más de 500 genes asociados a enfermedades hereditarias, y analizar aneuploidias y enfermedades monogénicas de forma conjunta o separada. Ofrece resultados más rápidos y un coste más asequible.
Diagnóstico Genético Preimplantacional (DGP) para Enfermedades Monogénicas
El DGP se utiliza también para detectar enfermedades monogénicas, causadas por mutaciones en un solo gen, como la fibrosis quística o la hemofilia. Antes de realizar el DGP, se identifica la mutación específica en los padres a través de un estudio de informatividad. Una vez localizada la mutación y determinado el tipo de herencia, se aplican herramientas genéticas como la PCR o la secuenciación masiva para analizar los embriones.
Transferencia de Embriones
Tras obtener los resultados del análisis genético, los embriones genéticamente sanos son transferidos al útero materno o vitrificados para futuros intentos. Los embriones con alteraciones genéticas, incluso si presentan buena morfología, son descartados. Si los embriones fueron vitrificados, se descongelan y se transfieren en un ciclo posterior, tras una preparación endometrial con estrógenos y progesterona. En casos donde hay varios embriones sanos, se selecciona el de mejor calidad morfocinética para maximizar la probabilidad de implantación y embarazo.
Transferencia en Fresco vs. Ciclo Diferido
La transferencia embrionaria puede realizarse en fresco (en el mismo ciclo de estimulación ovárica) o en ciclo diferido (en un ciclo posterior, tras la vitrificación de los embriones). Históricamente, se creía que las transferencias en fresco eran más eficaces, pero los avances en las técnicas de congelación lenta y, sobre todo, la vitrificación han demostrado que los ciclos diferidos con embriones vitrificados pueden ofrecer tasas de embarazo comparables o incluso superiores.
La transferencia en ciclo diferido está indicada en varias situaciones:
- Cuando la elevación de los niveles de progesterona el día de la administración de Ovitrelle podría afectar negativamente la implantación (niveles > 1 ng/ml), indicando una posible asincronía entre el endometrio y el embrión.
- En ciclos de acumulación de embriones para realizar un Test Genético Preimplantacional (PGT).
- Casos de abortos de repetición o fallo de implantación.
- Ciclos en los que se realizan estudios de receptividad endometrial previos a la transferencia.
La preparación del endometrio en ciclos diferidos se realiza con fármacos (estrógenos) para simular el ciclo natural. Estudios recientes sugieren que las tasas de embarazo pueden ser mayores con la transferencia de embriones vitrificados en comparación con embriones en fresco.
Adopción de Embriones
La adopción de embriones es un tratamiento en el que parejas que han logrado un embarazo mediante FIV donan sus embriones sobrantes a otras parejas o mujeres que los necesitan. Los embriones donados provienen de parejas que han pasado por los mismos requisitos y controles que los donantes de óvulos o esperma.
Comparativa de Transferencia en Día 3 vs. Blastocisto
La decisión sobre el estadio de desarrollo óptimo para la transferencia embrionaria (día 3 o blastocisto) es un tema de debate científico con el objetivo de mejorar las tasas de embarazo y de recién nacidos vivos. La transferencia en estadio de blastocisto (día 5 o 6) generalmente se asocia con mayores tasas de embarazo, implantación y parto en comparación con la transferencia en día 3.
Las ventajas de la transferencia en blastocisto incluyen:
- Mayor tasa de embarazo y de recién nacidos vivos.
- Permite una selección embrionaria más rigurosa, ya que solo los embriones con mayor potencial de desarrollo alcanzan esta fase.
- Menor número de embriones a transferir, lo que reduce el riesgo de embarazos múltiples y sus complicaciones asociadas.
- Se ha observado una disminución del porcentaje de abortos, posiblemente debido a una mejor selección del embrión y a una mayor sincronía con la receptividad endometrial.
Sin embargo, existen consideraciones importantes:
- No todos los embriones alcanzan la fase de blastocisto en cultivo in vitro (entre el 40% y el 60% de los ovocitos fecundados).
- La evaluación morfológica de los embriones es subjetiva, y un embrión morfológicamente normal en día 3 puede ser cromosómicamente anormal. La activación del genoma embrionario en la fase de blastocisto permite una selección más precisa.
- En algunos casos, es preferible la transferencia en día 3 si no se dispone de suficientes embriones de buena calidad para cultivar hasta blastocisto o si existe riesgo de cancelación de la transferencia por bloqueo del desarrollo.
Factores que Influyen en la Transferencia
La decisión sobre cuándo transferir embriones (fresco o congelado, día 3 o blastocisto) puede verse influenciada por varios factores:
- Edad materna: En pacientes menores de 35 años con embriones de buena calidad, la transferencia en blastocisto puede mejorar las tasas.
- Niveles de estradiol y progesterona: Niveles elevados de estradiol o progesterona en ciertos momentos del ciclo pueden afectar la receptividad endometrial y la tasa de embarazo, haciendo más recomendable la transferencia en ciclo diferido.
- Historial de la paciente: Antecedentes de abortos recurrentes, fallos de implantación o estudios de receptividad endometrial pueden influir en la estrategia de transferencia.
Preguntas Frecuentes
¿Qué probabilidad hay de que no queden embriones después del PGT?
La probabilidad de no obtener embriones sanos tras un PGT depende de varios factores, incluyendo la edad materna, la reserva ovárica y la calidad de los embriones. Cuantos más embriones disponibles para el análisis, mayores son las posibilidades de obtener embriones viables. La edad materna avanzada, en particular, puede afectar el número y la calidad de los ovocitos y embriones resultantes.
¿Cuántos embriones se transfieren después de hacer un DGP?
Generalmente, se recomienda la transferencia de un solo embrión, especialmente en casos de edad materna avanzada o patologías genéticas graves, para evitar el riesgo de embarazos múltiples. El número de embriones a transferir se basa en la calidad del embrión, su estadio de desarrollo y las características individuales de la paciente.
¿En qué tipo de casos se está utilizando el DGP?
El DGP se utiliza principalmente en casos de edad materna avanzada (para cribado de aneuploidias), parejas con antecedentes de enfermedades genéticas graves (fibrosis quística, distrofia miotónica, etc.), pacientes con abortos recurrentes y factor masculino severo.
¿Es lo mismo DGP y PGT?
PGT es el término general para los estudios genéticos preimplantacionales. Incluye el PGT-A (cribado de aneuploidias), PGT-M (diagnóstico de enfermedades monogénicas) y PGT-SR (diagnóstico de anomalías estructurales cromosómicas).
tags: #embriones #congelados #a #posteriori #pgs