El bloqueo embrionario es un término utilizado para describir la incapacidad de los embriones para desarrollarse hasta la fase de blastocisto. Normalmente, estos embriones detienen su desarrollo en el día +3 o +4, permaneciendo en el estadio de mórula o células.
Aproximadamente entre el 50% y el 60% de los embriones tienen la capacidad de alcanzar la etapa de blastocisto. Aquellos que no lo consiguen sufren el denominado arresto embrionario. Diversos factores pueden ser la causa de este bloqueo, incluyendo una mala calidad ovocitaria y seminal. Por ejemplo, se ha observado que la fragmentación del ADN espermático tiene un efecto negativo en el desarrollo embrionario, provocando una evolución más lenta de los embriones y relacionándose negativamente con el arresto embrionario.
Otro factor crucial a considerar es la edad del ovocito. Se sabe que la presencia de anomalías cromosómicas en el ovocito aumenta con la edad de la mujer, lo que influye en la carga genética del embrión y, por ende, en su desarrollo. Además, diversos estudios demuestran que una de las principales causas del arresto embrionario es la presencia de anomalías cromosómicas en las células del embrión. Concretamente, se ha observado que casi el 70% de los embriones que no forman blastocisto presentan anomalías cromosómicas.
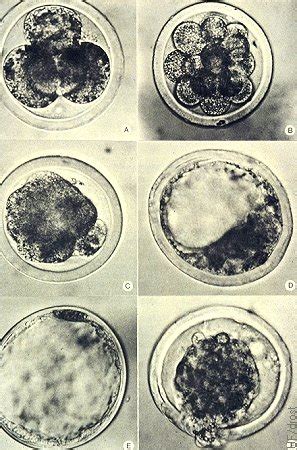
Parámetros Morfológicos para la Selección Embrionaria
Los avances tecnológicos han permitido el cultivo de embriones hasta el día +6 del desarrollo embrionario. Este cultivo prolongado permite seleccionar los embriones con mayor capacidad para formar blastocisto en los días +5/+6, facilitando así una mejor selección embrionaria.
Existen ciertos parámetros morfológicos que permiten seleccionar los embriones con mejor pronóstico para la implantación:
Número de Células y Simetría
Se considera un embrión de mayor calidad aquel que presenta un número par de células simétricas, o un número impar de células con una asimetría muy leve. El número de células también es importante según el día de desarrollo: de 2 a 5 células en día +2, y de 6 a 10 en día +3.
Fragmentación
La formación de fragmentos en el embrión puede dificultar la comunicación celular entre los blastómeros, lo que a su vez puede obstaculizar la formación de la mórula (alrededor del día 4) y posteriormente del blastocisto (a partir del día 5). Alikani et al. (1999) clasificaron los embriones según el porcentaje y patrón de distribución de los fragmentos:
- Fragmentación tipo I: menos del 5%, asociada a un blastómero o proveniente de la fragmentación de los corpúsculos polares.
- Fragmentación tipo II: fragmentos localizados cerca del espacio perivitelino, de tamaño similar. Corresponden a la fragmentación parcial o completa de un blastómero.
- Fragmentación tipo III: fragmentos pequeños distribuidos por todo el embrión, entre o periféricamente a los blastómeros.
- Fragmentación tipo IV: fragmentos grandes, similares a blastómeros, distribuidos por todo el embrión y asociados a blastómeros irregulares.
- Fragmentación tipo V: fragmentos necróticos, granulares, asociados a blastómeros con citoplasma contraído.
Multinucleación
Se refiere a la presencia de más de un núcleo por blastómero. Es importante distinguir entre:
- Binucleación: debida a una división nuclear sin citocinesis.
- Multinucleación: presencia de más de 2 núcleos por blastómero.
- Micronucleación: presencia de micronúcleos.
Tanto la multinucleación como la micronucleación se relacionan con una menor tasa de implantación y un menor desarrollo embrionario hasta blastocisto.
Características del Citoplasma
El citoplasma puede presentar diversas características que influyen en la calidad embrionaria:
- Granuloso: ligado a una mayor actividad transcripcional.
- Vesiculado: asociado a procesos degenerativos en las blastómeras.
- Presencia de halo citoplasmático: el citoplasma se encuentra contraído, relacionado con una menor tasa de desarrollo hasta blastocisto.
- Vacuolas: su importancia depende de la cantidad y tamaño; pueden bloquear el desarrollo.
Grado de Compactación
A partir del día +3 del desarrollo, se inicia la compactación celular, un indicativo de la activación del genoma propio del embrión. Un mayor grado de compactación se asocia con un mejor pronóstico. Durante este proceso, el embrión puede descartar blastómeros y fragmentos que no formarán parte del futuro blastocisto.
El Desarrollo Fetal y Mecanismos de Autocorrección
El desarrollo de un bebé humano es un proceso complejo que parte de dos células germinales, el óvulo y el espermatozoide, para formar un conjunto de células que crecen y se multiplican a través de diversas fases: cigoto, blastocisto, embrión y feto. Durante las primeras semanas, pueden surgir problemas que resulten en anomalías cromosómicas graves, algunas de las cuales pueden llevar a la interrupción del embarazo, mientras que otras son compatibles con la vida pero pueden causar enfermedades o síndromes cromosómicos.
A pesar de la complejidad, la mayoría de las veces el proceso culmina con el nacimiento de un bebé sano. Estudios recientes, como el realizado por Jan Tesarik, sugieren que esto puede deberse a la capacidad de los embriones para corregir anomalías cromosómicas durante su desarrollo. Se ha comprobado que la mayoría de embriones humanos contienen proporciones variables de células con anomalías cromosómicas, pero la frecuencia de estas células disminuye durante la evolución embrionaria, lo que sugiere la existencia de un mecanismo de autocorrección.
El doctor Tesarik explica que estas anomalías son más habituales en mujeres de mayor edad debido al aumento de errores en los ovocitos. Sin embargo, estos errores también pueden ocurrir en las primeras divisiones celulares o ser aportados por los espermatozoides. Muchas de las células anormales contienen dos o más núcleos (multinucleación). Aunque muchas clínicas evitan la transferencia de embriones con células multinucleadas, estudios recientes indican que estos embriones pueden dar lugar a embarazos y nacimientos similares a los de embriones normales, aunque con una probabilidad ligeramente menor. Esto podría deberse a que las células afectadas por anomalías cromosómicas se autoexcluyen del desarrollo futuro, mientras que las células sanas continúan, dando lugar a un feto normal.
Tesarik se basa en otros trabajos, como uno japonés de 2015, que demostró que los embriones con células multinucleadas 2-3 días después de la fecundación tenían menor probabilidad de llegar a blastocisto. Sin embargo, aquellos que alcanzaban esta etapa tenían la misma capacidad de implantarse y originar un embarazo normal. En la misma línea, un estudio canadiense afirma que los embriones inicialmente multinucleados que llegan a blastocisto no presentan una tasa de anomalías cromosómicas mayor que los embriones aparentemente normales desde el inicio.
Paralelismo con Células Precancerosas y Análisis de ADN
El mecanismo de autocorrección de los embriones es similar al que utiliza el organismo adulto para eliminar errores cromosómicos en la multiplicación celular que podrían dar lugar a células cancerosas. El organismo cuenta con procesos, como la parada de la división celular, caracterizada por la aparición de múltiples núcleos antes de la desaparición de estas células, para prevenir la formación de tumores.
El estudio de estos paralelismos entre los mecanismos de autocorrección de los embriones y la eliminación de células adultas precancerosas podría, a medio y largo plazo, profundizar el conocimiento en ambos campos de investigación.
Uno de los problemas recurrentes en la fertilidad asistida son los fallos de implantación o los abortos espontáneos. Un nuevo estudio de Tesarik permite detectar anomalías de la impronta genética de los espermatozoides a partir del análisis del ADN libre liberado en la sangre y el semen testicular. Actualmente, existen métodos para determinar el origen celular del ADN libre y esclarecer el origen de patologías como el cáncer. En la producción de espermatozoides, se producen importantes cambios en determinados genes (evolución epigenética) que no alteran la secuencia genética pero sí la actividad génica. Estas anomalías de la impronta genética generalmente no impiden la fecundación, pero pueden causar fallos de implantación, abortos espontáneos o anomalías en los recién nacidos. El análisis de la impronta en el ADN libre testicular proporcionará información sobre estos riesgos.
Este análisis también puede ser útil en casos de azoospermia (ausencia de espermatozoides) debida a una producción defectuosa en los testículos. El análisis del ADN libre aislado del semen en hombres con azoospermia es un método no invasivo que puede predecir la capacidad de las espermátidas redondas para formar embriones normales y evaluar los efectos de tratamientos para mejorar su desarrollo.
Qué es la fragmentación del ADN espermático
Criterios de Selección Embrionaria en Programas de Reproducción Asistida
En el contexto de la reproducción asistida, especialmente en programas de gestación subrogada, la selección de embriones es un proceso crucial. Los futuros padres buscan garantizar las mejores condiciones para el futuro bebé, identificando los embriones con mayor potencial de éxito y reduciendo los riesgos de fracaso, aborto o complicaciones durante el embarazo.
Un embrión de "baja calidad" se refiere a aquel que, según los criterios establecidos, tiene una menor probabilidad de implantarse o de resultar en un embarazo exitoso. Los expertos evalúan el embrión en diferentes momentos del cultivo (normalmente hasta el día 3, 5 o 6) para observar su crecimiento. Se analizan aspectos como el número de células, la velocidad de división, la fragmentación (pequeños trozos de citoplasma desprendidos), la masa de células internas (que formará al bebé) y la capa externa (trofoectodermo, que dará origen a la placenta).
Un meta-análisis reciente ha destacado la importancia de la morfología del blastocisto para predecir su calidad, otorgando mayor peso al trofoectodermo que a la masa celular interna o al grado de expansión. En términos sencillos, un embrión con pocas células, alta fragmentación o estructura poco definida tiene menos probabilidades de implantarse.
Además de la apariencia, la composición genética del embrión es fundamental. Las alteraciones cromosómicas (aneuploidías) aumentan el riesgo de no implantación, de interrupción del embarazo o de malformaciones genéticas.
Evaluación Morfológica y Genética
El proceso de selección embrionaria incluye la evaluación de:
- Día 3: Se evalúa el número de células y la fragmentación. Se revisan también la simetría celular, la presencia de vacuolas o granulación.
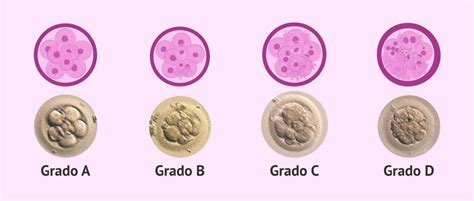
- Día 5-6 (Blastocisto): Se analiza el grado de expansión, la calidad de la masa celular interna (ICM) y del trofoectodermo (TE). Los estudios indican que los blastocistos con trofoectodermo de calidad "A" tienen mayores probabilidades de implantación exitosa.
En paralelo o como complemento, algunos laboratorios ofrecen pruebas genéticas preimplantacionales (PGT-A) para detectar alteraciones cromosómicas. Esta parte del proceso ayuda a descartar embriones con alto riesgo de fallo.
Una vez evaluados, los embriones se ordenan según su calidad (morfología + genética) para determinar el orden de transferencia, congelación o uso en gestación subrogada.
Factores que Influyen en la Calidad Embrionaria
Además de los criterios morfológicos y genéticos, otros factores influyen en la calidad embrionaria:
- Edad de la donante o de la mujer que aporta los óvulos: a mayor edad, mayor riesgo de alteraciones.
- Calidad del laboratorio y las condiciones de cultivo.
- Técnica de fertilización utilizada.
- Calidad del semen.
Es importante destacar que una calificación morfológica inferior no implica imposibilidad de implantación. Según varios estudios, embriones con esta calificación pueden dar lugar a un bebé sano. La calidad es un factor de éxito, no una condena.
La Selección Embrionaria en la Gestación Subrogada
El proceso de selección de embriones es especialmente relevante en la gestación subrogada, ya que optimiza el ciclo para los futuros padres y la gestante. Permite:
- Reducir ciclos fallidos.
- Realizar una transferencia más dirigida y segura.
- Aumentar la transparencia y la confianza de los futuros padres.
- Mejorar la planificación del ciclo y del presupuesto.
- Fomentar decisiones informadas.
Es recomendable preguntar sobre el sistema de clasificación de embriones utilizado (método de Gardner, guías ESHRE/ALPHA) y solicitar información clara sobre el número de embriones creados, su calidad y las razones de descarte.
Un ejemplo práctico es el caso de María y David, quienes, tras generar 6 embriones y realizar pruebas genéticas, optaron por transferir el embrión con morfología óptima y genética euploide, logrando una implantación exitosa y embarazo.
Criterios de Valoración y Desarrollo Embrionario
El desarrollo embrionario comienza con la fecundación, donde el cigoto se divide para formar la mórula (2-32 células) y luego el blastocisto (hasta 200 células). Este proceso puede interrumpirse, impidiendo el desarrollo a blastocisto. Habitualmente, entre el 40% y el 60% de los embriones alcanzan la etapa de blastocisto.
Los embriones de mejor calidad continúan su desarrollo, mientras que los de menor calidad se detienen. Sin embargo, un embrión de categoría C podría, en algunos casos, desarrollarse hasta blastocisto.
Las causas de la detención del desarrollo embrionario pueden ser múltiples. La calidad ovocitaria es crucial, ya que un óvulo de mala calidad puede interrumpir el proceso reproductivo. El componente masculino, como la teratospermia (espermatozoides con morfología anormal), también juega un papel importante.
Antes de la FIV, el embriólogo selecciona los gametos de mejor calidad. Una vez formado el blastocisto, el embrión está listo para implantarse en el útero materno.
La Multinucleación y su Relevancia
La multinucleación, la presencia de dos o más núcleos por blastómero, es un fenómeno interesante en el desarrollo embrionario. Aunque muchas células cromosómicamente anormales presentan multinucleación, los embriones pueden ser capaces de excluir estas células. Los resultados de estudios indican que las células multinucleadas detienen su desarrollo y su expresión genética queda bloqueada, mientras que las células normales continúan.
A pesar de estos hallazgos, muchos equipos de FIV siguen evitando la transferencia de embriones con células multinucleadas como primera opción, ya que aún queda investigación por realizar.
Cinética Embrionaria y Sistemas Time-Lapse
Desde el punto de vista morfológico, se consideran diversos elementos en la selección embrionaria. La cinética embrionaria, observada a través de sistemas TIME-LAPSE, ha supuesto un avance notable para monitorizar el desarrollo embrionario de forma continua.
Es importante no considerar los embriones de calidad intermedia como inapropiados o defectuosos. Aunque tengan menos probabilidades, también pueden dar lugar a un embarazo viable.
Qué es la fragmentación del ADN espermático
La fecundación in vitro y la transferencia embrionaria son procesos complejos donde la calidad de los embriones es un factor determinante para el éxito reproductivo.
tags: #embriones #celulas #irregulares