Los avances logrados en la segunda mitad del siglo XX en el diagnóstico, tratamiento y curación de las enfermedades malignas en niños y adolescentes representan uno de los hitos más significativos en oncología, comparable a otros logros de la pediatría.
Antes de la década de 1950, la curación de pacientes oncológicos era limitada, especialmente en tumores sólidos diagnosticados precozmente y extirpables quirúrgicamente. El retinoblastoma y el tumor de Wilms fueron los primeros tumores malignos susceptibles de curación mediante cirugía. La radioterapia, utilizada desde los años 30, comenzó a mostrar tasas de curación en el linfoma de Hodgkin en etapas iniciales en las décadas de 1950 y 1960. La quimioterapia, desarrollada en los años 50, mejoró las posibilidades de curación al actuar sistémicamente, siendo eficaz en cánceres hematológicos y reduciendo recaídas por metástasis microscópicas en tumores sólidos tratados solo con cirugía.
En Chile, la creación del Programa Infantil Nacional de Drogas Antineoplásicas (PINDA) en 1988 ha impulsado avances a nivel nacional, con más de 4.000 pacientes tratados hasta la fecha. Esto ha resultado en que, a principios del siglo XXI, las posibilidades de curación en oncología pediátrica superen el 65%, revirtiendo la tendencia previa a la década de 1960-1970.
La disminución de la mortalidad infantil debido a un control efectivo de enfermedades infecciosas y desnutrición, junto con avances en la atención neonatal, ha incrementado la relevancia del cáncer infantil, a pesar de su baja incidencia.
Diagnóstico del Cáncer Infantil
La incidencia del cáncer en la infancia es baja en comparación con patologías pediátricas comunes como enfermedades respiratorias e infecciosas. Esto puede llevar a que el pediatra general no considere el cáncer como primera sospecha diagnóstica, resultando en diagnósticos tardíos, como se evidencia en la comparación de evaluaciones del Programa PINDA.
En niños, a diferencia de los adultos, la mayoría de los tumores presentan una rápida progresión, incluyendo leucemias, linfomas (como el linfoma de Burkitt, uno de los de crecimiento más rápido), y neuroblastomas.
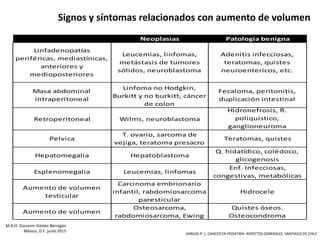
La diversidad sintomatológica de las neoplasias pediátricas, a menudo presentándose como un aumento de volumen, dificulta el diagnóstico temprano. Este síntoma puede confundirse con patologías infecciosas, inflamatorias o quísticas. La tabla 2 detalla síntomas y signos relacionados con aumentos de volumen en neoplasias y patologías benignas, destacando la importancia de considerar neoplasias ante cualquier aumento de volumen sin características inflamatorias.
Los avances en imagenología, como la ecotomografía y la tomografía computarizada (TAC), son cruciales para precisar la naturaleza, localización y extensión de las masas tumorales. La resonancia magnética (RNM) es fundamental para la evaluación de tumores óseos y del sistema nervioso central.
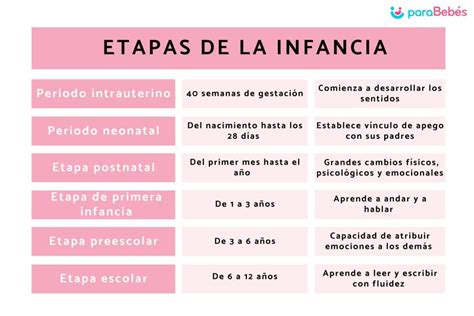
Además de los aumentos de volumen, existen síntomas y signos inespecíficos que pueden orientar hacia una neoplasia (Tabla 3). La edad de presentación varía según el tipo de tumor, como se ilustra en la Tabla 4, que muestra la mediana de edad para diversos tumores pediátricos según datos del PINDA.
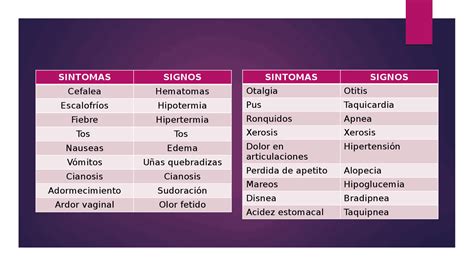
La Tabla 5 resume los signos y síntomas sospechosos según el diagnóstico, facilitando la orientación clínica inicial.
Ciertos síndromes genéticos se asocian con un riesgo significativamente mayor de desarrollar cáncer infantil. La Tabla 6 enumera síndromes genéticos asociados a cáncer, como la trisomía 21 (síndrome de Down) y la anemia de Fanconi.

Confirmación Diagnóstica y Estadificación
Ante la sospecha de una enfermedad maligna en un niño, el médico general o pediatra debe referirlo a un centro oncológico especializado para evitar demoras diagnósticas. El PINDA acredita 14 centros capacitados para diagnóstico y tratamiento en Chile.
La confirmación diagnóstica se basa en la biopsia quirúrgica, realizada por cirujanos con experiencia oncológica para minimizar complicaciones. Los estudios histopatológicos, incluyendo inmunohistoquímica, son esenciales para tumores sólidos. En patologías hematológicas, el mielograma y estudios de inmunotipificación por citometría de flujo son fundamentales. La precisión de estudios genéticos (cariogramas) y moleculares tiene relevancia pronóstica.
Antes de iniciar el tratamiento, es indispensable el estudio de etapificación o estadiaje, que determina la presencia de metástasis regionales o a distancia mediante estudios de imagenología. El tratamiento y pronóstico dependen de la etapa del tumor, generalmente clasificada en Etapa I (tumor primario), Etapa II (extensión local), Etapa III (extensión regional) y Etapa IV (metástasis a distancia).
Impacto Psicológico del Diagnóstico de Cáncer
A pesar de los avances, el cáncer infantil sigue siendo percibido como una enfermedad potencialmente fatal. El diagnóstico genera en la familia un estado inicial de shock y desesperanza, seguido por mecanismos de defensa como negación e ira. La adaptación ocurre al recibir información clara y establecer una relación de confianza con el equipo médico.
Es común la sobreprotección del niño enfermo, a menudo descuidando a los hermanos. El apoyo psicológico familiar es crucial para reforzar la resiliencia, disminuir la angustia y prevenir repercusiones negativas en la salud mental y la recuperación del niño.
En el niño, predominan los síntomas de ansiedad y temor al dolor y la separación. En adolescentes, pueden surgir rebeldía, rechazo, frustración por limitaciones y sentimientos depresivos.
Datos y Cifras del Cáncer Infantil
Se estima que anualmente unos 400.000 niños y adolescentes (0-19 años) padecen cáncer a nivel mundial. Las leucemias, tumores cerebrales y neuroblastomas son los más frecuentes en niños, mientras que en adolescentes predominan linfomas, cáncer de huesos y tiroides.
En países de ingresos altos, la tasa de curación supera el 80% gracias al acceso a atención integral. En países de ingresos bajos o medianos, la curación se alcanza en menos del 30% de los casos, debido a la falta de diagnóstico, diagnósticos erróneos o tardíos, dificultades de acceso, abandono del tratamiento, toxicidad y recidivas.
Solo el 29% de los países de ingresos bajos disponen habitualmente de medicamentos contra el cáncer, frente al 96% en países de ingresos altos.

Panorama General del Cáncer Infantil
El cáncer es una de las principales causas de mortalidad en la infancia y adolescencia, con tasas de supervivencia que varían drásticamente según el país de residencia. Mientras que en países de ingresos altos más del 80% de los niños se curan, en muchos países de ingresos bajos o medianos esta proporción no alcanza el 30%.
Los cánceres infantiles generalmente no son prevenibles ni detectables mediante tamizaje, pero la mayoría son curables con tratamientos como cirugía, radioterapia o quimioterapia con medicamentos genéricos.
Las bajas tasas de supervivencia en países de ingresos bajos o medianos se atribuyen a diagnósticos tardíos, imprecisos, falta de acceso a tratamiento, abandono, toxicidad y recidivas evitables. La mejora del acceso a la atención oncológica pediátrica, incluyendo tecnologías y medicamentos esenciales, es una intervención costo-efectiva que eleva las tasas de supervivencia.
La disponibilidad de sistemas de datos sobre cáncer infantil es fundamental para mejorar la calidad de la atención y orientar decisiones políticas.
Causas del Cáncer Infantil
El cáncer se origina por alteraciones genéticas en una célula que prolifera descontroladamente, invadiendo tejidos y provocando daños graves. A diferencia de los adultos, las causas de la mayoría de los cánceres infantiles son desconocidas, con poca relación con factores ambientales o de estilo de vida.
Algunas infecciones crónicas, como las asociadas al VIH, virus de Epstein-Barr o paludismo, son factores de riesgo de cáncer infantil, especialmente en países de ingresos bajos o medianos. La vacunación contra hepatitis B y virus del papiloma humano es importante para prevenir cánceres hepático y cervicouterino, respectivamente.
Alrededor del 10% de los niños con cáncer presentan una predisposición genética. La investigación continúa para comprender mejor estos factores.
Mejora del Desenlace Clínico en Cáncer Infantil
Dado que la prevención es limitada, el diagnóstico temprano y preciso, seguido de tratamiento eficaz y apoyo adaptado, son las estrategias clave para reducir la morbilidad y mejorar la evolución clínica.
Diagnóstico Precoz
La detección temprana del cáncer aumenta la probabilidad de respuesta al tratamiento, mejora la supervivencia, reduce el sufrimiento y permite terapias menos intensivas. El diagnóstico precoz se basa en:
- Conocimiento de síntomas por familias y personal de atención primaria.
- Evaluación clínica, diagnóstico y determinación del estadio rápidos y precisos.
- Inicio rápido del tratamiento.
Programas de diagnóstico temprano han demostrado éxito en diversos contextos, a menudo mediante colaboración entre gobiernos, sociedad civil y organizaciones no gubernamentales. Signos de alerta como fiebre persistente, cefalea intensa, dolores óseos y pérdida de peso deben ser reconocidos por familias y profesionales.
El tamizaje rara vez es útil para el cáncer infantil, excepto en casos de alto riesgo genético, como ciertas formas de retinoblastoma hereditario.
Tratamiento
Un diagnóstico correcto es imprescindible para prescribir el tratamiento adecuado, que puede incluir quimioterapia, cirugía y radioterapia. El tratamiento debe considerar el desarrollo físico y cognitivo del niño, así como su estado nutricional, requiriendo un equipo multidisciplinario especializado.
Persisten grandes desigualdades globales en el acceso a diagnósticos eficaces, medicamentos esenciales, servicios de anatomía patológica, hemoderivados, radioterapia, tecnologías, apoyo psicosocial y cuidados paliativos.
Cuando se brinda atención oncológica adecuada, más del 80% de los cánceres infantiles son curables. El tratamiento farmacológico a menudo utiliza medicamentos genéricos de bajo costo de la Lista Modelo OMS de Medicamentos Esenciales. El seguimiento permanente es necesario para detectar recidivas y efectos a largo plazo.
Cuidados Paliativos
La asistencia paliativa alivia los síntomas del cáncer y mejora la calidad de vida de pacientes y familiares. Estos cuidados son esenciales desde el diagnóstico, independientemente de la intención curativa del tratamiento.
Los cuidados paliativos pueden extenderse a domicilio, proporcionando analgesia y apoyo psicosocial. La disponibilidad de morfina oral y otros analgésicos es crucial para el manejo del dolor oncológico moderado o intenso.
Respuesta de la OMS
En 2018, la OMS lanzó la Iniciativa Mundial contra el Cáncer Infantil, ofreciendo orientación y asistencia técnica para mejorar la atención oncológica pediátrica. El objetivo es alcanzar una tasa de supervivencia de al menos el 60% para 2030, duplicando la cifra actual y salvando un millón de vidas adicionales en la próxima década.
El Marco CureAll proporciona recursos para evaluar capacidades, establecer prioridades e implementar protocolos terapéuticos. La Plataforma Mundial por el Acceso a los Medicamentos contra el Cáncer Infantil, lanzada en 2021, busca asegurar el suministro continuo de fármacos pediátricos de calidad.
La OMS, junto a la Agencia Internacional de Investigaciones sobre el Cáncer (CIIC) y otros socios, trabaja para:
- Reforzar el compromiso político contra el cáncer infantil.
- Apoyar la creación de centros oncológicos y redes regionales de calidad.
- Elaborar normas y herramientas para diagnóstico, tratamiento y cuidados paliativos.
- Mejorar el acceso a medicamentos y tecnologías esenciales.
- Evitar dificultades económicas y aislamiento social de las familias.
Avances Terapéuticos y Terapias Innovadoras
La investigación en nuevos tratamientos oncológicos ha revolucionado el manejo del cáncer, abordando sus características biológicas ("hallmarks"). Esto incluye fármacos dirigidos a vías de señalización intracelular, inhibidores del ciclo celular, anti-angiogénicos e inmunoterapia.
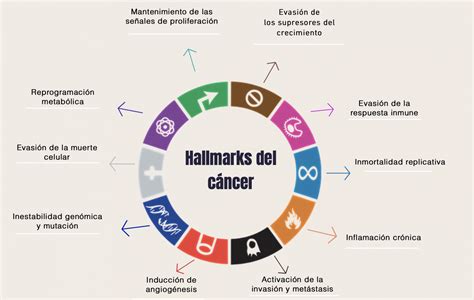
La inmunoterapia utiliza el propio sistema inmunitario del paciente para combatir el cáncer. Los anticuerpos monoclonales marcan células cancerosas para potenciar la respuesta inmune, como el blinatumomab. Las terapias de células CAR-T modifican genéticamente linfocitos T para que reconozcan y ataquen tumores específicos.
Las terapias dirigidas actúan sobre alteraciones genéticas específicas de los tumores. Los inhibidores del receptor de tirosina quinasa neurotrófico (NTRK) han revolucionado el tratamiento de tumores con estas alteraciones. Los inhibidores de la quinasa del linfoma anaplásico (ALK), como el crizotinib, han mostrado respuestas significativas en ciertos tumores.
Muchos fármacos oncológicos pediátricos se desarrollaron inicialmente para adultos, con un retraso considerable en su implementación en pediatría. La investigación en tumores exclusivamente pediátricos es un área de mejora.
Investigación Clínica y Ensayos Terapéuticos
Los ensayos clínicos son la principal herramienta para evaluar la seguridad y eficacia de nuevos tratamientos en humanos. Su complejidad requiere unidades especializadas con equipos multidisciplinarios experimentados.
La investigación farmacológica in vitro e in vivo mide la efectividad de nuevos fármacos contra células tumorales y analiza posibles mecanismos de resistencia.
La secuenciación masiva (NGS) y otras tecnologías de alta resolución permiten identificar alteraciones genéticas secundarias que modulan el pronóstico y abren nuevas posibilidades terapéuticas.
Tratamiento Multimodal y Quimioterapia
El tratamiento multimodal del cáncer infantil combina cirugía, radioterapia para control local y quimioterapia para erradicar la enfermedad sistémica. Los protocolos de quimioterapia utilizan combinaciones de fármacos con diferentes mecanismos de acción.
La quimioterapia combinada, administrada simultánea o secuencialmente, aumenta la remisión y prolonga su duración, superando la resistencia a fármacos aislados. La quimioterapia adyuvante se administra tras el control local del tumor para eliminar micrometástasis, siendo eficaz en tumores pediátricos frecuentes. La quimioterapia neoadyuvante, administrada antes del tratamiento local, reduce el tamaño tumoral y facilita la cirugía o radioterapia.
Las quimioterapias de rescate se emplean en caso de recaída, utilizando fármacos con mecanismos de acción diferentes a los previos.
Resistencia a la Quimioterapia
La resistencia a citostáticos es la principal causa de fracaso terapéutico en el cáncer infantil. Puede ser intrínseca o adquirida, y afectar a uno o múltiples fármacos (resistencia a múltiples drogas).
Mecanismos como el aumento de la eliminación del fármaco fuera de la célula (ej. glicoproteína P - gp-P) contribuyen a la resistencia. Se investigan quimiosensibilizantes para superar estos mecanismos, aunque los efectos tóxicos de algunos fármacos limitan su uso.
Modificación de Fármacos y Nuevas Formulaciones
La modificación de agentes quimioterápicos existentes busca mejorar sus perfiles farmacocinéticos, distribución tisular, eficacia y/o reducir toxicidades. Esto incluye:
- Asociación con polietilén glicol (pegilación): Prolonga la vida media de fármacos como la asparraginasa (pegaspargasa), reduciendo su inmunogenicidad y frecuencia de administración.
- Encapsulación liposomal: Disminuye la toxicidad de fármacos como la doxorrubicina (doxorrubicina liposomal) y la anfotericina B.
Los análogos de nucleósidos modificados, como la citarabina encapsulada (Depocyte®), mejoran el perfil terapéutico y reducen la toxicidad en administración intratecal.
Terapias Moleculares Dirigidas
Las terapias moleculares dirigidas actúan sobre moléculas específicas implicadas en la división y crecimiento tumoral. Ejemplos incluyen inhibidores de tirosina quinasa como el imatinib. La identificación de alteraciones genéticas específicas permite el desarrollo de tratamientos personalizados.
La detección de mutaciones como BRAF-V600E y reordenamientos en el gen ALK ha abierto nuevas vías terapéuticas para diversos tumores pediátricos.
Bases Genéticas del Cáncer Infantil
El cáncer infantil es una enfermedad genética rara, causada por la acumulación de cambios en el ADN que transforman células sanas en tumorales. Estos cambios pueden ser somáticos (específicos del tumor) o germinales (hereditarios).
Los Síndromes de Predisposición a Cáncer (SPCs), causados por mutaciones germinales, aumentan significativamente el riesgo de desarrollar tumores. La identificación de un SPC es compleja debido a la penetrancia incompleta y mutaciones de novo, pero es clave para el manejo clínico individualizado.
La identificación de mutaciones "drivers" (altamente implicadas en la oncogénesis) y alteraciones secundarias es crucial para el diagnóstico, pronóstico y aproximación terapéutica, especialmente con el avance de tecnologías como la secuenciación masiva (NGS).
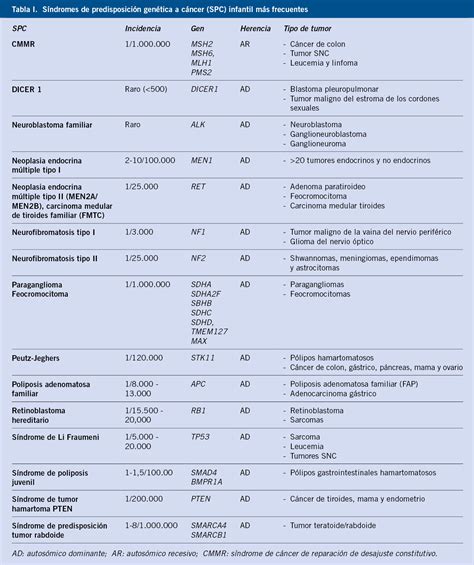
La caracterización genética permite diferenciar subtipos moleculares en tumores aparentemente idénticos y detectar mutaciones sensibles o resistentes a fármacos dirigidos.
Evolución y Estadística del Cáncer Infantil
Los avances terapéuticos han reducido la mortalidad por cáncer infantil en casi un 60% desde los años 60. Sin embargo, el cáncer sigue siendo la principal causa de muerte por enfermedad en niños y adolescentes.
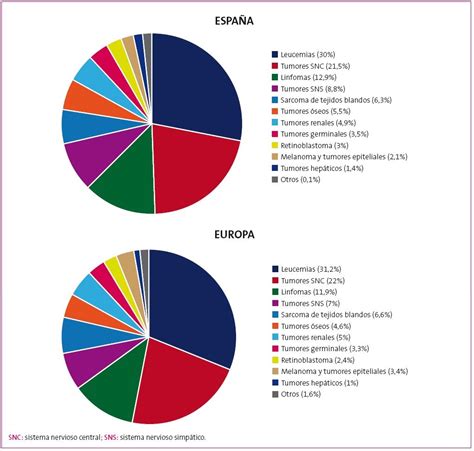
En España, se diagnostican aproximadamente 1.100 nuevos casos anuales en niños de 1 a 14 años. La leucemia aguda es el cáncer infantil más frecuente (30%), seguida por tumores del sistema nervioso central (21,7%) y linfomas (12,7%).
La supervivencia a 5 años del diagnóstico en España se acerca al 80%, resultados comparables a los de Estados Unidos y Europa. Tumores como el linfoma de Hodgkin, nefroblastomas, retinoblastomas y tumores germinales gonadales presentan supervivencias superiores al 90%.
Ejemplo Clínico: Leucemia Linfoblástica Aguda con Síndrome de Li-Fraumeni
Se presenta el caso de un varón de 14 años con sospecha de leucemia, que tras diagnóstico de leucemia linfoblástica aguda (LLA) con cariotipo hipodiploide, se derivó a consulta de predisposición a cáncer infantil. El estudio genético reveló una variante patogénica en el gen TP53, confirmando el síndrome de Li-Fraumeni. Este síndrome incrementa el riesgo de desarrollar otros tipos de cáncer a lo largo de la vida, requiriendo seguimiento específico que incluye exámenes físicos periódicos, estudios de imagen y colonoscopias.